导读
大分子递送到体外和体内细胞是许多治疗方法的关键。目前,基因编辑面临递送工具到目标细胞的挑战,AAV载体存在负载大小限制和脱靶编辑等问题,LNPs虽减少脱靶,但在肝外组织应用仍有难度。因此,急需开发新递送策略。
刘如谦团队之前研究了类病毒颗粒(VLPs)作为基因编辑载体,VLPs不含病毒基因组,结合了病毒递送的高效性和非病毒递送的暂时性优点。
他们开发的工程化VLPs(eVLPs)实现了高效蛋白递送和基因编辑,特别是在小鼠肝脏和视网膜中。通过优化eVLPs,提高了体内碱基编辑效率并减少了脱靶。此外,他们开发的prime editor(PE)-eVLPs实现了安全的体内递送。
为进一步提高eVLP性能,研究团队计划改进包装效率和递送效率,并通过定向进化优化eVLP变体。
2024年11月13日,博德研究所David R. Liu(刘如谦)团队在Nature Biotechnology上发表了一篇题为“Directed evolution of engineered virus-like particles with improved production and transduction efficiencies”的论文,开发了一个定向进化系统,通过带有barcode的sgRNA识别唯一的eVLP变体,筛选到了具有更好RNP包装、释放及递送效率的v5 eVLPs,为改进eVLPs提供了基础。

文章索引
【IF】46.9
研究结果
一. 带有barcode的sgRNA可识别具有不同特性的eVLPs
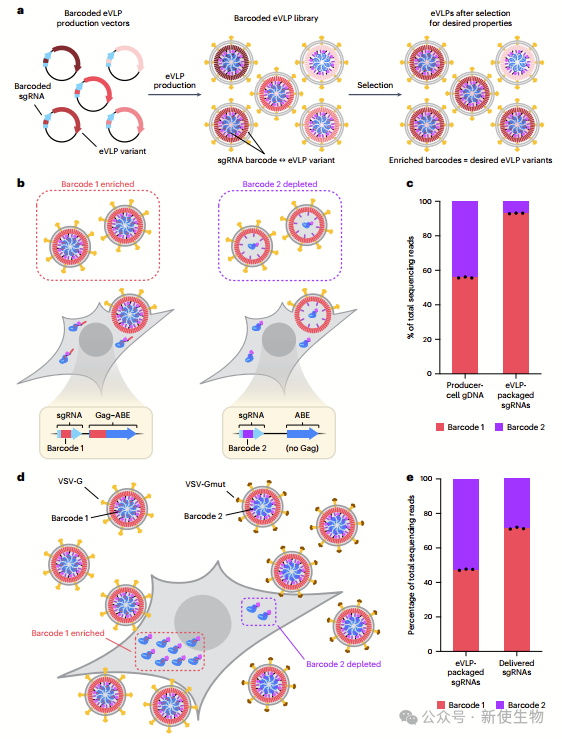
作者开发了一种定向进化系统,利用带有barcode的引导RNA(sgRNA)唯一标识每个eVLP变体。通过将带有barcode的sgRNA与eVLP变体共同表达,并经过选择后,通过测序识别优选变体。
在模拟选择实验中,证明了此方法能有效区分具有不同功能的eVLP变体,验证了该系统的有效性,为筛选具有期望特性的eVLP变体提供了新的方法。
二. 突变并筛选带有barcode的eVLP衣壳库
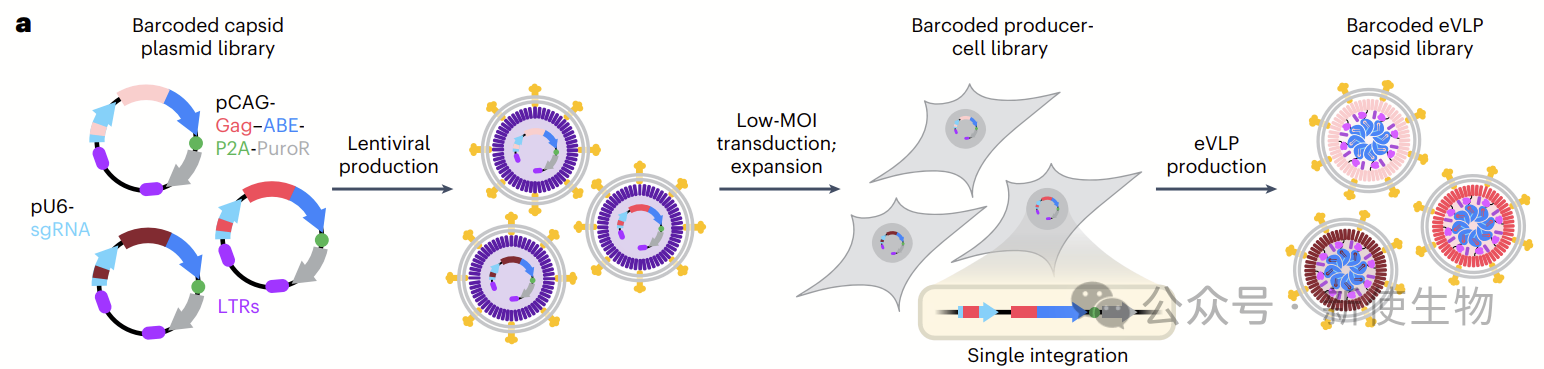
作者应用进化系统,突变并筛选了eVLP衣壳,以提高其包装ABE RNP货物的能力。
通过构建了一个包含3762个MMLV Gag蛋白突变体的barcoded eVLP衣壳库,并通过低MOI转导生产细胞,成功生成了带有barcode的eVLP生产细胞库。
高通量测序分析显示99%的barcode序列被检测到,为eVLP进化实验奠定了基础。
三. 筛选结果揭示了衣壳突变体如何影响eVLP特性
作者对barcoded VLP衣壳突变库进行了两次筛选,分别针对eVLP生产和转染效率进行优化。约8%的突变体在生产效率上优于经典eVLP衣壳,而0.7%的突变体提高了效率。
大多数突变体在生产和转染上表现不佳,少数突变体则在某一方面有所改善,表明eVLP生产和转染效率受不同机制调控。

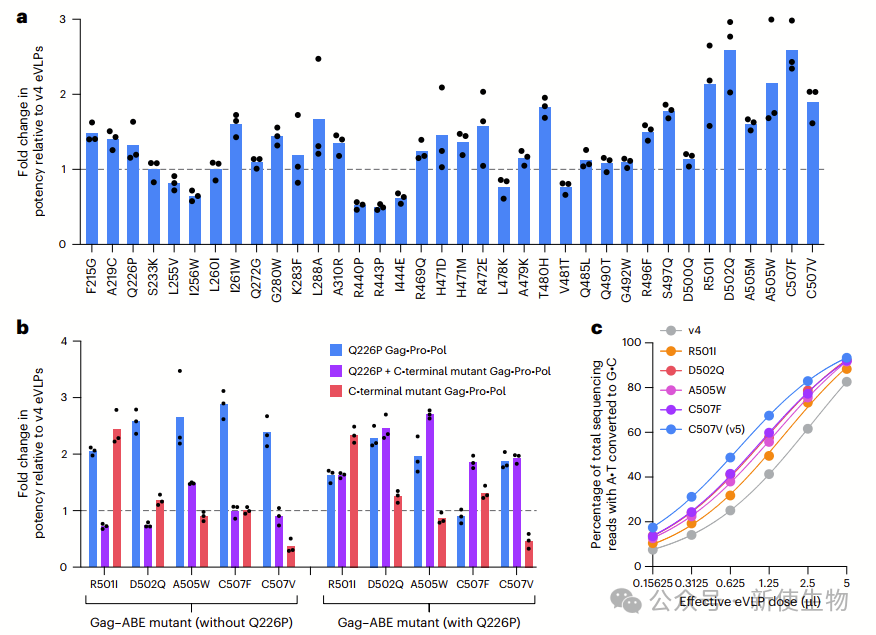
四. 衣壳突变组合提高eVLP效能
通过对36种衣壳突变体的筛选和组合优化,作者发现GagC507V–ABE与GagQ226P–Pro–Pol组合(v5 BE-eVLPs)显著提高了eVLP的基因编辑效能,比v4 BE-eVLPs提高了3.7倍。
在小鼠细胞中,v5 BE-eVLPs也表现出更低的剂量需求,提升了效能。这些结果为提高eVLP的基因编辑效能提供了新的突变组合,并具有重要的应用潜力。

五. v5 eVLPs提升人类初级造血干细胞中的碱基编辑效能
v5 BE-eVLPs在初级人类造血干细胞中的碱基编辑效能比v4 BE-eVLPs提高2.6倍,且最低剂量即可达到v4的最高效能。
重要的是,v5 eVLPs不影响HSPC的存活性,显示出在大规模应用中的潜力。

六. v5 eVLPs表现出更好的负载和释放效果
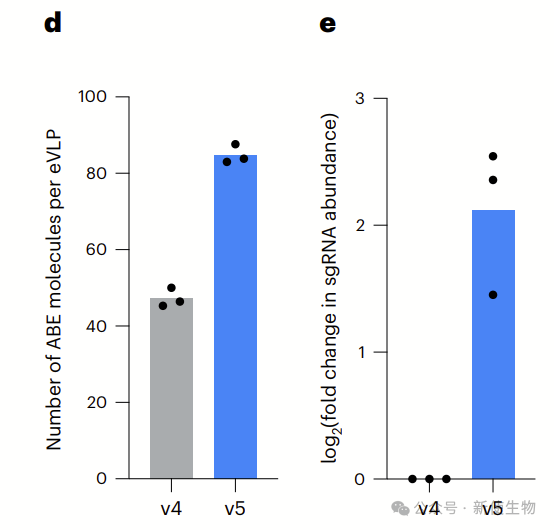
v5 eVLPs通过Q226P和C507V突变改善了负载和释放。Q226P突变影响外壳成熟过程,优化大分子RNP包装,而C507V突变破坏了核衣壳结构中的锌指域,去除病毒基因组包装功能,促进RNP包装。
实验显示,v5 eVLPs在ABE蛋白和sgRNA包装量上分别提高1.8倍和4.3倍,且具有更高效的负载释放能力,显著提升了基因编辑效能。

七. v5 eVLPs表现出外壳结构和颗粒大小的变化
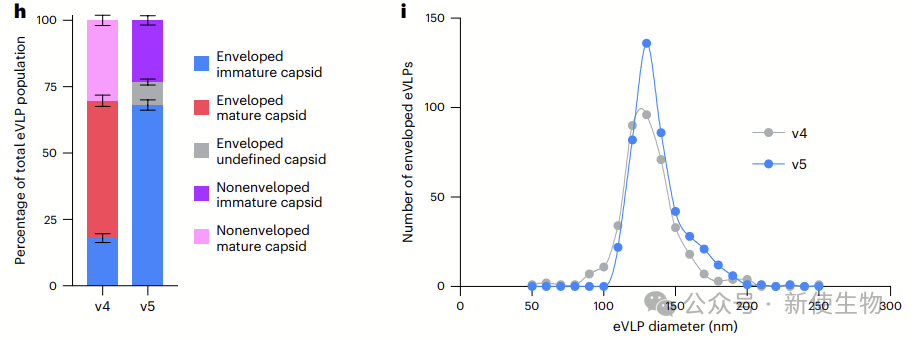
通过冷冻电镜分析,v4 eVLPs存在三种主要的衣壳结构:包膜未成熟、包膜成熟和无包膜成熟,而v5 eVLPs则主要呈现包膜未成熟、包膜不明确和无包膜未成熟结构。
v5 eVLPs缺乏成熟衣壳,可能通过未成熟衣壳提高了RNP载体的递送效率。此外,v5 eVLPs的平均直径较v4 eVLPs略大,可能能容纳更多货物。

总结
本文开发了一种eVLP进化系统,通过带有barcode的引导RNA标记变体,筛选出具有改进特性的eVLP。通过优化衣壳突变,开发了第五代(v5)eVLP,展示出比v4 eVLPs高2-4倍的递送效能。
超高的准确性为研究非经典的开放阅读框(ORFs)提供极大便利,提高微肽(肿瘤新生抗原)的挖掘效率。
简便快速的操作让翻译组分析不再设有门槛,每位科研学者都能轻松上手。
另外新使生物提供多物种多聚核糖体分析(Polysome profiling),了解更多翻译组技术信息可登录杭州新使生物技术有限公司

感谢关注新使生物,翻译组测序可以联系新使生物


 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们