
导读
自mRNA 疫苗在新冠疫情中展现出强大潜力以来,mRNA 技术已成为再生医学领域的重要突破口。传统再生疗法如细胞移植、基因治疗和重组蛋白递送,分别面临细胞存活低、基因组整合风险高、蛋白半衰期短等局限,而mRNA 具有无需核转位、瞬时表达、无插入突变风险等优势,为解决这些难题提供了新方向。
近年来,mRNA 化学修饰、转录本工程和纳米递送技术的进步,有效克服了 mRNA 固有的不稳定性、免疫原性等问题,使其在蛋白补充、细胞重编程和转分化等再生场景中实现精准应用。
2025年8月30日,哈佛大学医学院陶伟团队在Cell Biomaterials上发表了题为 “mRNA-based technology for engineered regenerative medicine” 的综述文章,系统总结了mRNA 技术在再生医学中的优化策略、应用场景及转化进展,深入分析当前挑战并提出未来方向。
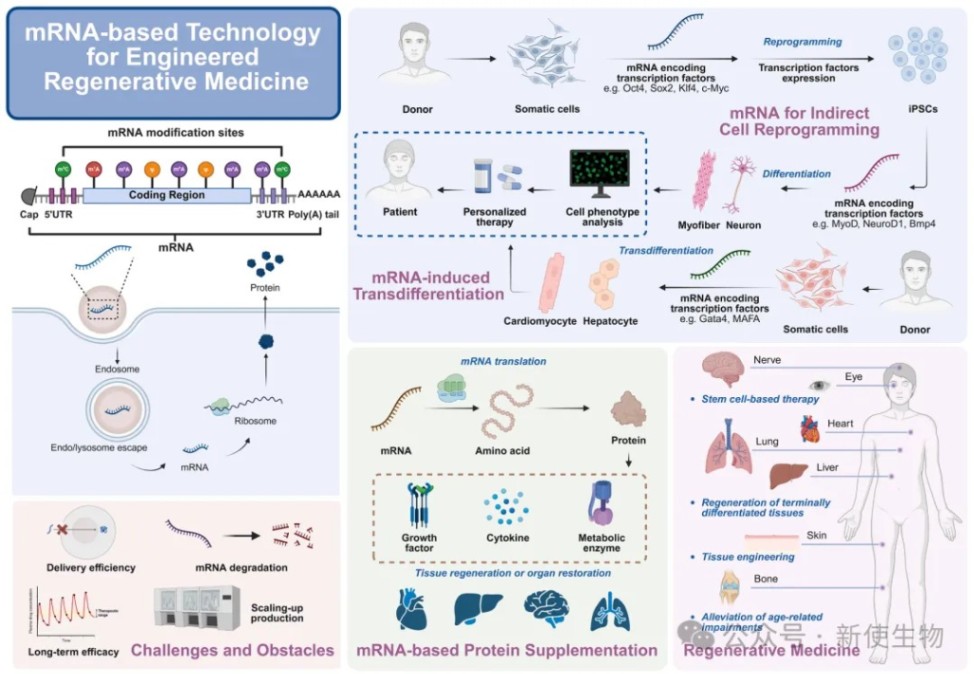
综述整理
一、驱动组织再生的mRNA化学修饰
为了应用于再生医学,科学家们对mRNA的稳定性、翻译效率和免疫原性进行了大量优化。
1.1)mRNA结构优化
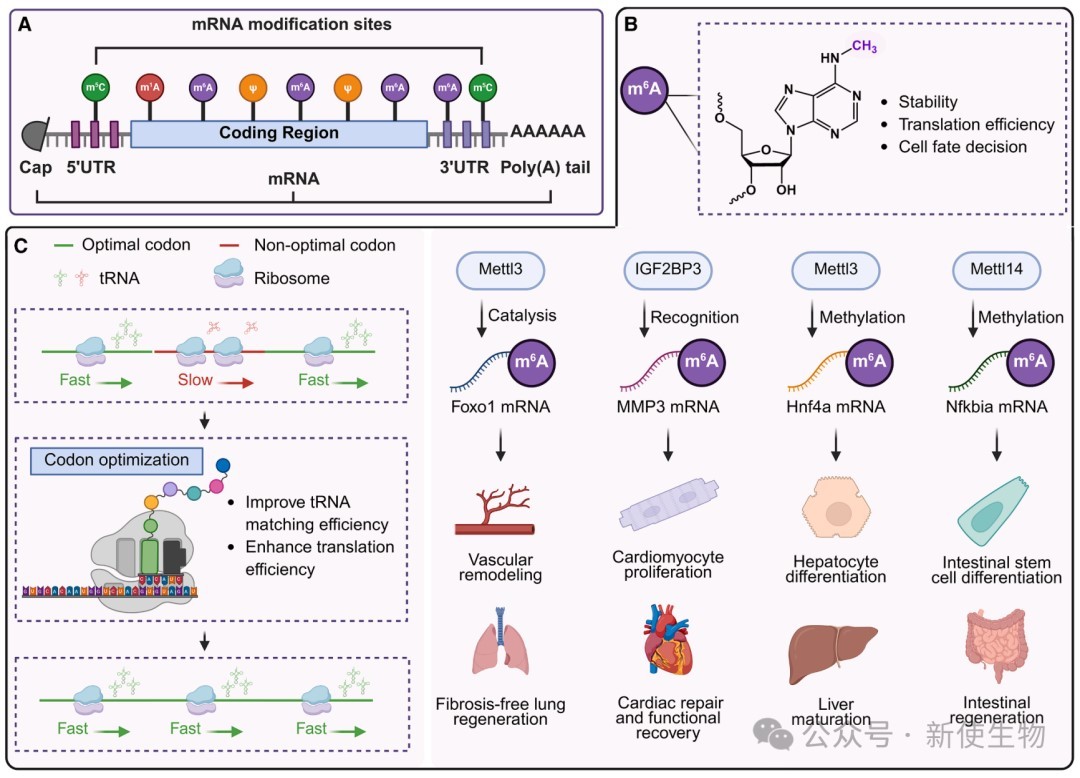
mRNA的关键结构元件,包括5′端帽、5′和3′非翻译区(UTR)、编码序列和poly(A)尾,都经过工程化改造以增强其功能。
例如,优化加帽结构(如Cap1)能保护mRNA免于降解并促进翻译起始。
1.2)核苷酸化学修饰
将天然核苷酸替换为化学修饰的核苷酸,如假尿苷 (Ψ)、5-甲基胞苷 (m5C) 和N1-甲基腺苷 (m1A),能显著降低mRNA的免疫原性并提高其稳定性。
1.3)m6A修饰的关键作用
N6-甲基腺苷 (m6A) 作为mRNA上最普遍的修饰,在组织再生中扮演核心调控角色,它能动态调节mRNA的稳定性、剪接和翻译,从而精细调控基因表达。
m6A修饰在血管重塑、心脏修复、肝脏发育和肠道干细胞存活等多个再生过程中都极为重要。
1.4)密码子优化
通过优化mRNA编码区的密码子,可以在不改变蛋白质序列的情况下显著提高翻译效率,从而用更低的剂量达到理想的治疗效果。
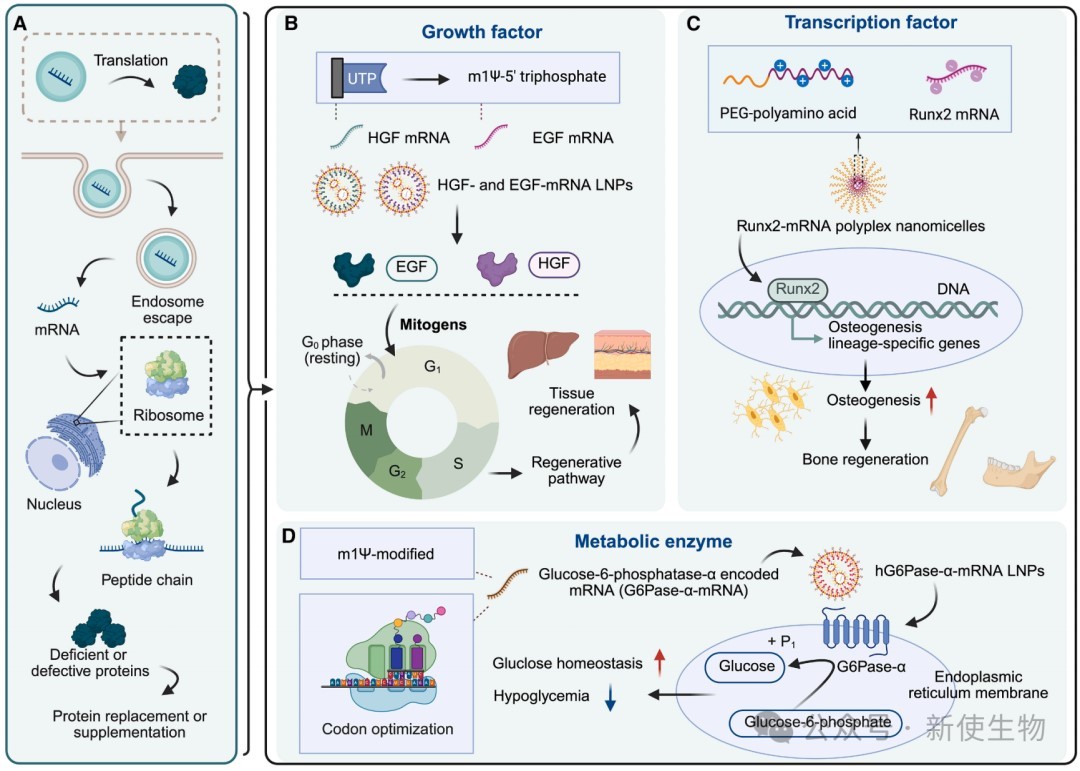
二、基于mRNA的蛋白质替代或补充疗法
mRNA技术提供了一种创新的蛋白质疗法,通过在体内细胞中直接翻译生成所需蛋白质,克服了重组蛋白半衰期短和病毒载体存在安全风险的局限。
2.1)生长因子
利用mRNA在局部瞬时表达生长因子,可有效促进组织修复。
HGF和EGF:递送编码肝细胞生长因子(HGF)和表皮生长因子(EGF)的mRNA-LNP,能有效逆转肝脏脂肪变性,加速肝再生并恢复肝功能。
IGF-1:局部递送胰岛素样生长因子1(IGF-1)的mRNA,可有效促进骨骼肌再生,且避免了全身给药的副作用。
VEGFC/VEGFA:血管内皮生长因子C(VEGFC)的mRNA疗法可促进淋巴管再生,用于治疗淋巴水肿;VEGFA的mRNA则能修复肺部或心脏的血管损伤。
BMP-2:骨形态发生蛋白-2(BMP-2)的mRNA可高效促进大段骨缺损的愈合,且效果优于重组蛋白。
2.2)转录因子
通过mRNA表达关键转录因子,可调控细胞分化和组织形成。例如,递送编码Runx2的mRNA可显著增强骨再生和矿化。
2.3)代谢酶
对于因酶缺陷导致的代谢性疾病,mRNA疗法可提供功能性酶以恢复代谢平衡。
G6Pase-α:针对Ia型糖原累积病的G6Pase-α mRNA疗法,可恢复肝脏中的酶活性,纠正低血糖。
PCCA/PCCB:针对丙酸血症的mRNA-3927疗法,通过递送编码PCCA和PCCB亚基的两种mRNA,已在临床试验中显示出恢复酶活性的潜力。
2.4)结构蛋白
mRNA还可用于补充结构蛋白。例如,通过细胞外囊泡递送编码I型胶原蛋白(COL1A1)的mRNA,可有效补充光老化皮肤中损失的胶原蛋白,减少皱纹形成。
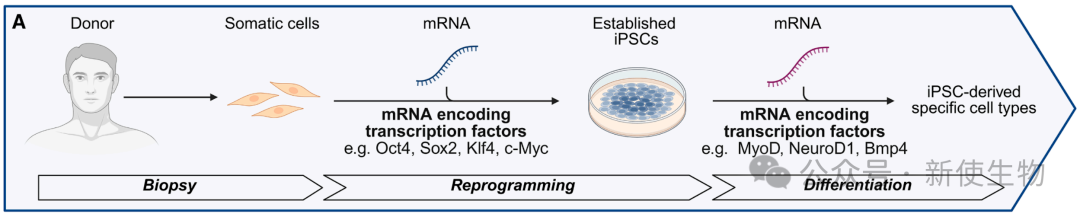
三、mRNA介导的间接细胞重编程
间接重编程指将体细胞诱导为诱导性多能干细胞(iPSCs),再将其定向分化为所需细胞类型。
mRNA技术以其瞬时、无整合、高效率的特点,成为生成iPSCs及其衍生物的安全工具。
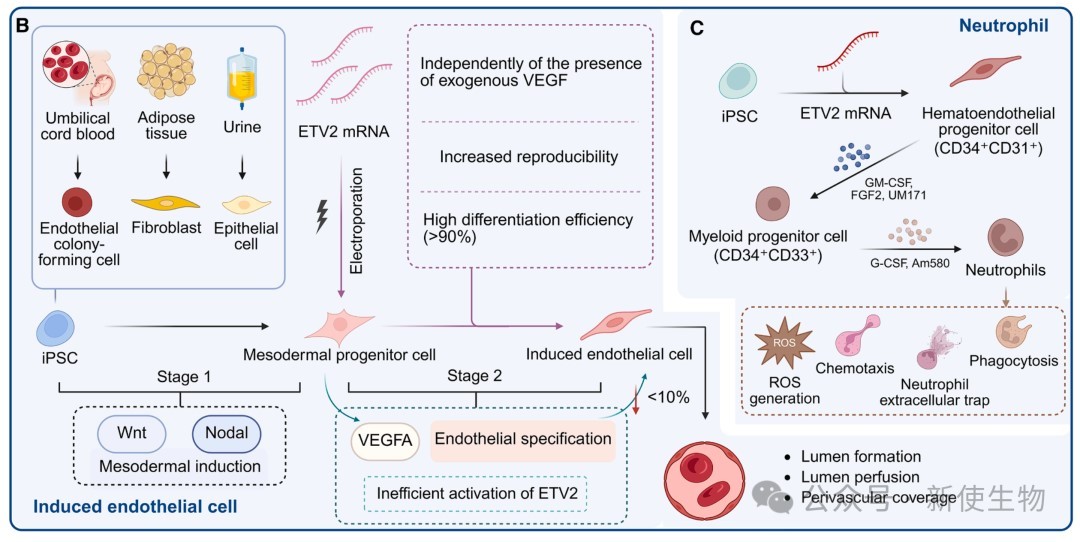
3.1)h-iPSC衍生的内皮细胞
通过递送编码关键转录因子ETV2的mRNA,可以高效、均一地将h-iPSCs中间体分化为功能性内皮细胞,促进体内血管形成。
3.2)h-iPSC衍生的中性粒细胞
利用ETV2的mRNA驱动h-iPSCs向造血内皮祖细胞分化,再结合细胞因子,可在14天内高效生成具有完全功能(如趋化、吞噬)的中性粒细胞。
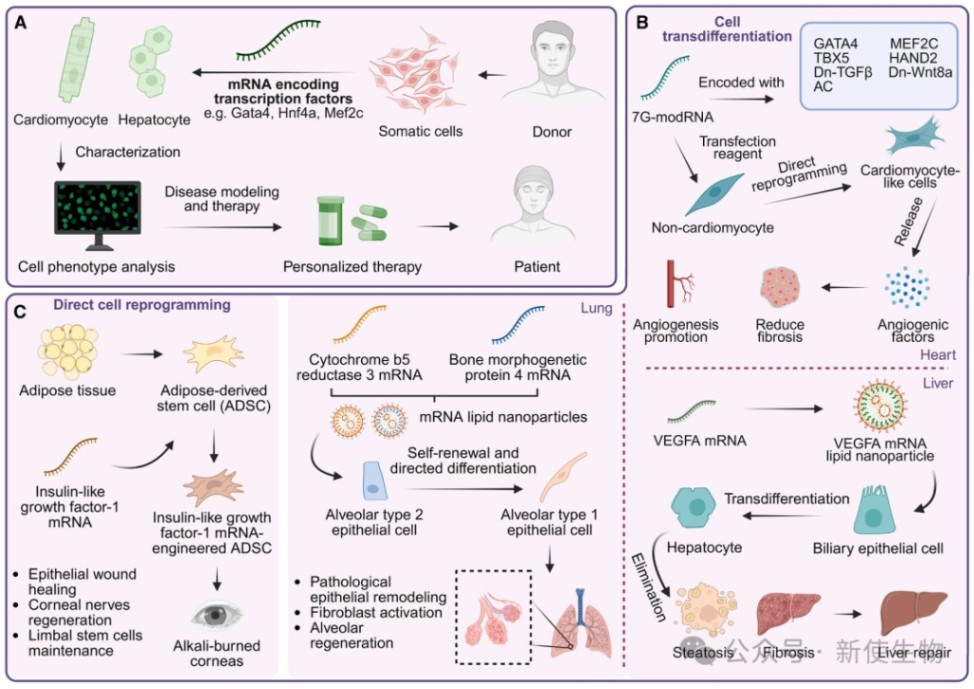
四、mRNA诱导的细胞转分化与直接细胞重编程
mRNA能够直接将一种体细胞转化为另一种功能细胞(转分化),或增强干细胞的治疗潜力,从而绕过iPSC阶段,简化治疗流程。
4.1)细胞转分化
“7G-mRNA”鸡尾酒疗法(编码Gata4, Mef2c, Tbx5等7个因子)可将非心肌细胞重编程为心肌样细胞,用于心脏修复。
VEGFA mRNA可诱导胆管上皮细胞转分化为肝细胞,促进肝脏再生。
CYB5R3和BMP-4 mRNA可恢复肺泡II型(AT2)细胞的干性,促进肺泡再生。
4.2)直接细胞重编程
IGF-1 mRNA修饰的脂肪干细胞(ADSC)能显著加速角膜损伤的修复,展现出更强的再生能力。
五、总结与展望
尽管mRNA再生医学取得突破,仍需优化持续表达、组织靶向、长期稳定性与免疫副作用。未来可通过AI/ML优化RNA设计,结合水凝胶、支架等多材料平台实现精准控释,并用单细胞与空间转录组锁定关键靶点。此外,环状RNA(circRNA)和自扩增RNA(saRNA)等新型RNA药物正在成为提高表达稳定性与治疗持续性的热点方向。
| 新使生物专业翻译组一站式服务平台 |
| 产品名称 |
点击图片查看
点击图片查看


 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们
