
导读
线粒体是细胞的能量工厂,其绝大多数蛋白质由核基因组编码,在细胞质中合成后被转运至线粒体内部。传统观点认为,这一转运过程主要发生在蛋白质完整合成之后。
然而,越来越多的证据表明,一部分mRNA和核糖体会被招募到线粒体外膜附近。这种局部翻译机制被认为可以提高蛋白质转运效率、促进蛋白质复合物的正确组装。
在酵母等模式生物中,对该过程已有初步研究,但在哺乳动物中,线粒体局部翻译的普遍性、生理意义及其调控机制仍不清楚。阐明这些问题对于深入理解细胞区室化调控基因表达的复杂性至关重要。
2025年8月27日,美国怀特黑德生物医学研究所Jonathan S. Weissman团队在Cell上发表了一篇题为“Proximity-specific ribosome profiling reveals the logic of localized mitochondrial translation”的论文,开发了一种名为LOCL-TL的光遗传学新技术,能够以密码子级别的分辨率监测细胞内特定位置的蛋白质翻译过程,并揭示了哺乳动物细胞中存在两种截然不同且功能各异的线粒体蛋白局部翻译机制。

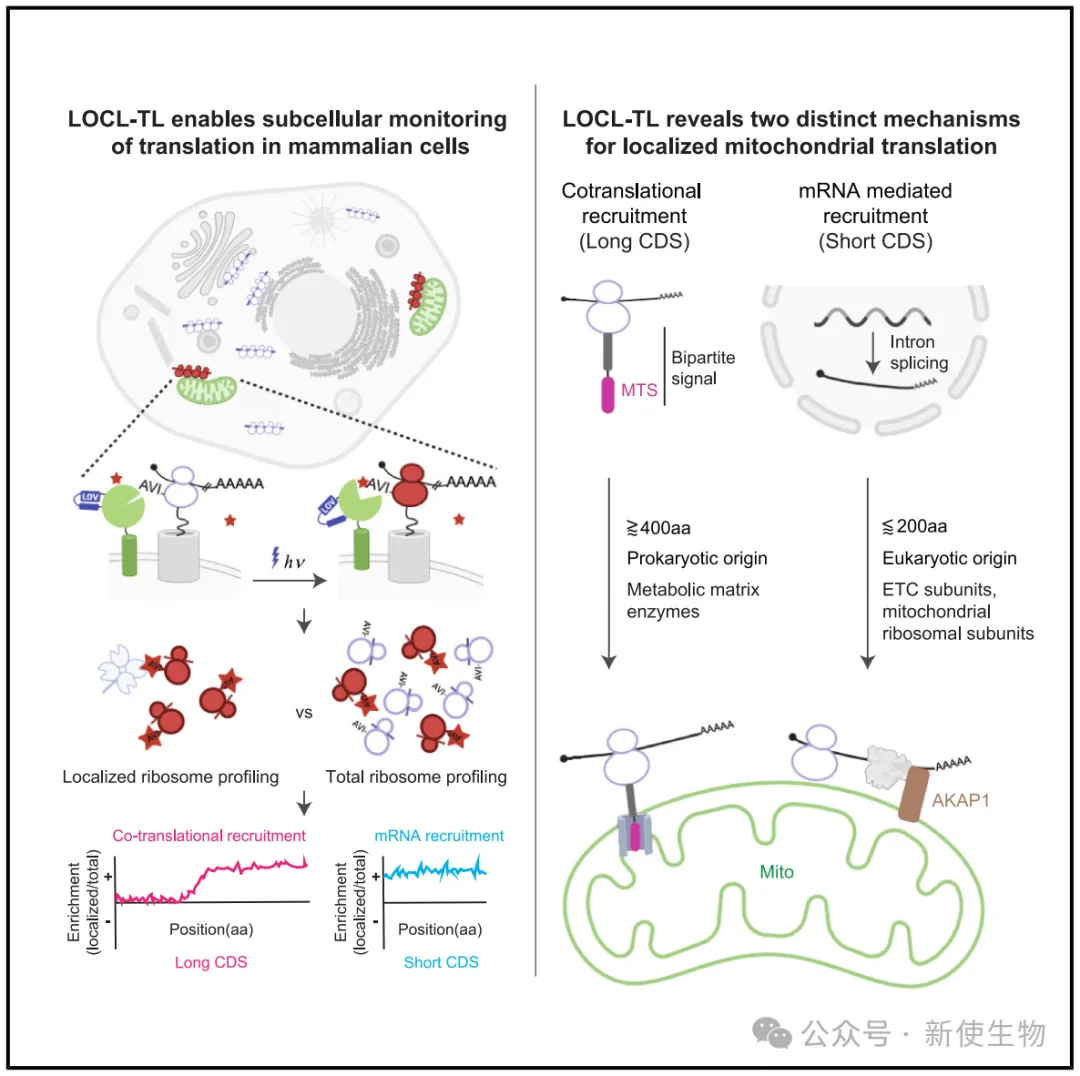
文章索引
【标题】Proximity-specific ribosome profiling reveals the logic of localized mitochondrial translation
【发表期刊】Cell
【发表日期】2025年8月27日
【作者及团队】美国怀特黑德生物医学研究所Jonathan S. Weissman团队
【IF】42.5
研究结果
一、LOCL-TL技术的建立与验证
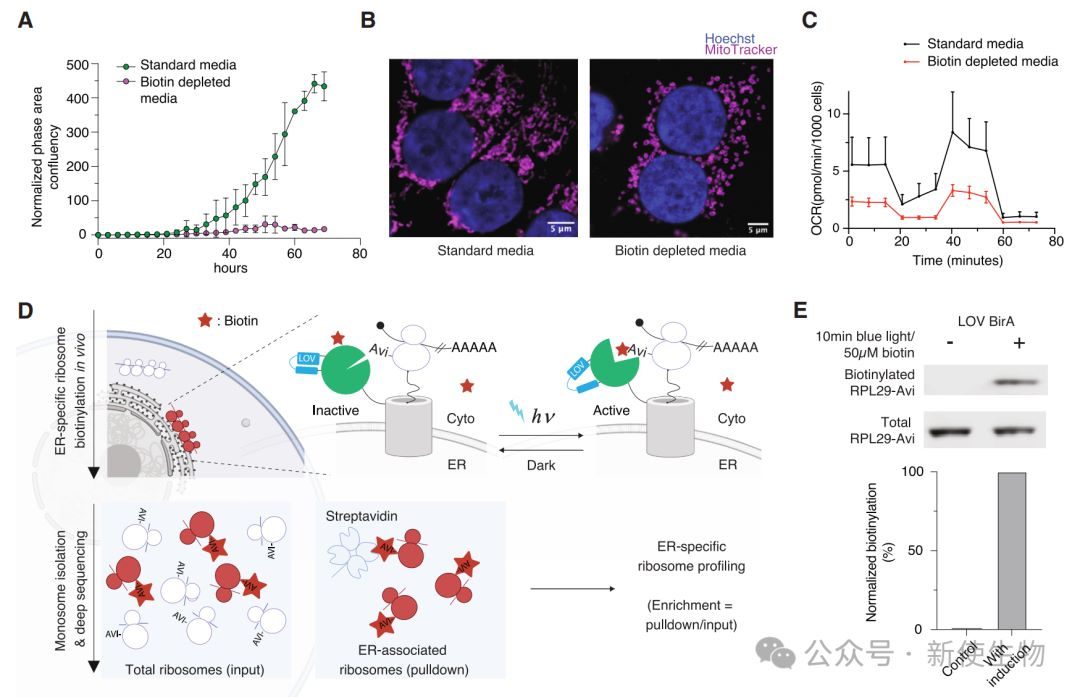
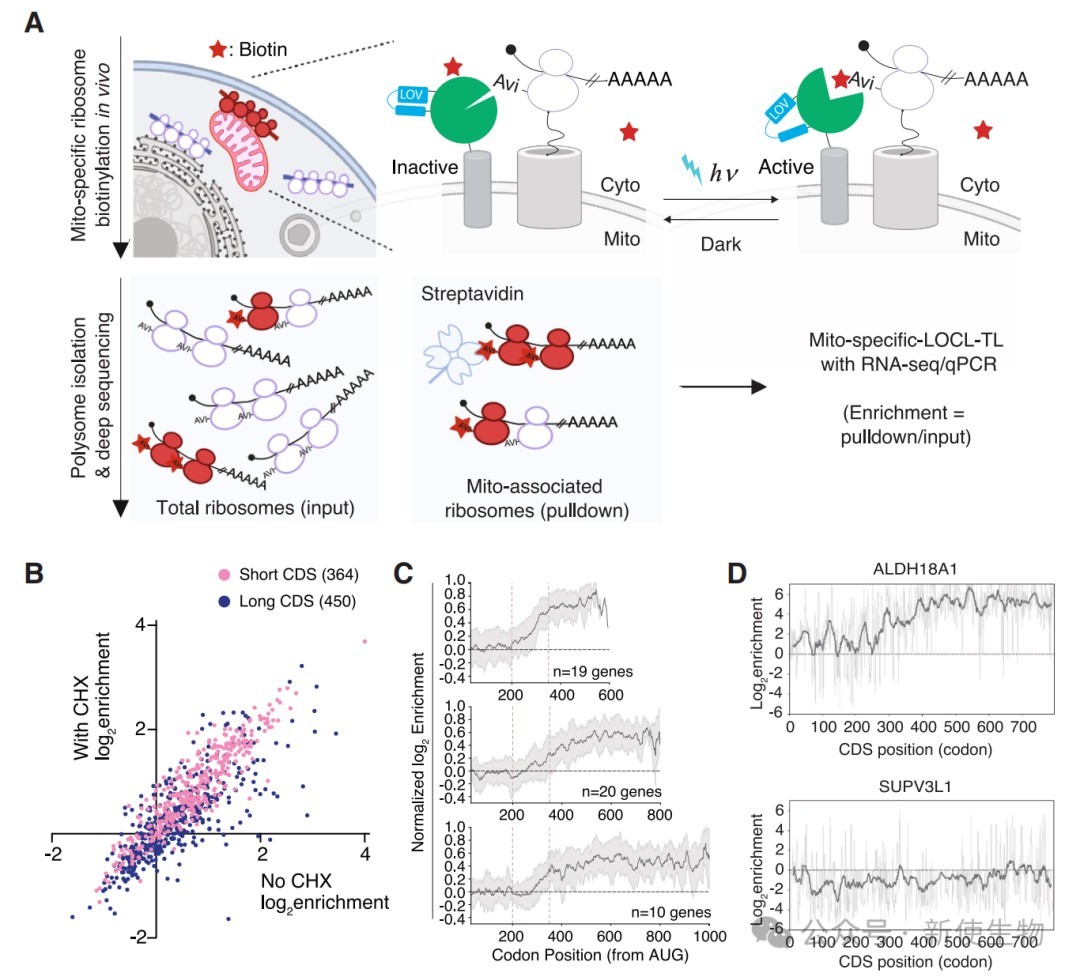
通过将光敏结构域LOV与生物素连接酶BirA结合,研究人员开发出一种可被蓝光精确调控的邻近标记工具(LOCL-TL)。
二、线粒体局部翻译图谱揭示了两类功能和长度迥异的蛋白质
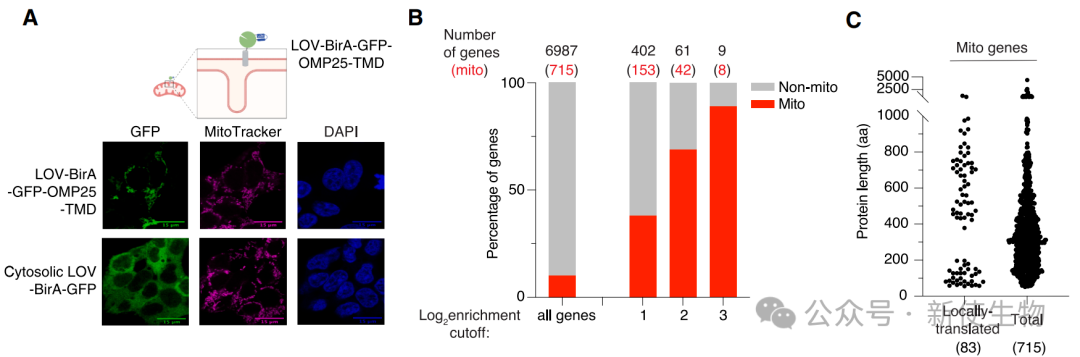
利用LOCL-TL技术,研究发现约20%的核编码线粒体蛋白在线粒体外膜上优先翻译。
这些蛋白可被显著分为两类,一类是编码序列(CDS)较短(<200氨基酸)的蛋白,主要富集为电子传递链(ETC)亚基。
而另一类是CDS较长(>400氨基酸)的蛋白,主要为代谢通路中的酶类。
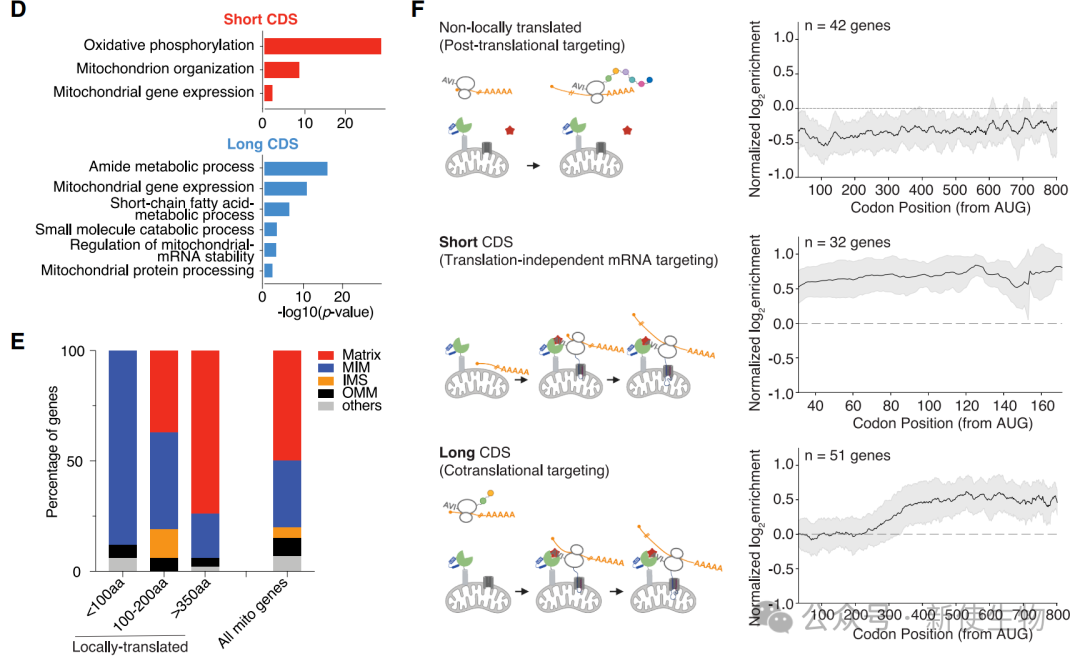
三、长短两类蛋白的线粒体招募机制截然不同
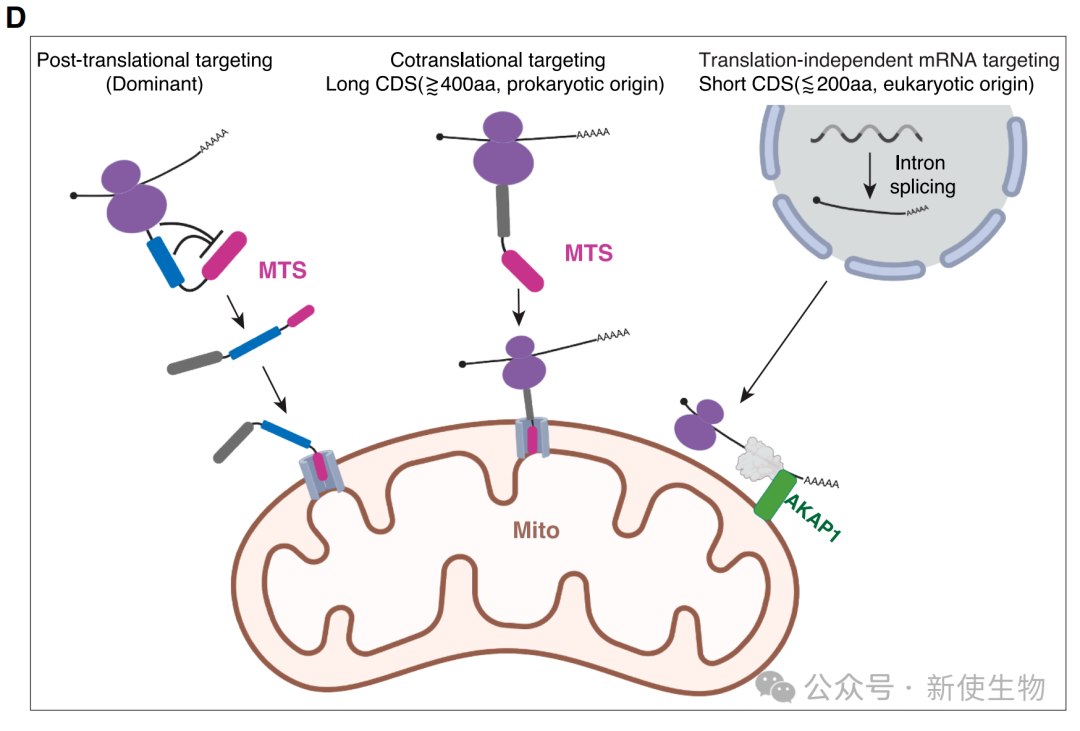
通过Ribo-seq核糖体印迹分析,研究发现长CDS蛋白在细胞质中开始翻译,待新生肽链长出约250个氨基酸后,核糖体-新生肽链复合物才被招募到线粒体表面。
相反,短CDS蛋白的mRNA转录本则在翻译开始前就已被靶向至线粒体。
四、新生肽链中的二分式信号介导长CDS蛋白的共翻译招募
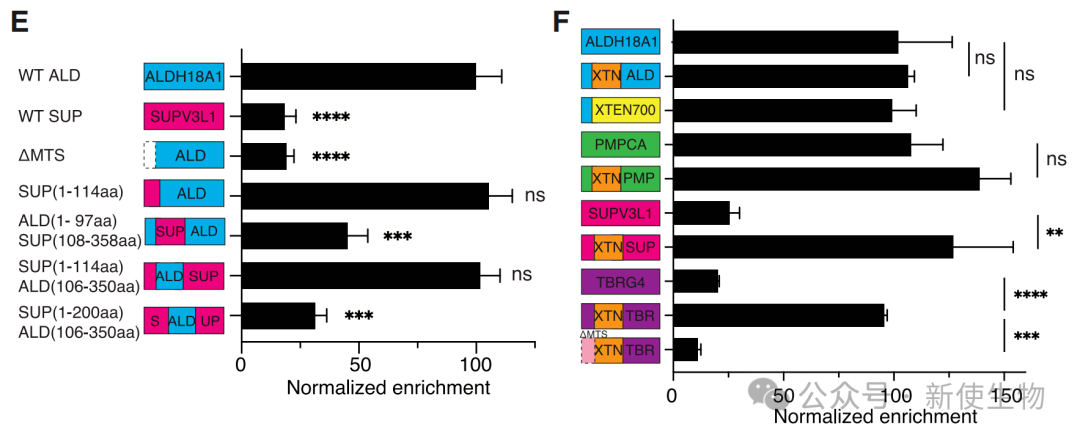
研究团队证实长CDS蛋白的共翻译招募依赖于其N端的一个“二分式信号”:一个经典的线粒体靶向序列(MTS)加上其下游一段非抑制性的氨基酸序列。
然而,翻译后输入的蛋白则在该区域含有一段“抑制性”序列,阻止其在翻译完成前与线粒体结合。
五、mRNA元件和内含子剪接决定短CDS转录本的线粒体定位
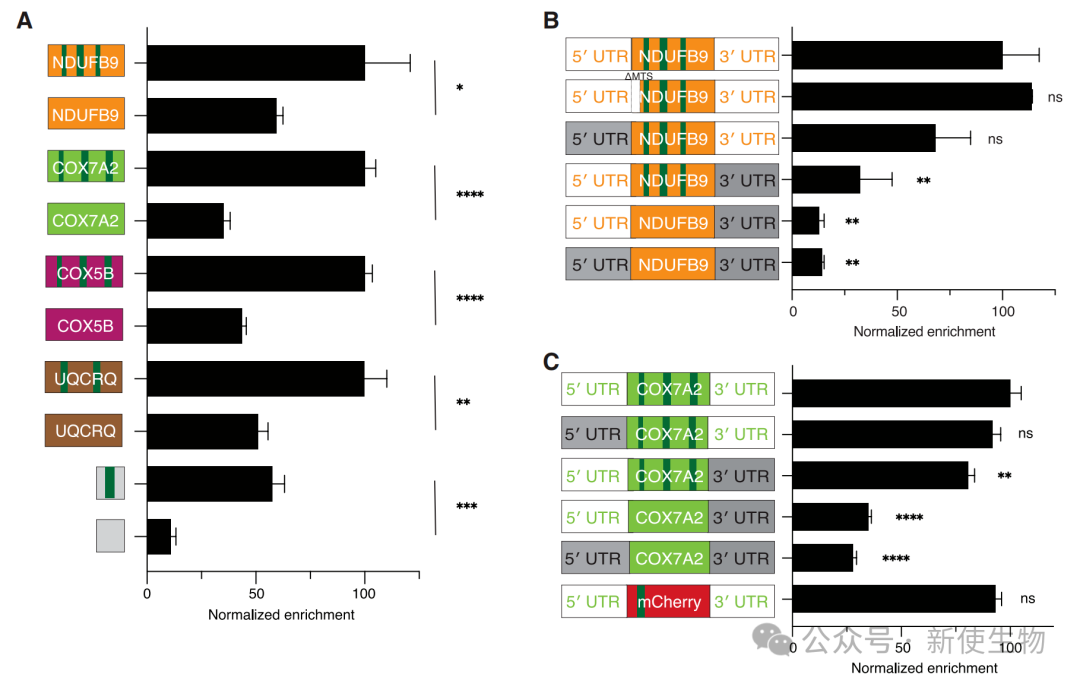
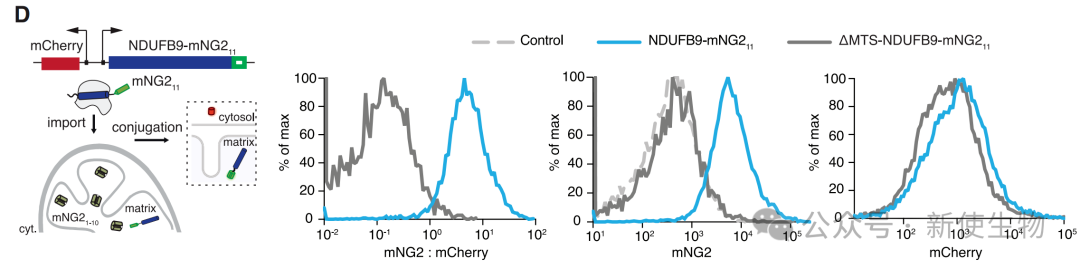
作者发现,与长CDS蛋白不同,短CDS蛋白的局部翻译由其mRNA决定。
其5' UTR、3' UTR以及内含子的存在是mRNA被招募到线粒体的充分必要条件,而蛋白质编码区本身及其是否含有MTS则与招募过程无关。
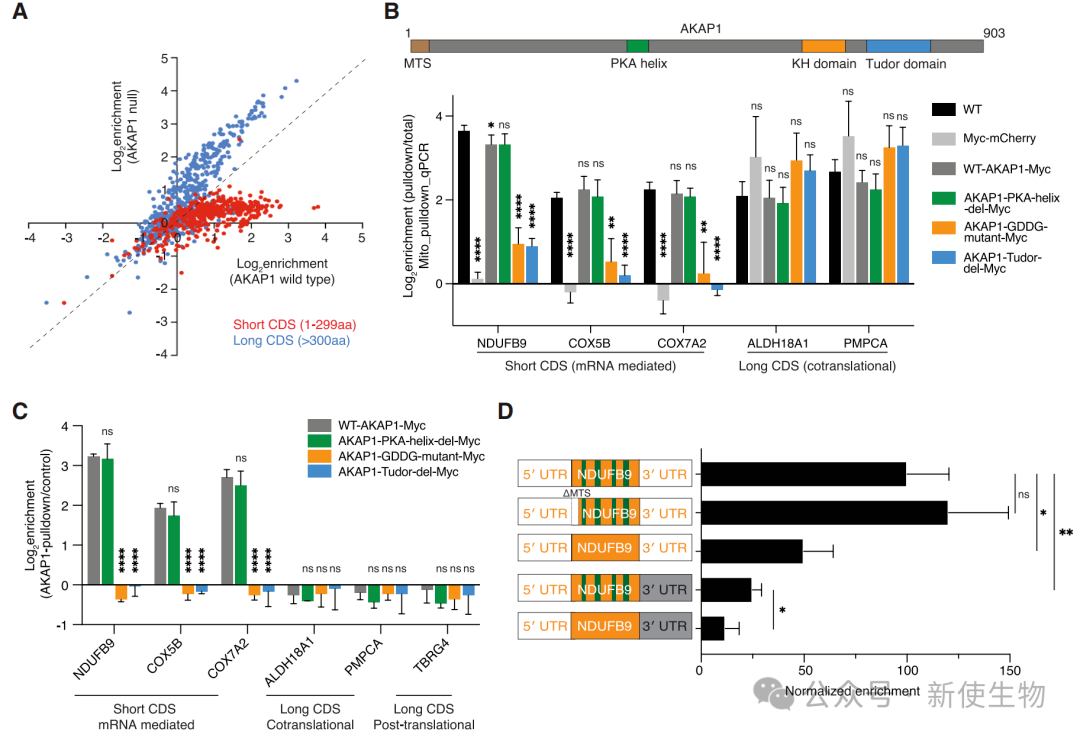
六、AKAP1蛋白是介导短CDS转录本线粒体招募的关键因子
通过基因敲除和回补实验,研究人员发现定位于线粒体外膜的RNA结合蛋白AKAP1是招募短CDS mRNA的关键。
AKAP1通过其RNA结合结构域直接与这些mRNA结合,敲除AKAP1会导致短CDS蛋白的局部翻译显著下降,蛋白水平也随之降低。
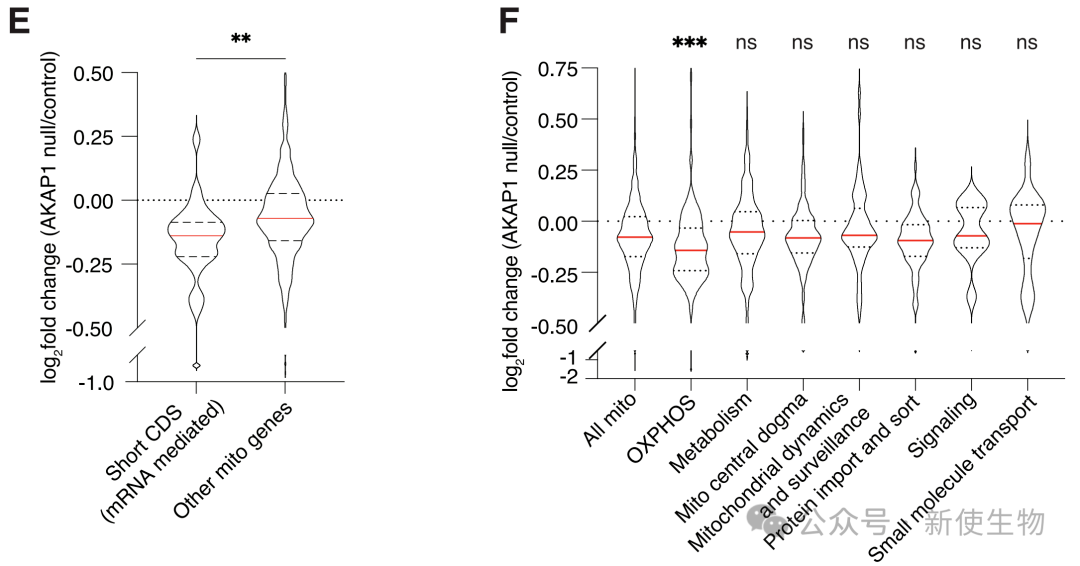
七、长CDS蛋白的局部翻译机制在进化上更为古老和保守
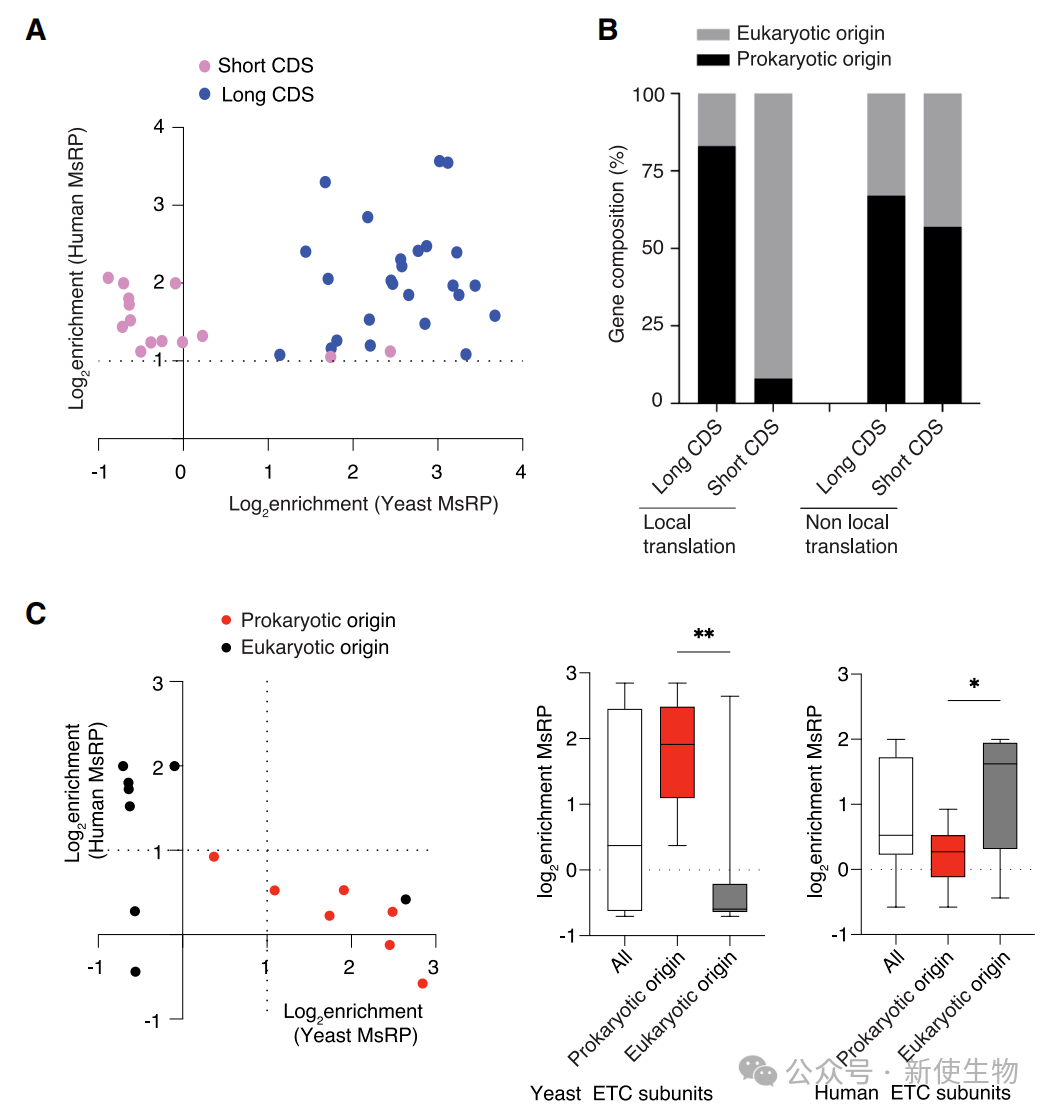
通过与酵母的数据进行比较,研究发现长CDS蛋白的共翻译招募机制在从酵母到人类的进化过程中是保守的。
然而,由AKAP1介导的短CDS蛋白mRNA招募机制在酵母中不存在,这可能是一种更晚近进化出的、用于精细调控高等生物呼吸链合成的策略。
总结
本研究通过开发光遗传技术LOCL-TL,揭示了哺乳动物细胞中存在两种并行的、在机制和进化起源上都截然不同的线粒体蛋白局部翻译通路。该发现不仅深化了对线粒体生物发生和代谢调控的理解,也为研究局部翻译在其他生理和病理过程中的作用提供了新的研究范式。
我们能够针对微量细胞或组织,如卵母细胞、卵巢、临床穿刺样品等产出高质量翻译组数据结果。
超高的准确性为研究非经典的开放阅读框(ORFs)提供极大便利,提高微肽(肿瘤新生抗原)的挖掘效率。
另外新使生物提供多物种多聚核糖体分析(Polysome profiling),了解更多翻译组技术信息可登录 www.neoribo.com
点击图片查看
点击图片查看


 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们
