
导读
去分化脂肪肉瘤(DDLPS)是一种罕见且具有高度侵袭性的恶性肿瘤,其主要驱动因素是一个维持肿瘤增殖的核心转录调控回路(CRC)。该疾病临床治疗面临巨大挑战,术后复发率和转移风险高,且缺乏有效的靶向治疗手段。
CRC是由主转录因子精心编排的整合遗传程序,它决定细胞身份并驱动恶性转化,并已被证实参与多种癌症的发生发展。DDLPS的CRC由MYC、FOSL2和RUNX等核心转录因子构成,这些因子的高效转录和前馈激活是导致DDLPS恶性特征的关键。
尽管已有研究表明XPO1在DDLPS中可能发挥作用,但其与DDLPS核心驱动因子CRC之间的具体联系尚不明确,因此亟需探索新的治疗策略。
2026年4月16日,浙江大学徐良和陈烨团队合作,在Oncogene上发表了题为“XPO1 inhibitor KPT-330 disrupts the core transcriptional regulatory circuitry of dedifferentiated liposarcoma by modulating the translation process”的研究论文。该研究发现XPO1抑制剂KPT-330通过双相机制(抑制翻译起始与延伸)破坏DDLPS的核心转录调控回路,并揭示了XPO1与核糖体蛋白及翻译起始因子之间的功能互作。


文章索引
【标题】XPO1 inhibitor KPT-330 disrupts the core transcriptional regulatory circuitry of dedifferentiated liposarcoma by modulating the translation process
【发表期刊】Oncogene
【发表日期】2026年4月16日
【作者及团队】浙江大学徐良和陈烨团队
【IF】7.3
研究结果
一、抑制XPO1功能可破坏DDLPS的CRC稳态
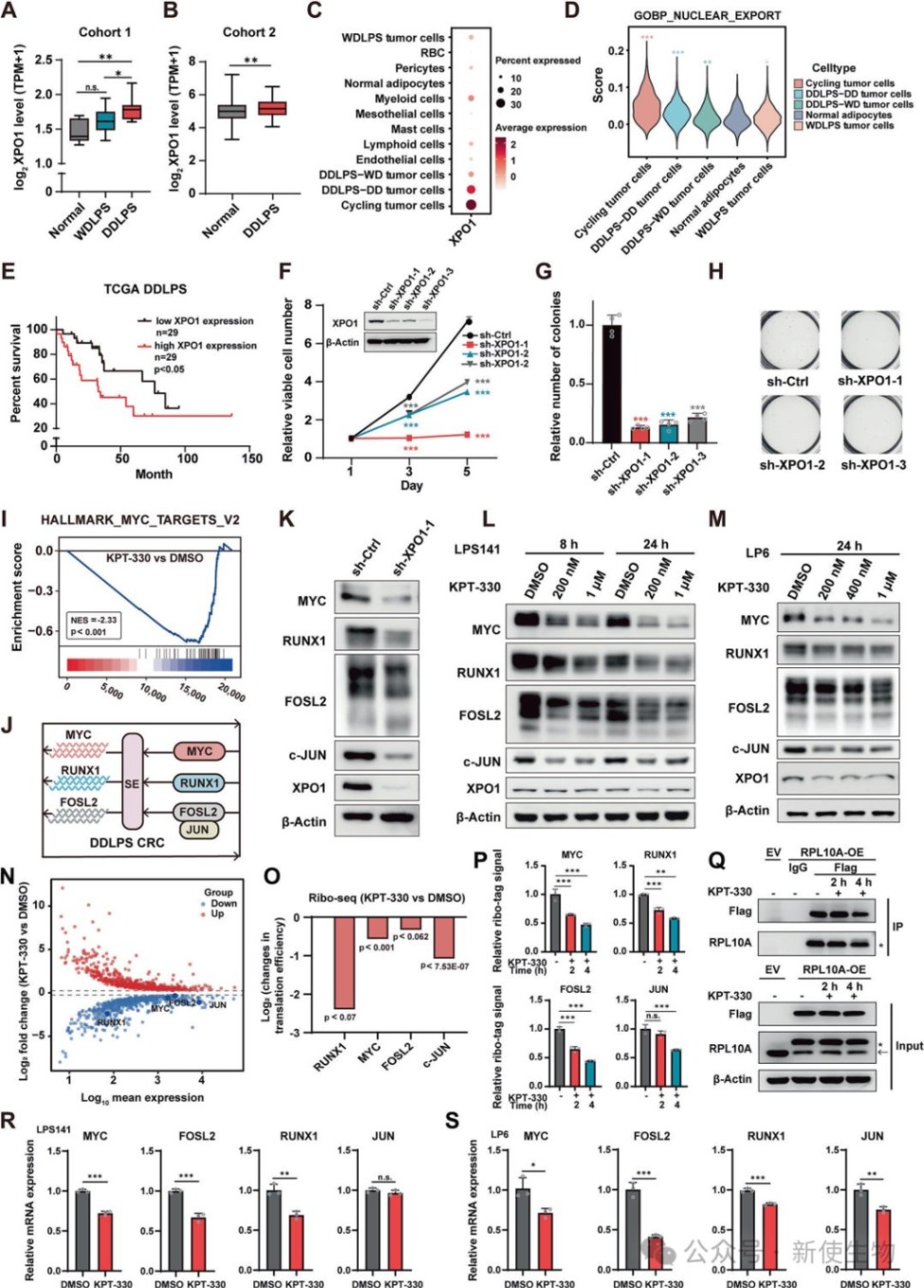
通过转录组学和细胞实验发现,XPO1在DDLPS组织中高表达且与不良预后相关。
使用KPT-330或通过基因敲低抑制XPO1功能,能够显著降低DDLPS细胞中MYC、RUNX1和FOSL2等CRC核心转录因子的蛋白水平,Ribo-seq核糖体印迹分析表明这主要是通过抑制其翻译效率实现的。
二、KPT-330通过阻断核糖体大亚基的核输出影响全局翻译
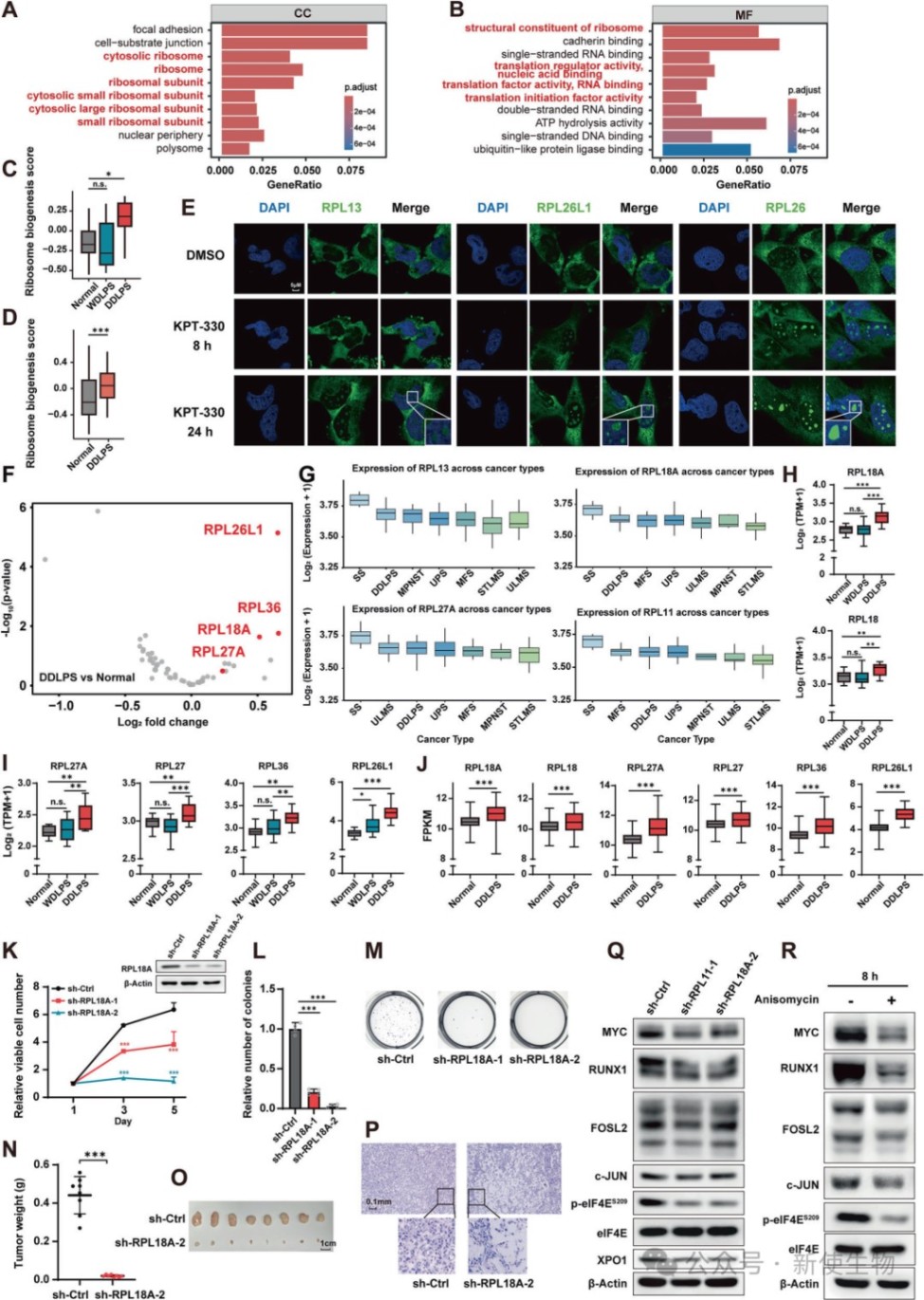
研究发现,DDLPS对核糖体生物合成高度依赖,且RPL11和RPL18A等大亚基蛋白对其恶性增殖至关重要。
长时间使用KPT-330处理后,免疫荧光实验显示核糖体大亚基蛋白被滞留在核仁,这表明药物通过阻碍核糖体成熟来抑制翻译延伸过程,从而影响全局蛋白合成。
三、KPT-330通过优先抑制MYC翻译来瓦解CRC稳态
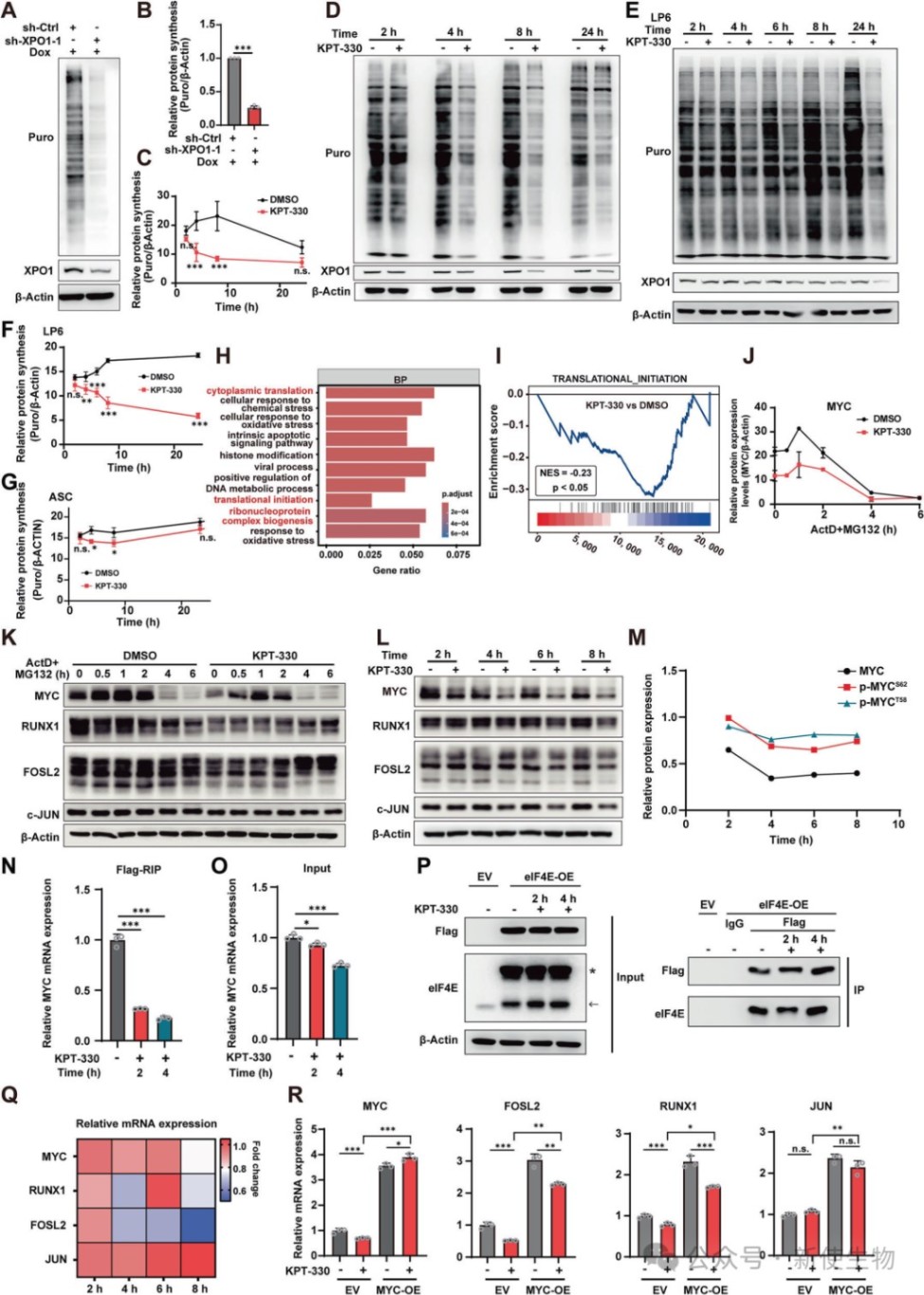
通过蛋白合成速率检测和Ribo-seq核糖体印迹分析发现,KPT-330在用药早期(2-4小时)就能迅速抑制DDLPS细胞的翻译过程。
其中,CRC核心因子MYC的翻译最先受到抑制,其蛋白水平的快速下降进一步导致了整个CRC转录网络的失稳。
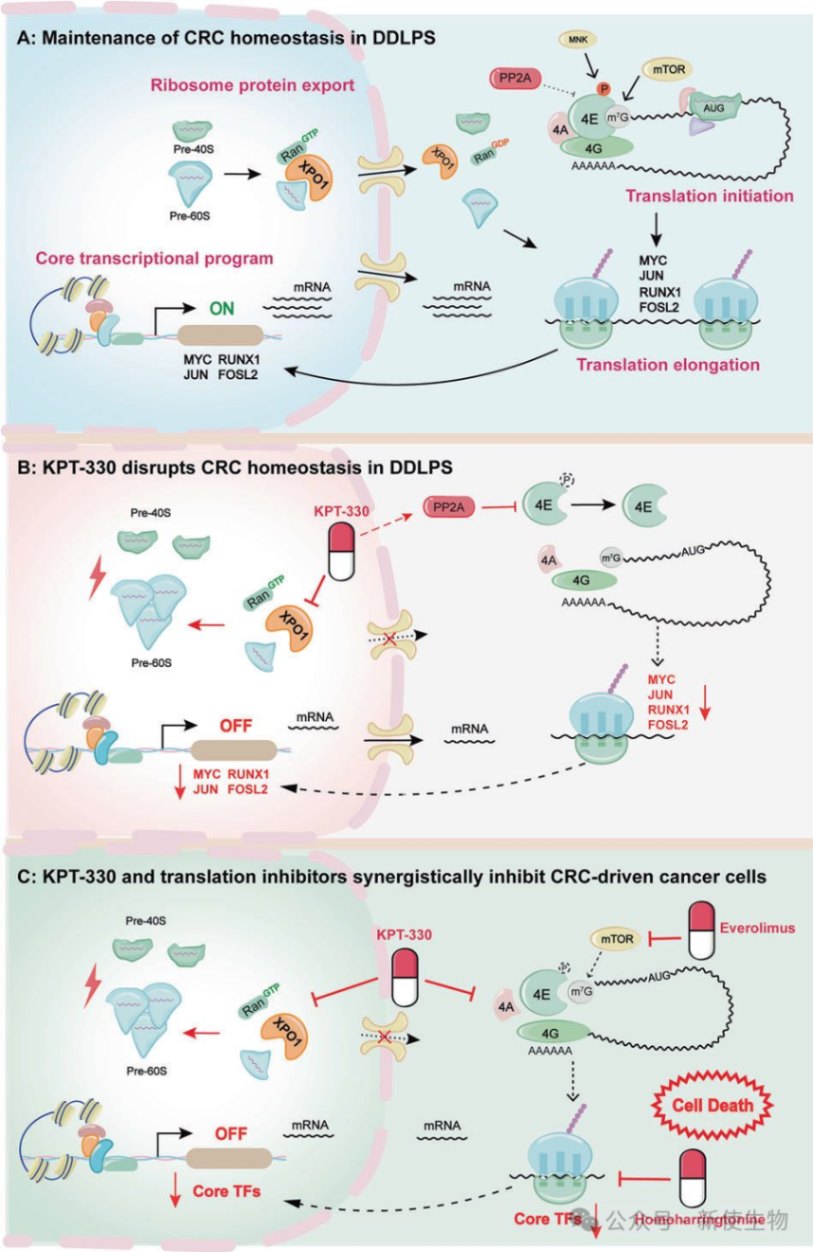
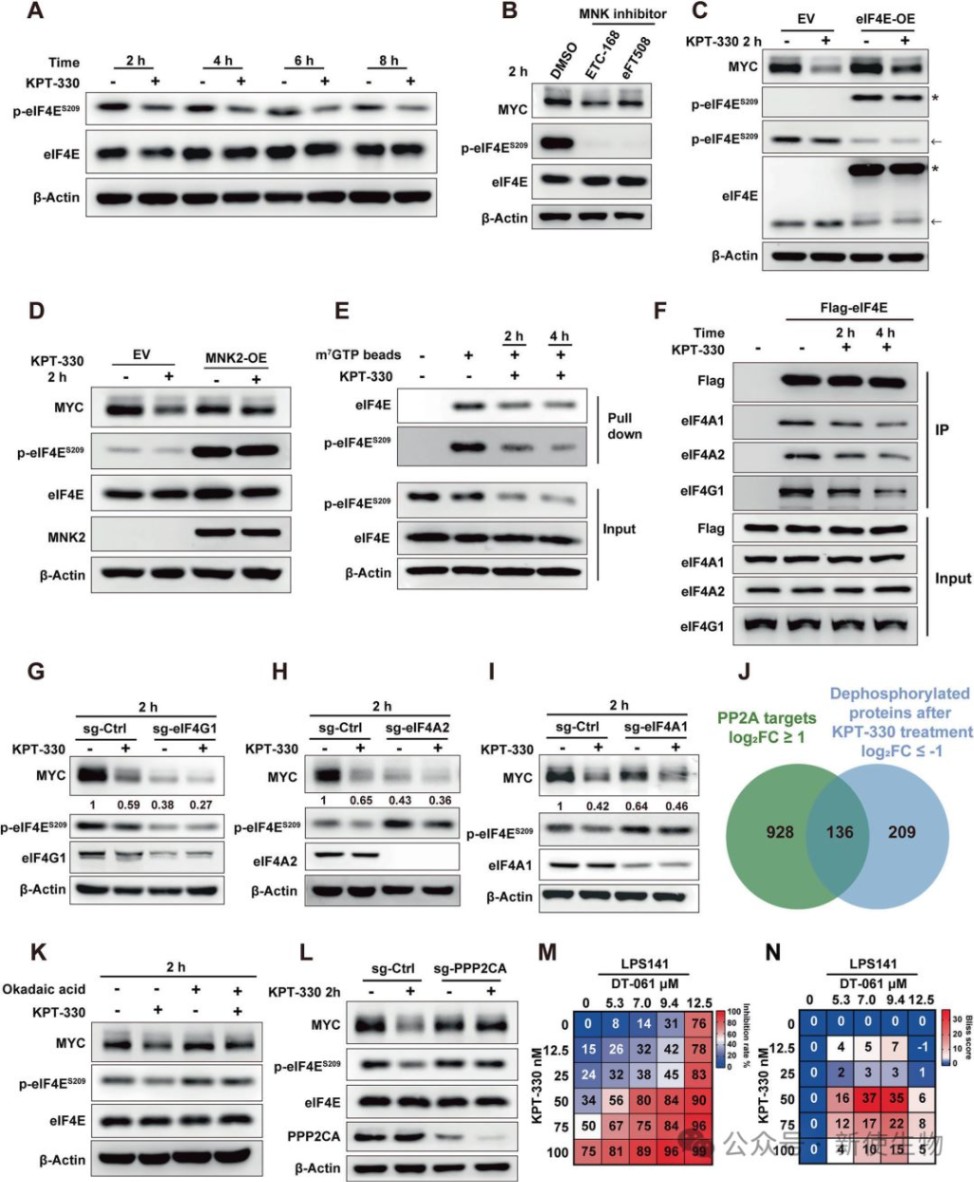
四、KPT-330通过激活PP2A和破坏eIF4F复合物来抑制MYC翻译起始
机制研究表明,KPT-330通过激活PP2A磷酸酶,导致eIF4E去磷酸化,削弱了其与mRNA 5'端帽子的结合能力。
同时,药物还破坏了eIF4E、eIF4G1和eIF4A等关键蛋白组成的翻译起始复合物(eIF4F)的组装,从而有效阻断了MYC的翻译起始。
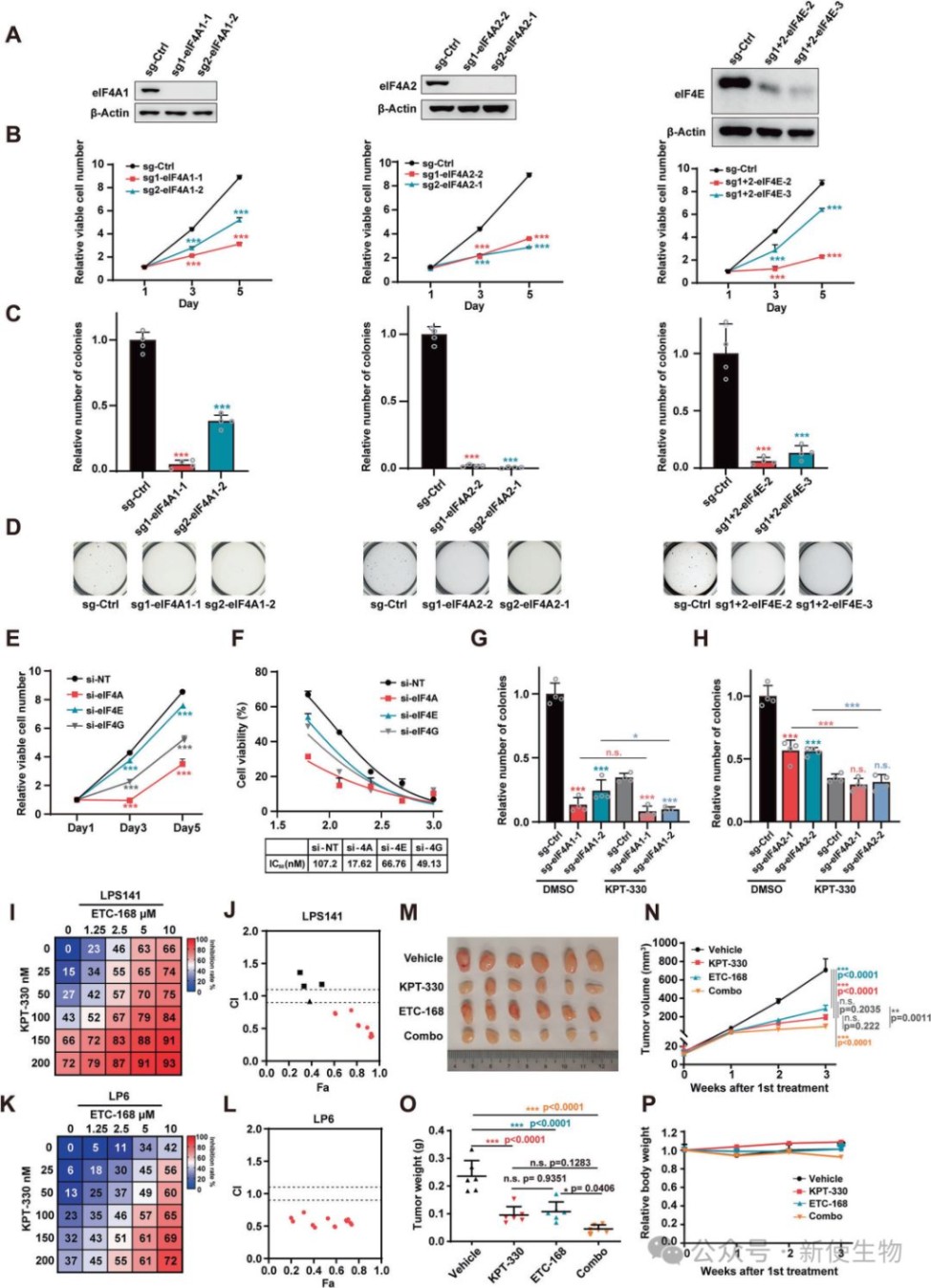
五、翻译起始通路是DDLPS的生存关键,抑制该通路可增强KPT-330疗效
通过基因编辑和RNA干扰技术敲低eIF4A1/2或eIF4E等翻译起始关键因子,能显著抑制DDLPS细胞的增殖和克隆形成能力。
此外,抑制翻译起始通路(如使用MNK抑制剂ETC-168)与KPT-330联用在体外和体内均表现出协同抗肿瘤效应。
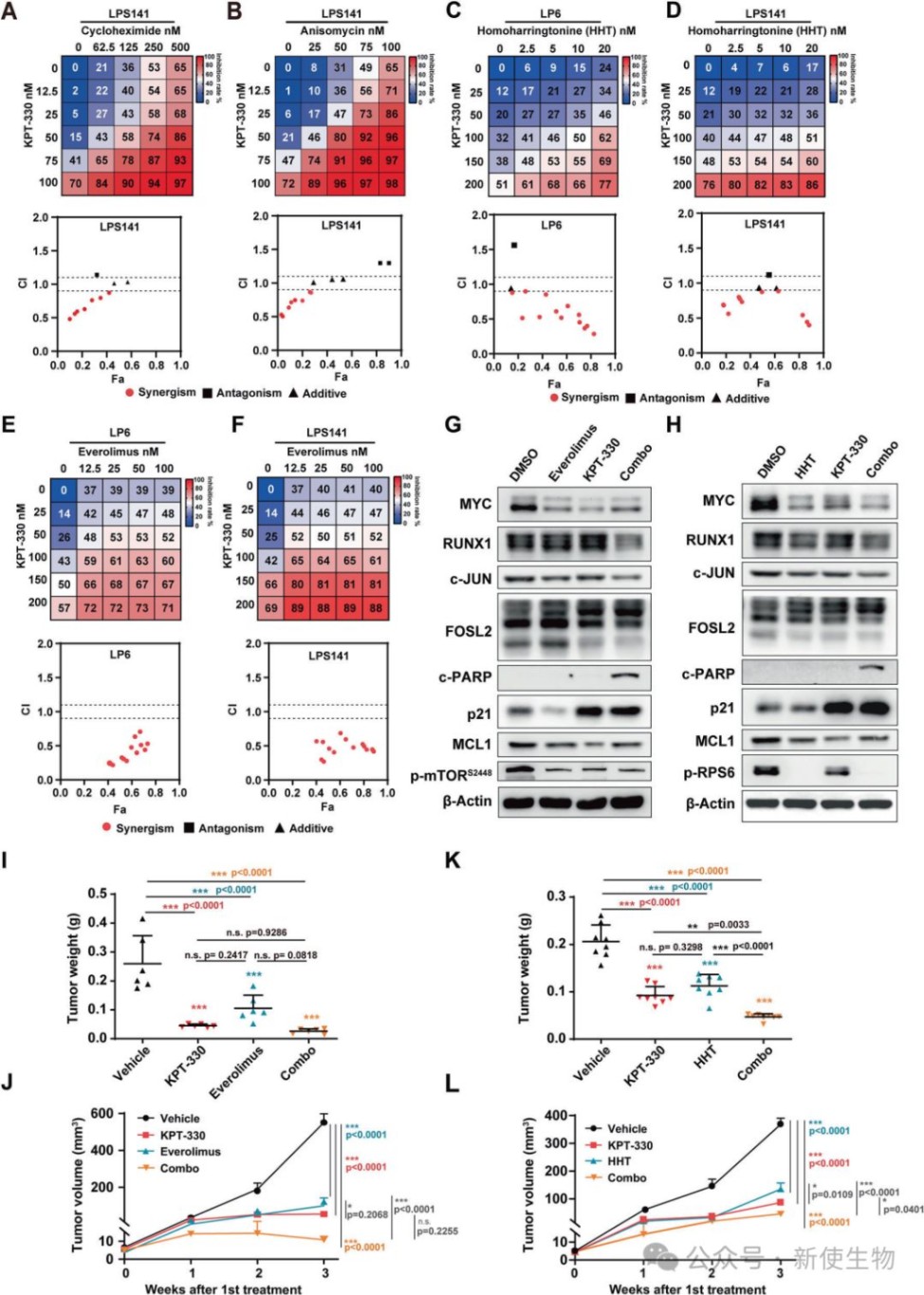
六、KPT-330与多种翻译抑制剂联用具有协同致死效应
药物联用实验证实,KPT-330与多种翻译抑制剂在DDLPS细胞和异种移植瘤模型中均展现出强大的协同抗癌活性。
联合用药能更有效地抑制CRC核心转录因子表达,并诱导更强的细胞凋亡。
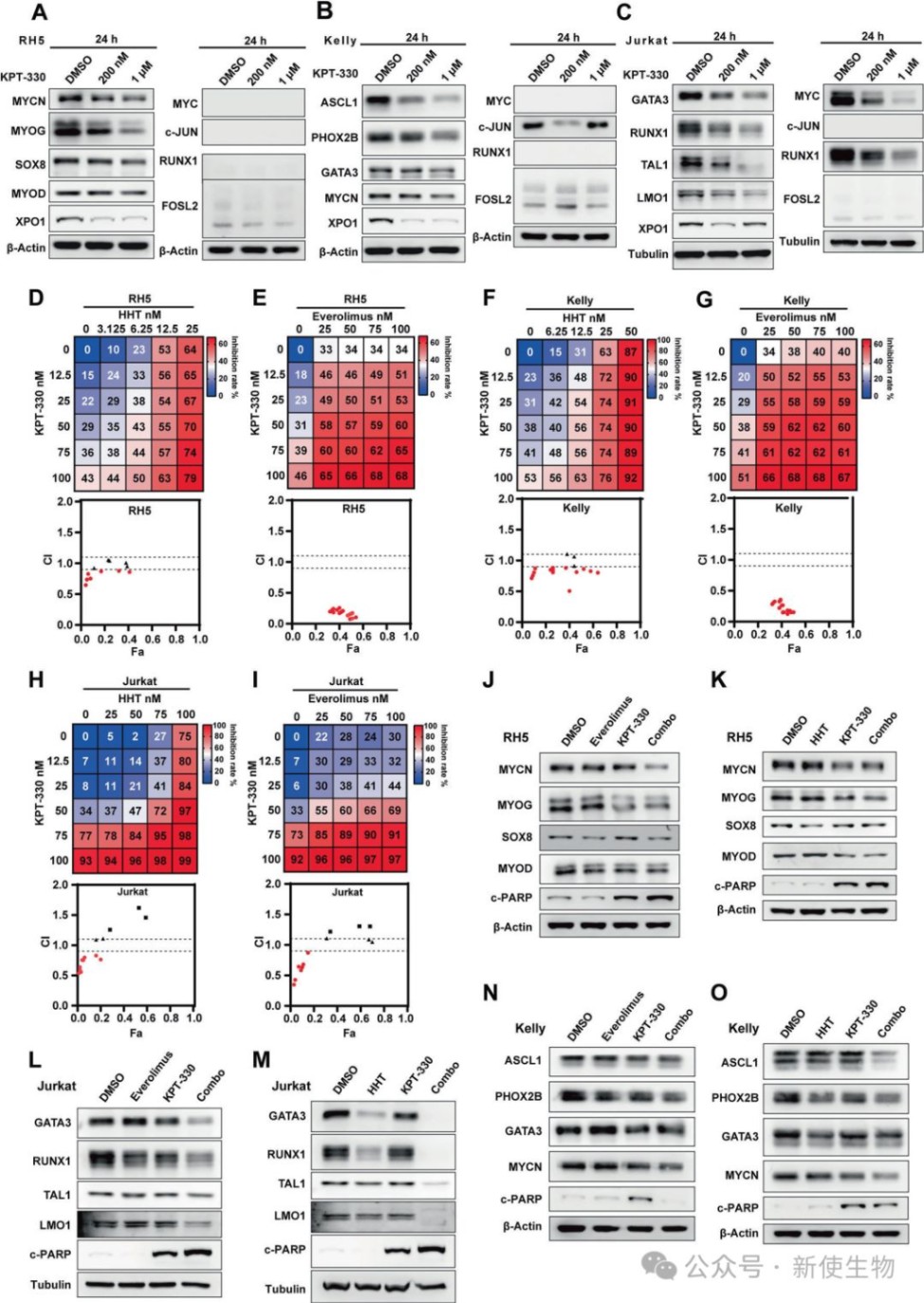
七、联合靶向XPO1和翻译是一种适用于多种CRC驱动癌症的广谱策略
研究将该策略扩展到其他CRC驱动的癌症模型,包括横纹肌肉瘤、T细胞白血病和神经母细胞瘤。
结果显示,KPT-330同样能有效破坏这些癌症的特异性CRC,并且与翻译抑制剂联用均表现出强大的协同杀伤效果,证明了该联合治疗策略的广泛适用性。
总结
本研究系统阐明了XPO1抑制剂KPT-330通过双相调控翻译过程来破坏DDLPS核心转录调控回路的全新作用机制。研究结果不仅为DDLPS的治疗提供了新的见解,还为开发基于XPO1抑制剂和翻译抑制剂的联合疗法,以治疗更广泛的CRC驱动型癌症,提供了强有力的临床前证据。


 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们
