
导读
核糖核酸酶(RNase)通过介导RNA加工和降解来塑造基因表达。这些酶在维持细胞稳态和促进不同环境条件下的动态适应中发挥着不可或缺的作用。
随着对各种RNase底物谱认识的不断深入,它们在协调不同基因表达环节中的交互作用逐渐被认可。部分多功能RNase能够针对多种RNA底物进行切割,从而在细胞面临应激时促进多维度的基因表达重编程。
血管生成素(ANG)作为RNaseA家族中最具代表性的成员,不仅是诱导新血管生成的关键因子,还参与神经保护与细胞增殖等生物学过程。ANG在不同细胞状态下展现出针对多种RNA底物的选择性活性,这使其成为研究多功能核糖核酸酶的理想原型。
2026年4月22日,德国哥廷根大学医学中心的Katherine E. Bohnsack和Markus T. Bohnsack团队在Trends in Biochemical Sciences上发表了题为“The multifunctional, stress-sensitive ribonuclease angiogenin cross-regulates different gene expression processes”的综述文章。该文系统阐明了血管生成素(ANG)作为一种应激敏感的多功能核糖核酸酶,通过在不同细胞区室中靶向特定RNA底物,协调转录、tRNA片段化及翻译过程的跨层面调控机制。

综述整理
一、ANG的双重角色:生理稳态的建设者与应激响应的调控者
ANG是一种分泌性蛋白,可在细胞内外发挥功能。其在细胞内的定位和功能表现出显著的上下游依赖性,在生理和应激条件下扮演着截然不同的角色。
生理条件下: 细胞内大部分ANG被转运至细胞核,并富集在核仁。在这里,它作为基因表达的促进者,通过刺激rRNA的合成来驱动核糖体的生物发生,从而支持细胞的生长和增殖。细胞质中残留的少量ANG则被其高效抑制剂RNH1所束缚,保持无活性状态。
应激条件下(如氧化应激、缺氧): ANG与RNH1的亚细胞定位发生逆转,ANG从核仁大量转移至细胞质,而RNH1则进入核仁。这一重定位赋予了ANG全新的功能:在细胞质中,游离的ANG被激活,特异性地切割tRNA,产生具有调控功能的tsRNAs,从而重塑细胞的翻译程序,帮助细胞适应压力。
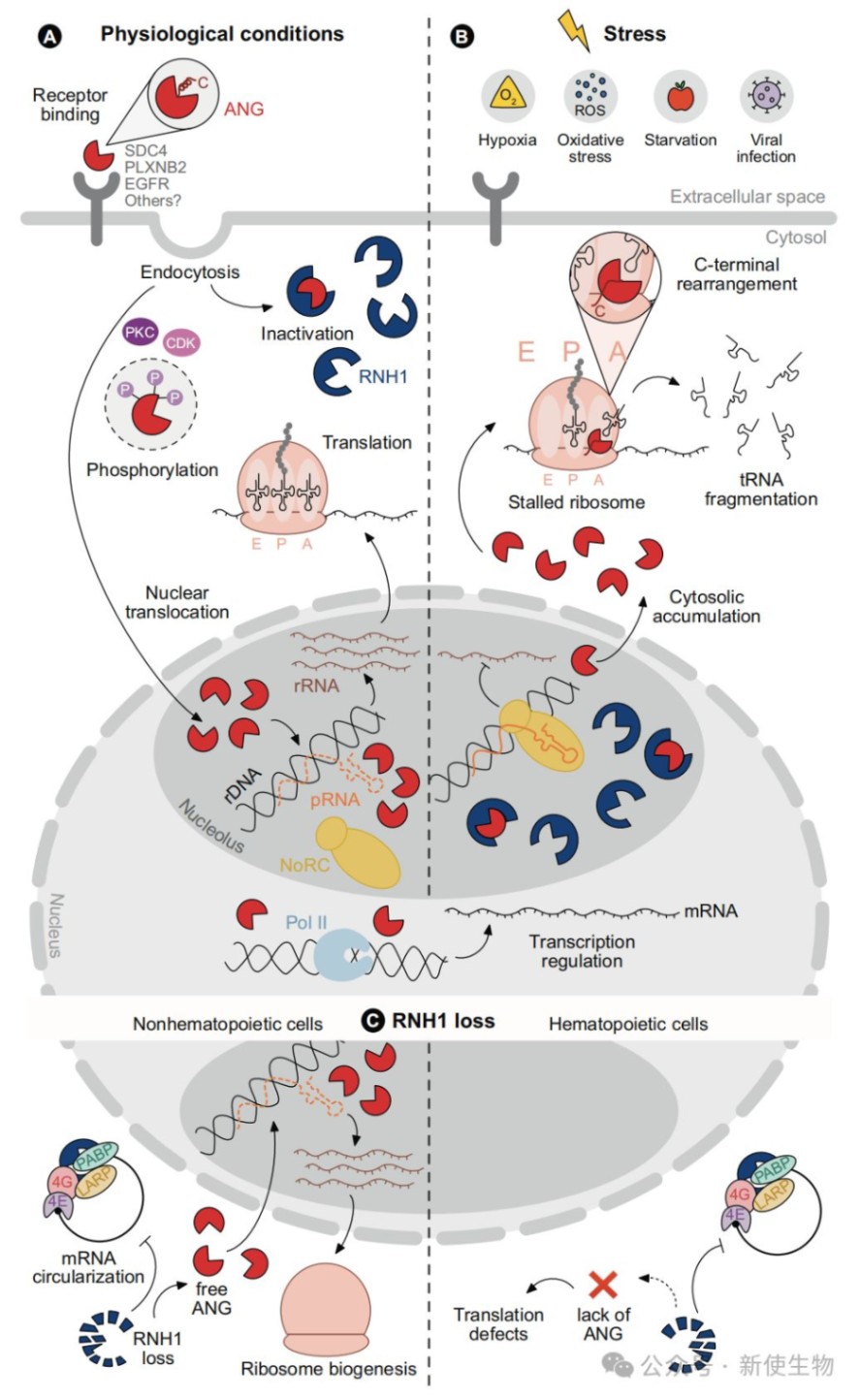
二、ANG对转录的调控:以核糖体生物发生为核心
2.1) 刺激rDNA转录的核心机制
ANG在核仁中的主要功能是促进由RNA聚合酶I(Pol I)介导的rDNA转录,其机制是:ANG通过其核酸酶活性,切割一种在rDNA启动子区域形成的、起抑制作用的启动子相关RNA(pRNA)。
pRNA被切除后,染色质重塑复合物NoRC便无法结合到rDNA启动子上。这导致局部染色质变得更加开放,从而极大地促进了rRNA的合成。
2.2) 调控蛋白编码基因转录的潜在作用
除了调控rDNA,ANG也存在于核质中,并可能参与调控由RNA聚合酶II(Pol II)介导的蛋白编码基因的转录。
研究发现,ANG能够结合某些基因启动子上的富含嘧啶的序列(ABE元件),或通过表观遗传机制来调控特定基因的表达,但这方面的机制尚不完全清楚。
三、ANG在应激下的核心功能:tRNA的切割与tsRNA的生成
在细胞质中,ANG介导的tRNA切割是其响应应激的核心功能。
3.1) 核糖体:ANG的“激活平台”与“定位向导”
长期以来,胞质中ANG如何被激活一直是个谜。最新研究揭示,停滞的核糖体是ANG的激活器。
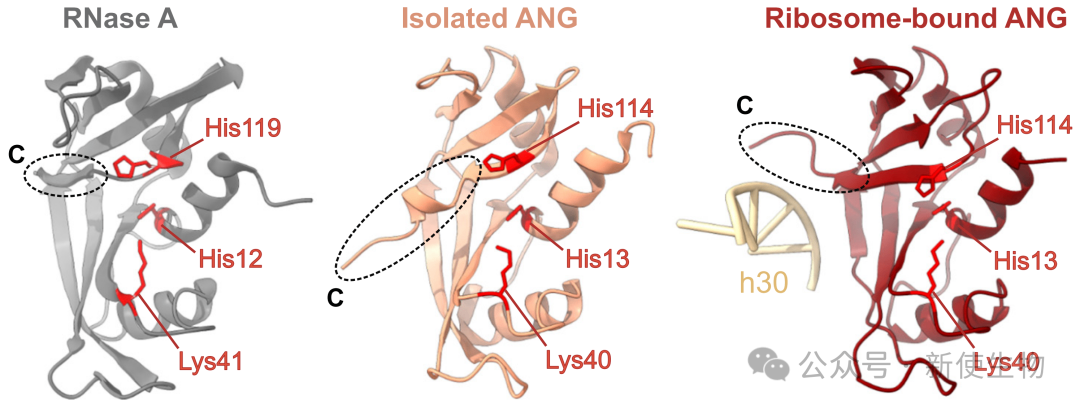
激活机制: 当ANG结合到A位点为空的延伸核糖体上时,核糖体的结构会诱导ANG的C端发生构象变化,从而完全暴露其被自身结构所遮蔽的催化活性位点。
特异性导向: 核糖体不仅激活ANG,还将其精确定位到新进入的tRNA的反密码子环(ACL)附近,引导其进行切割。
3.2) tsRNA的生成与功能多样性
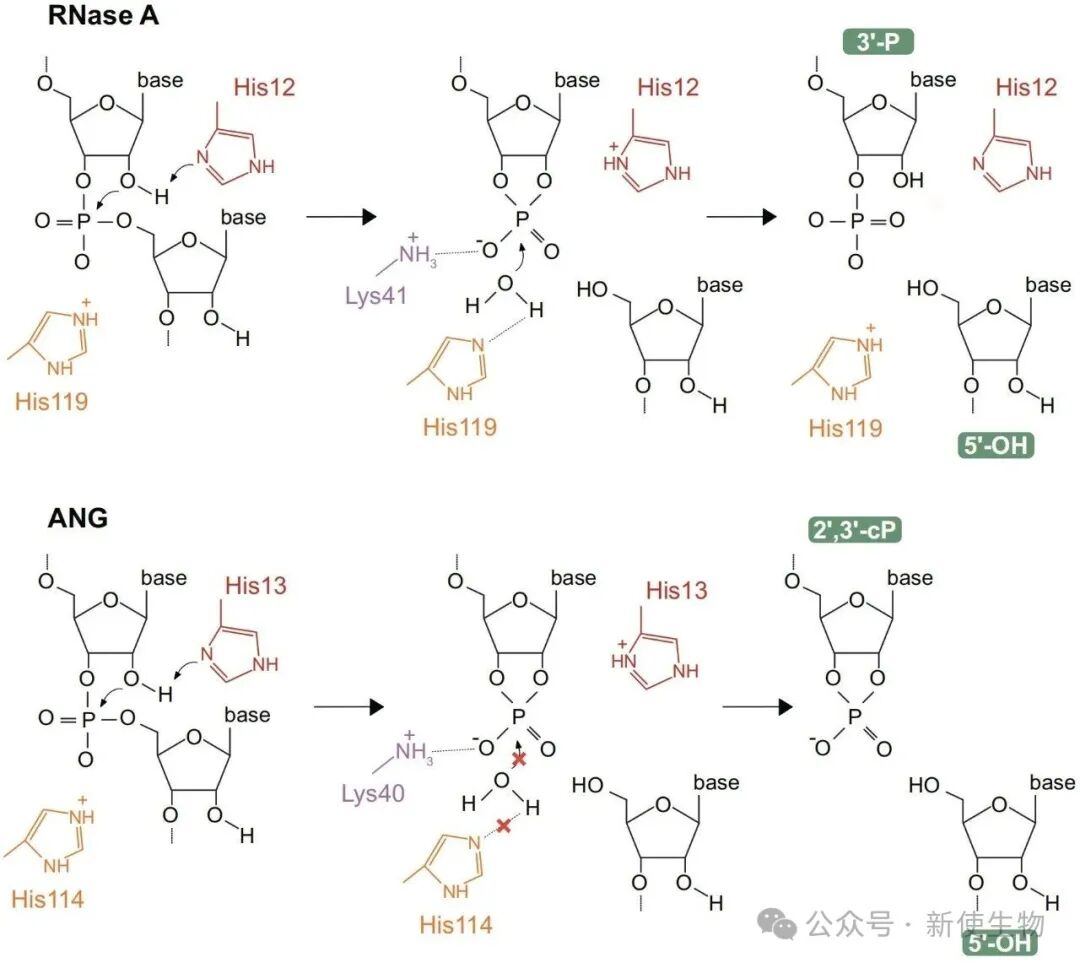
ANG在tRNA反密码子环处进行切割,产生5'-tsRNA和3'-tsRNA。这些tsRNA并非无意义的降解产物,而是重要的信号分子。
抑制翻译起始: 某些5'-tsRNA通过形成G-四链体结构,能够置换mRNA 5'帽子上的翻译起始复合物(eIF4F),从而抑制全局蛋白质合成。
促进应激颗粒(SGs)形成: tsRNA被报道能促进翻译停滞的复合物组装成应激颗粒,进一步调控应激下的翻译程序。
抑制细胞凋亡: 在渗透压胁迫下,ANG产生的tsRNA能够结合并抑制细胞色素c,从而阻止凋亡体的形成。
调控基因转录: 在斑马鱼中发现,一种tsRNA能够以反馈方式促进其亲本tRNA基因的转录。
四、ANG对翻译的直接调控
除了通过生成tsRNA间接调控翻译,ANG还能直接影响翻译过程。
切割rRNA: 早年研究发现,ANG可以直接切割18S rRNA,导致全局翻译抑制。
竞争性抑制: ANG结合在核糖体的A位点(解码中心),直接与进入的氨酰-tRNA竞争,从而阻碍翻译的解码步骤。
与RNH1协同调控: RNH1的缺失会影响mRNA环化(一种促进翻译的结构),导致翻译缺陷。在非造血细胞中,这种缺陷可以被代偿性上调的ANG(通过促进核糖体生成)所弥补,而在ANG低表达的造血细胞中,RNH1缺失则会导致严重的翻译抑制。
五、ANG活性的精密调控机制
作为一个功能强大的RNase,ANG的活性受到多层次的严密调控,以防其在不当的时间和地点造成破坏。
RNH1的强效抑制: RNH1是ANG的天然抑制剂,二者间的结合亲和力是已知蛋白质相互作用中最高的之一。在生理条件下,RNH1将胞质中的ANG牢牢锁定在无活性状态。
磷酸化修饰: ANG的磷酸化是其功能转换的关键开关。PKC和CDK等激酶对ANG的磷酸化,一方面能显著降低其与RNH1的结合力,另一方面是其进入细胞核的必要条件。
自身结构抑制: ANG的C末端会折叠回来,遮挡其催化活性中心,使其基础活性维持在很低的水平。只有在结合核糖体等激活因子后,这种自身抑制才被解除。
亚细胞区室化: 通过在细胞核、细胞质和细胞外空间之间的动态穿梭,ANG在不同区室执行不同的功能,构成了空间上的调控。
总结
本文全面总结了血管生成素(ANG)在基因表达调控中的多维角色,强调了其通过改变亚细胞定位和底物选择性来响应细胞应激的能力。ANG不仅是蛋白质合成的促进者,也是应激下翻译重构的指挥官,为开发针对血管生成相关疾病及神经退行性疾病的疗法提供了重要的理论基础。
| 新使生物专业翻译组一站式服务平台 |
| 产品名称 |
点击图片查看
点击图片查看


 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们
