
导读
作为专性细胞内寄生生物,病毒完全依赖宿主的mRNA翻译机制来合成其蛋白质。病毒mRNA的翻译会大量消耗宿主资源并施加结构限制,从而引发翻译应激。
翻译应激会激活细胞的监视反应,包括核糖体相关质量控制(RQC)、整合应激反应(ISR)、核糖体毒性应激反应(RSR)和先天性免疫反应(IIR)。其中,RQC系统通过降解异常翻译产物和mRNA来保障翻译的保真度。
因此,RQC被认为是宿主抵抗病毒感染的一道重要防线。然而,病毒也进化出了复杂的策略来劫持或抑制RQC,以优化自身蛋白质的生产并逃避宿主免疫监视,这构成了宿主与病毒之间一场持续的分子军备竞赛。
近日,瑞典卡罗林斯卡学院的Maria G. Masucci在Trends in Microbiology上发表了题为“Viruses and RQC: a molecular arms race at the heart of translation”的综述文章。该文系统阐述了病毒感染与宿主RQC之间复杂的相互作用,强调了RQC的抗病毒特性,并深入讨论了病毒如何通过重编程RQC来促进自身复制和免疫逃逸,为开发靶向翻译控制机制的新型抗病毒策略提供了新的视角。

综述整理
一、翻译应激与细胞的监视网络
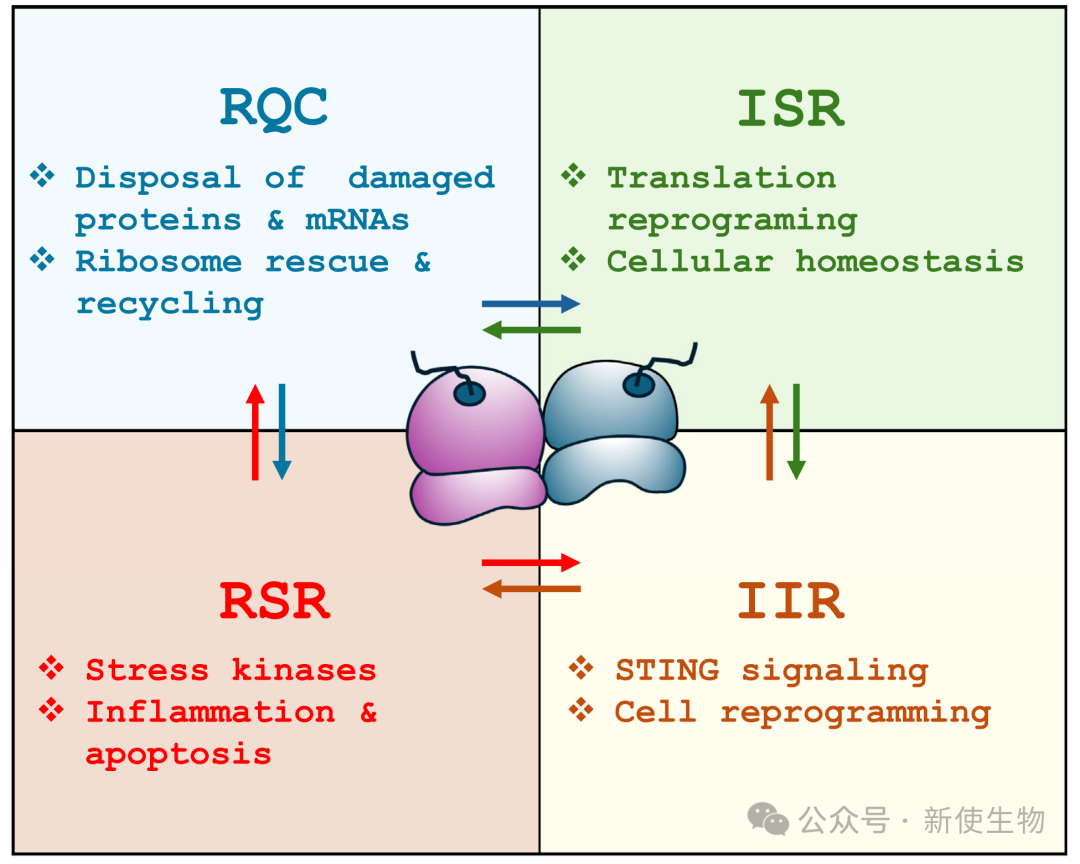
病毒mRNA的快速翻译以及其固有的翻译障碍(如稀有密码子、稳定二级结构)会导致核糖体暂停、停滞甚至碰撞(collision)。这种“交通堵塞”会激活细胞内一套相互关联的监视与应激反应系统:
核糖体相关质量控制 (RQC): 核心监视通路,负责拯救停滞的核糖体、降解异常的新生肽链和缺陷mRNA,维持翻译的效率和保真度。
整合应激反应 (ISR): 通过全局性抑制蛋白质合成来减轻翻译负荷,同时选择性翻译有助于细胞恢复稳态的蛋白。
核糖体毒性应激反应 (RSR): 在核糖体受到不可逆损伤时被激活,通过诱导炎症和细胞凋亡来清除受损细胞。
先天性免疫应答 (IIR): 感知到翻译异常后,通过cGAS-STING等通路诱导I型干扰素(IFN)的产生,建立抗病毒状态。
二、RQC通路的分子机制
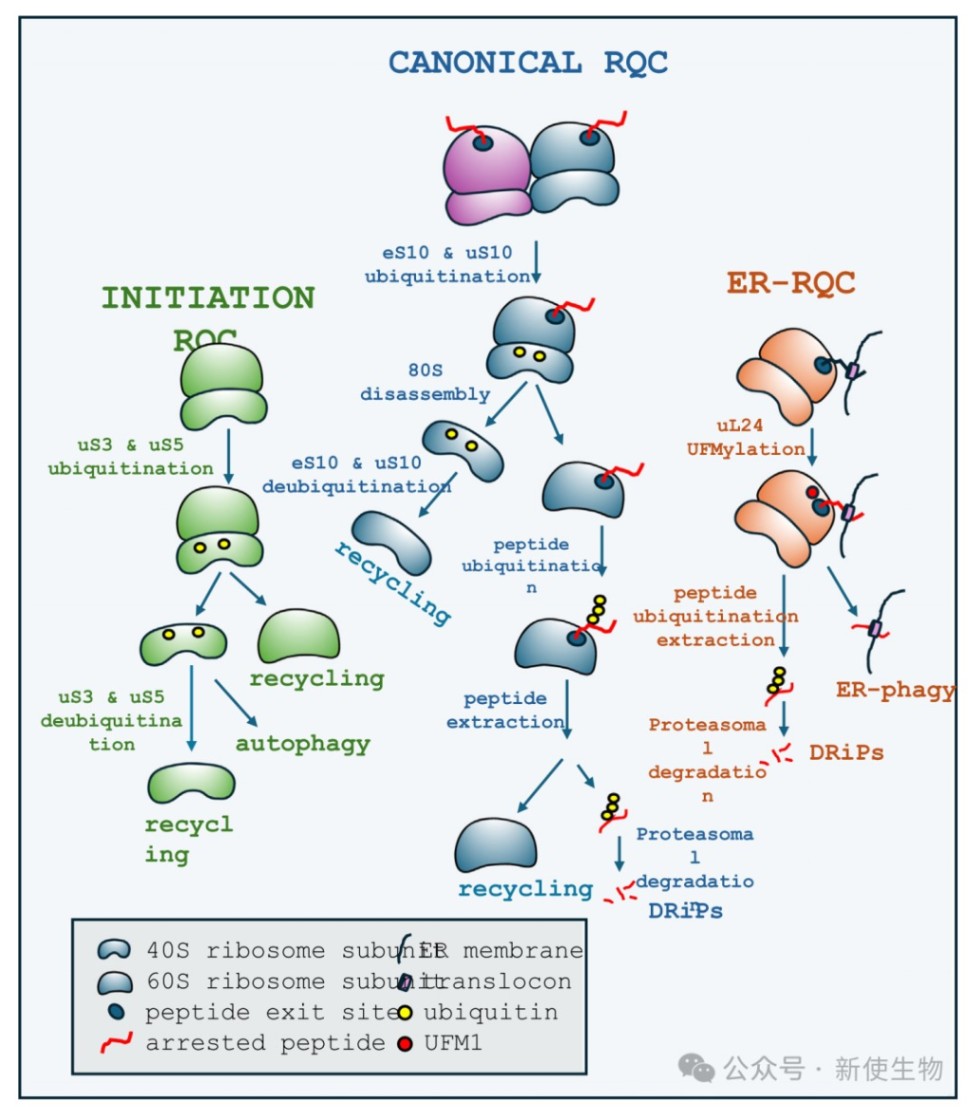
RQC是一个多分支、多层次的质量控制系统,针对翻译过程中不同阶段的停滞事件进行响应。
2.1) 经典RQC:应对翻译延伸停滞
当核糖体在翻译延伸过程中发生碰撞时,经典RQC被激活:
1. 碰撞感知: ZNF598(一种泛素连接酶)识别碰撞的核糖体,并特异性地泛素化前导核糖体小亚基(40S)上的eS10和uS10蛋白。
2. 亚基解离: ASCC复合物被招募到泛素化的40S亚基上,利用ATP水解的能量将停滞的前导核糖体分裂成40S和60S-肽酰-tRNA复合物。40S亚基随后被去泛素化并回收。
3. 新生肽链的处理:
CAT-尾化 (CAT-tailing):NEMF在新生肽链的C端添加一段由丙氨酸和苏氨酸组成的“尾巴”。
泛素化: 这条“尾巴”将肽链从核糖体出口通道中推出,暴露其内部的赖氨酸残基,随后被LTN1(另一种泛素连接酶)泛素化。
降解: 最终,泛素化的新生肽链被VCP/p97复合物从60S亚基上拔出,并递送至蛋白酶体降解。
2.2) 起始RQC (iRQC):应对翻译起始失败
当核糖体在起始密码子处停滞时,iRQC被激活。泛素连接酶RNF10会泛素化40S亚基上的uS3和uS5蛋白,标记该异常的40S亚基进行自噬降解或回收。
2.3) 内质网RQC (ER-RQC):应对分泌蛋白翻译停滞
当翻译分泌蛋白或膜蛋白的核糖体在内质网易位子通道处停滞时,ER-RQC被激活。
其关键特征是60S亚基上的uL24蛋白被一种叫做UFM1的类泛素分子修饰(UFMylation),该过程由UFL1连接酶复合物催化。
这会将停滞的核糖体与内质网相关降解(ERAD)或内质网自噬(ER-phagy)联系起来。
三、病毒对RQC的干扰与重编程
病毒进化出了多种策略来操控RQC,以服务于自身复制周期。
3.1) 痘病毒:对RQC的双向“重塑”
痘病毒(如牛痘病毒VacV)表现出一种精巧的时间调控策略:
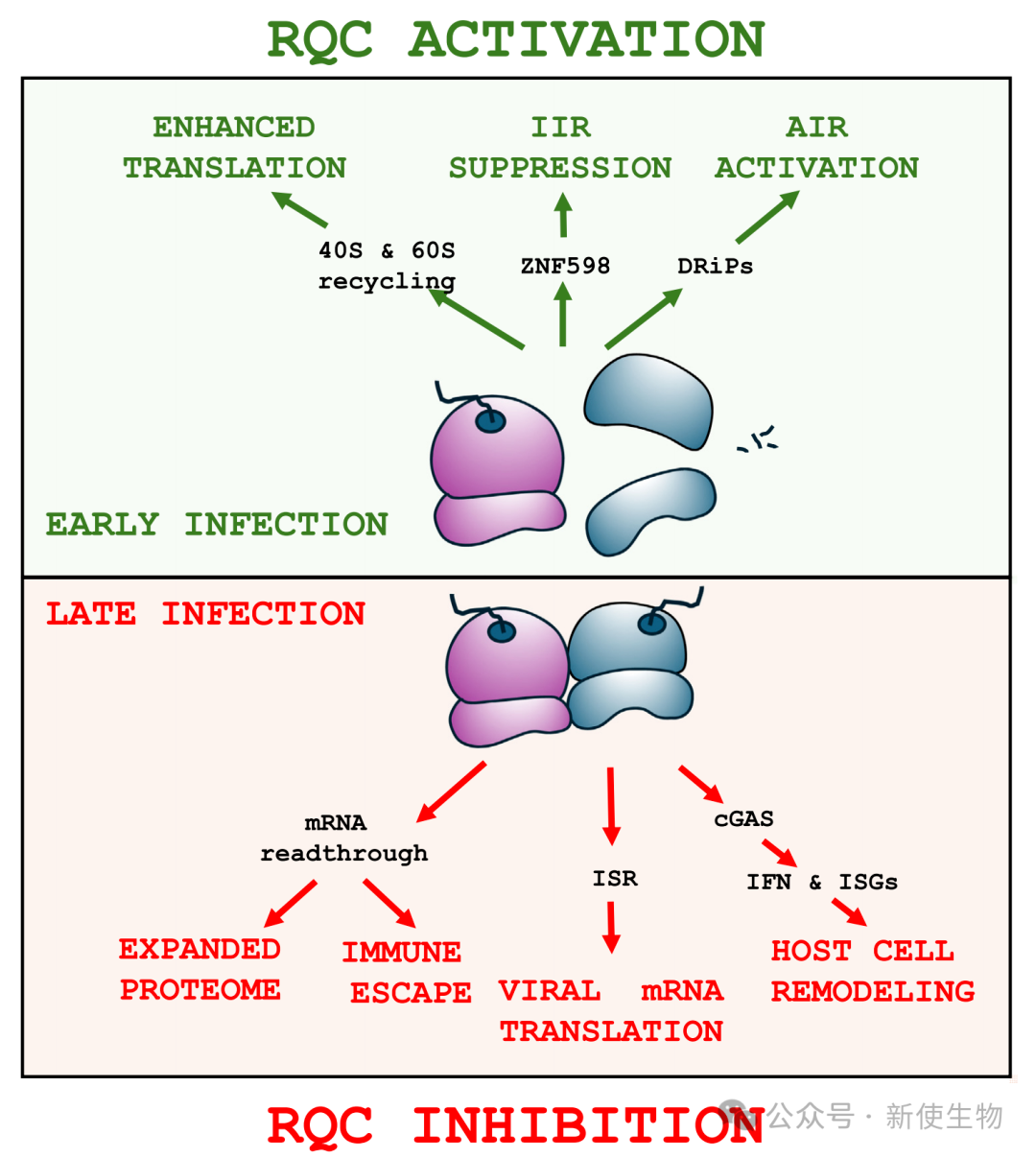
感染早期: 激活RQC。病毒似乎利用RQC的核糖体回收功能,以维持一个健康的核糖体池,高效合成早期病毒蛋白。
感染晚期: 抑制RQC。病毒晚期mRNA含有能诱导停滞的5'多聚腺苷酸(poly(A))前导序列。通过抑制RQC,病毒能够促进这些异常mRNA的通读翻译。其机制是病毒激酶B1R磷酸化RQC关键蛋白RACK1,从而重塑RQC的功能。
3.2) 疱疹病毒:利用vDUB直接关闭RQC
疱疹病毒(如EBV、HSV-1)编码一类保守的病毒去结合酶(vDUBs),如EBV的BPLF1。
1. 直接抑制: vDUB能够结合在翻译中的核糖体上,并直接移除由ZNF598、RNF10和UFL1等宿主连接酶添加在核糖体蛋白上的泛素和UFM1修饰,从而全面关闭经典RQC、iRQC和ER-RQC。
2. 一石二鸟:
促进病毒蛋白合成: RQC被抑制后,病毒能够翻译那些含有翻译障碍(如G-四链体结构)的mRNA(如EBNA1),扩大其蛋白质组。
劫持ISR: RQC的抑制导致碰撞核糖体累积,从而激活ISR。病毒进而利用ISR来抑制宿主蛋白合成,同时通过IRES或uORF等机制选择性翻译自身的mRNA。
3.3) RNA病毒:潜在的干扰策略
尽管研究尚少,但证据表明RNA病毒也可能干扰RQC。
例如,SARS-CoV-2的Nsp1蛋白能结合核糖体,似乎有助于解决核糖体停滞,这可能在最大化病毒翻译效率的同时,抑制了由碰撞核糖体激活的cGAS先天免疫信号。
四、RQC与抗病毒免疫的“双刃剑”效应
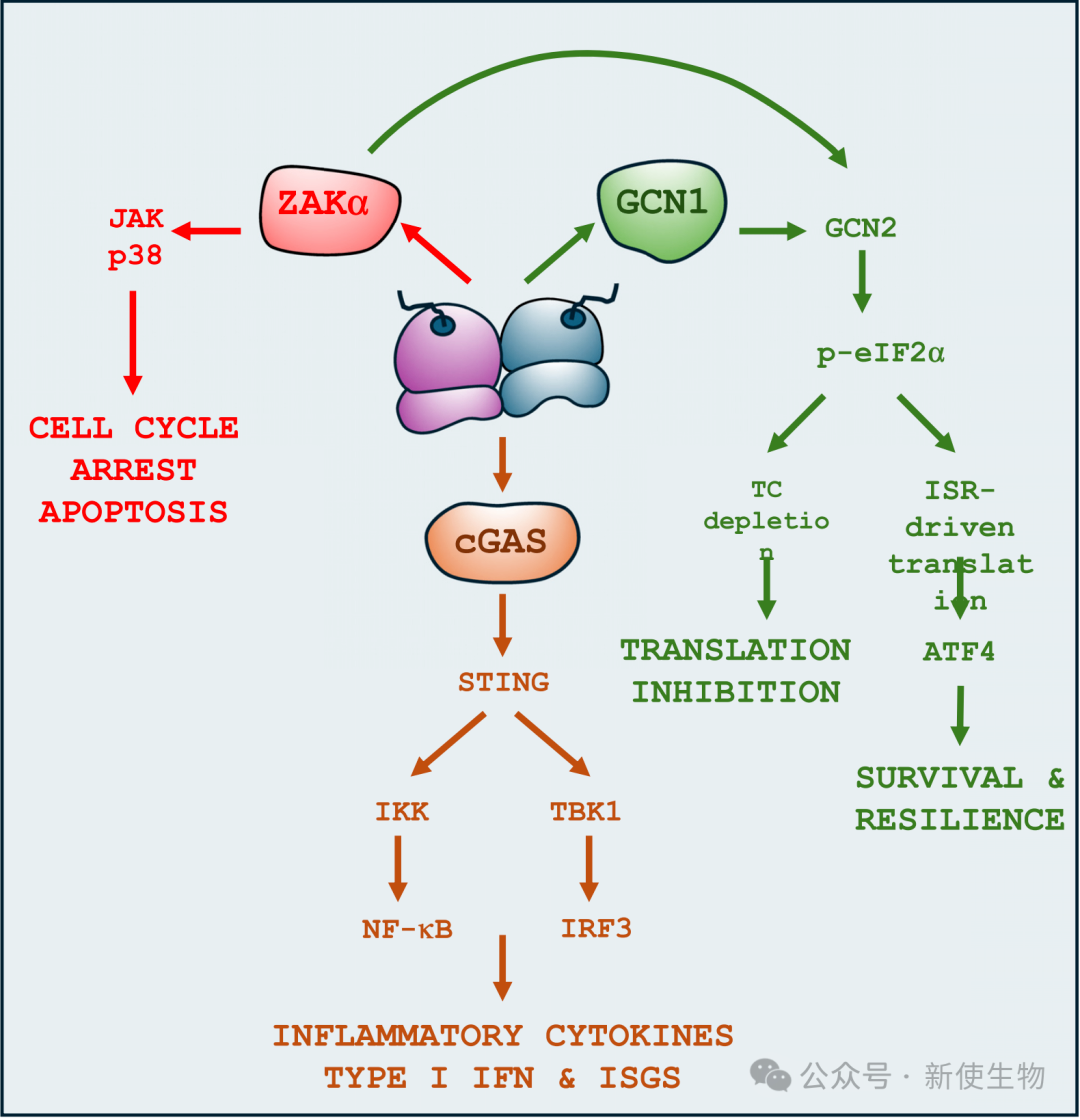
RQC不仅是翻译保真度的守护者,也是连接翻译应激与免疫系统的关键枢纽。
4.1) RQC与先天免疫:触发抗病毒警报
当RQC失活或不堪重负时,累积的碰撞核糖体可以直接作为模式识别受体cGAS的共激活因子。
这会启动cGAS-STING信号通路,导致I型干扰素的大量产生,从而建立一个广谱的抗病毒状态。
因此,RQC的正常运作对抑制过度的先天免疫激活至关重要。
4.2) RQC与适应性免疫:病毒抗原的主要来源
DRiPs的产生: RQC通路降解的异常新生多肽被称为缺陷核糖体产物(Defective Ribosomal Products, DRiPs)。
抗原呈递: DRiPs是MHC I类分子呈递的病毒抗原肽的主要来源。这些肽段能够被细胞毒性T淋巴细胞(CTLs)识别,从而清除被感染的细胞。
病毒的免疫逃逸策略: 病毒在感染晚期通过抑制RQC,可以有效减少DRiPs的产生,从而降低自身抗原的呈递,使被感染的细胞能够“隐身”,逃避CTL的杀伤,为病毒的最终成熟和释放争取时间。
总结
本文系统阐述了RQC作为细胞翻译质量监控核心,在病毒-宿主相互作用中扮演的关键角色。病毒并非被动应对,而是进化出了在感染不同阶段或激活或抑制RQC的精妙策略,以优化病毒蛋白生产并逃逸宿主免疫监视。深入理解这一分子军备竞赛的机制,为开发靶向翻译调控的新型广谱抗病毒疗法开辟了新的道路。
| 新使生物专业翻译组一站式服务平台 |
| 产品名称 |
点击图片查看
点击图片查看


 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们
