
导读
目前基因沉默技术已相对成熟,但选择性地激活细胞内特定mRNA的翻译仍然缺乏有效的工具。如何引导核糖体到特定的起始密码子而不改变mRNA的原始序列是项巨大的挑战。
真核生物的翻译起始是一个高度精细的过程,通常遵循5'端帽依赖的扫描模型。核糖体在mRNA上扫描并选择合适的起始密码子,但许多mRNA含有多个起始位点,它们会抑制下游主起始密码子的使用。
尽管已有一些方法尝试激活翻译,如利用CRISPR系统或内部核糖体进入位点(IRES),但它们都存在局限性,特别是在调控内源基因的选择性翻译起始方面。因此,迫切需要开发一种能够精确、可编程地引导核糖体到特定起始密码子的新工具。
2025年11月21日,康奈尔大学钱书兵团队在Nature Biotechnology发表了题为“Programmable initiation of mRNA translation by trans-RNA”的研究论文。研究设计了一种名为trans-RNA的可编程RNA工具,它通过自身携带的5’端帽结构和与靶标mRNA的碱基配对,能够引导核糖体到特定的起始密码子,从而激活或调控单个mRNA的翻译。

文章索引
【标题】Programmable initiation of mRNA translation by trans-RNA
【发表期刊】Nature Biotechnology
【发表日期】2025年11月21日
【作者及团队】康奈尔大学钱书兵和波尔多大学Yaser Hashem团队
【IF】41.7
研究结果
一、设计trans-RNA以实现对起始密码子选择的控制
研究人员设计了一系列带有5'端帽结构的短链RNA(trans-RNA),它们能与目标mRNA上的特定区域(如uORF和主ORF之间)形成双链结构。
通过调控trans-RNA 5'端非配对区域的长度,可以精确控制双链结构在核糖体上的位置,从而有效激活被uORF抑制的下游基因的翻译。
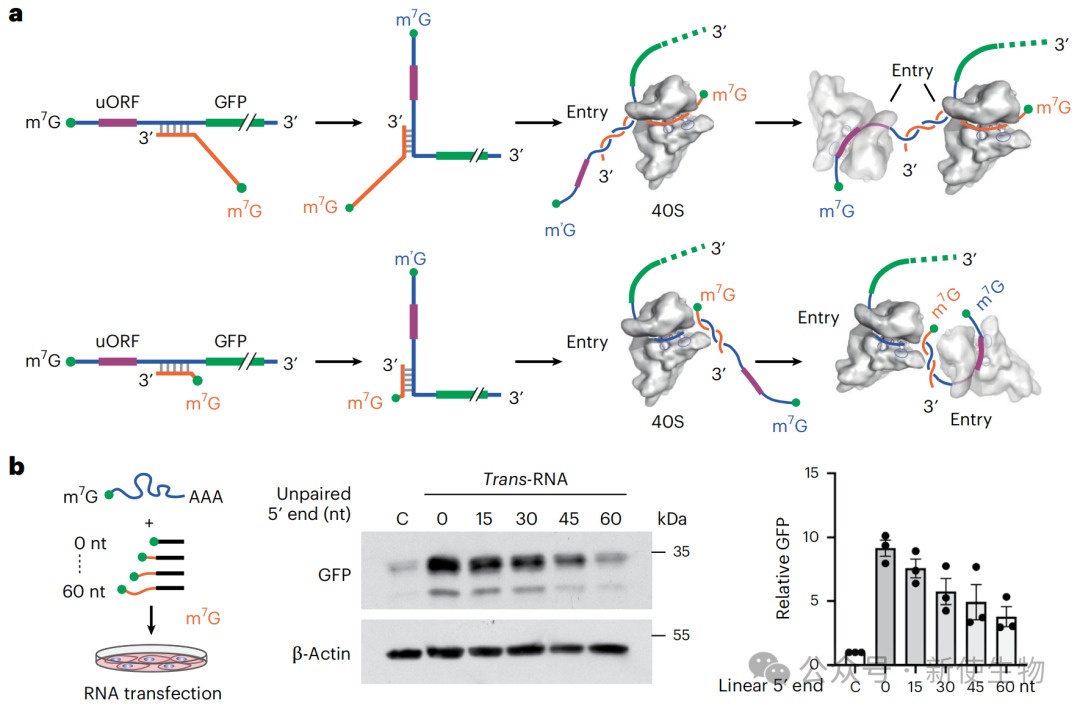
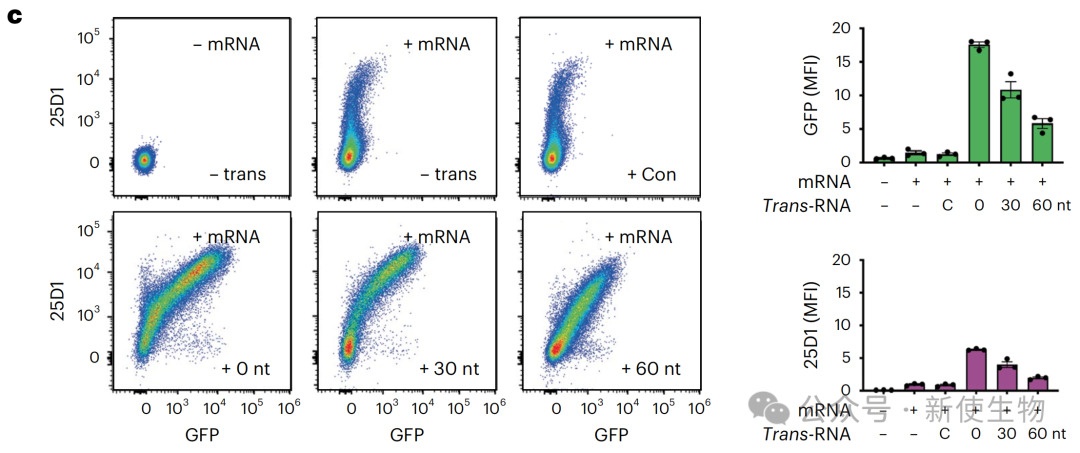
二、Trans-RNA通过协同机制促进核糖体扫描和翻译
利用实时荧光双链解旋实验,研究发现trans-RNA不仅通过自身的帽结构招募核糖体,还能与目标mRNA自身的帽结构协同作用。
这种协同作用可能通过形成一种环状结构,促进了从目标mRNA帽结构加载的核糖体的扫描效率。
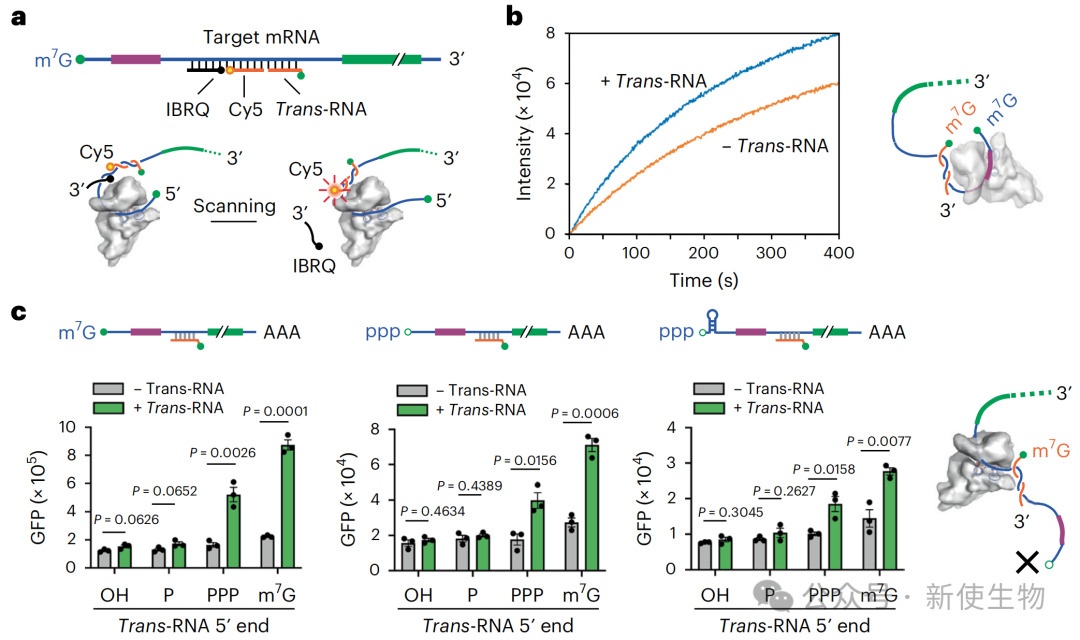
三、Trans-RNA的作用独立于靶标mRNA自身的帽结构
实验证明,即使靶标mRNA没有5'端帽子或其帽结构被茎环阻断,trans-RNA依然能够有效激活其翻译,证实了trans-RNA招募核糖体的独立性。
冷冻电镜结构分析进一步揭示了核糖体在trans-RNA作用下识别非经典起始密码子的分子细节。
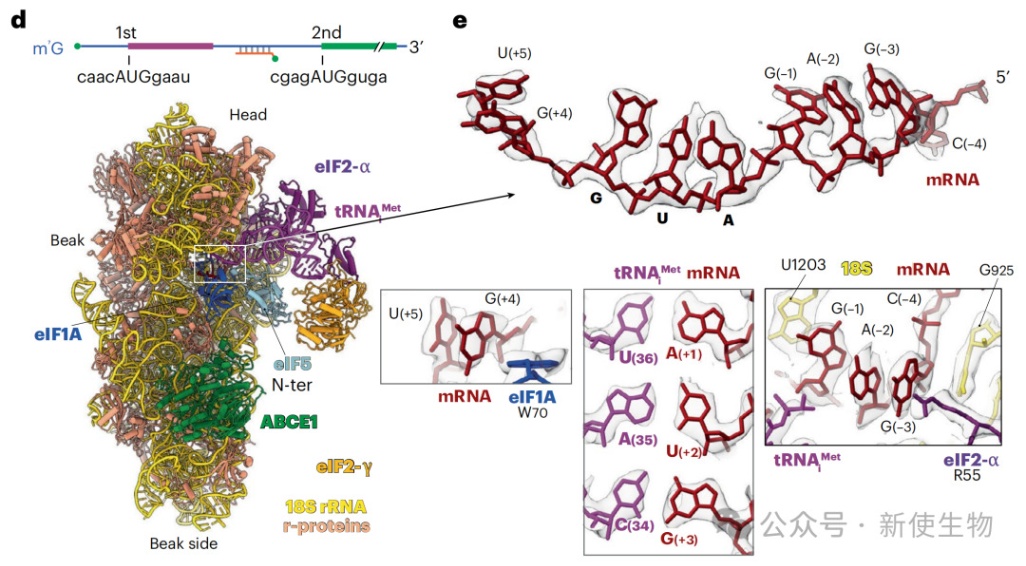
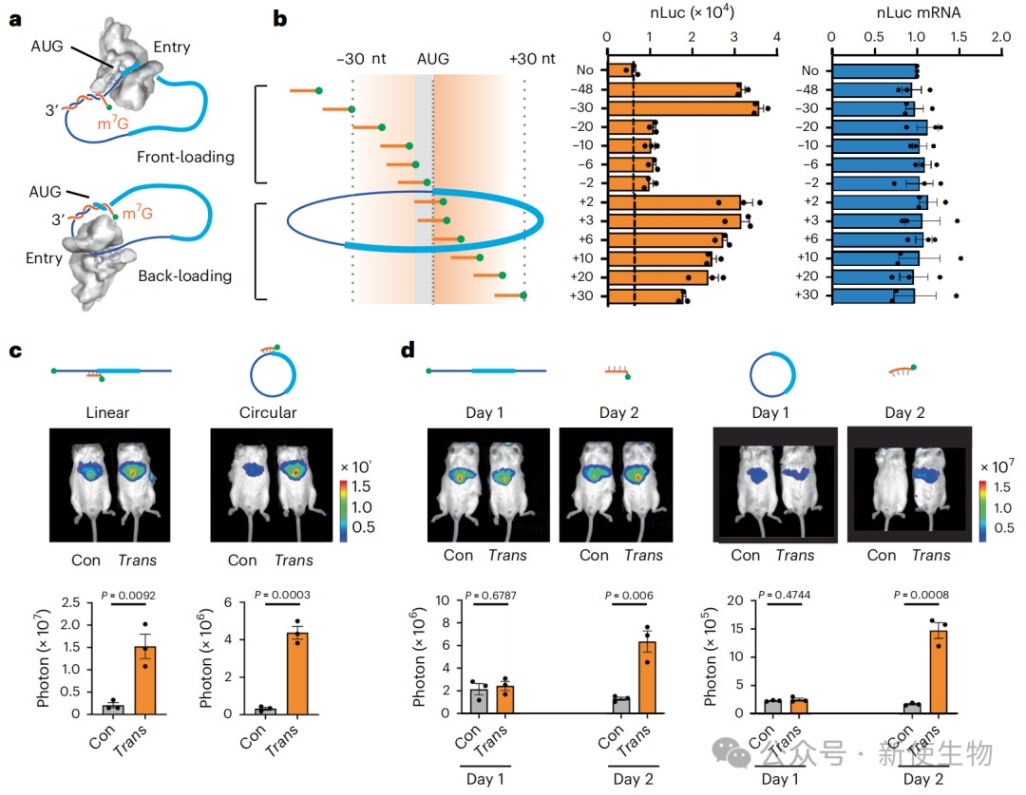
四、Trans-RNA能够驱动环状RNA(circRNA)的翻译
由于trans-RNA能够独立招募核糖体,研究人员将其应用于通常难以翻译的、不含IRES的circRNA。
实验表明,trans-RNA能够有效驱动circRNA的翻译,并且这种作用在小鼠体内通过脂质纳米颗粒(LNP)递送后依然高效,为circRNA的治疗应用开辟了新途径。
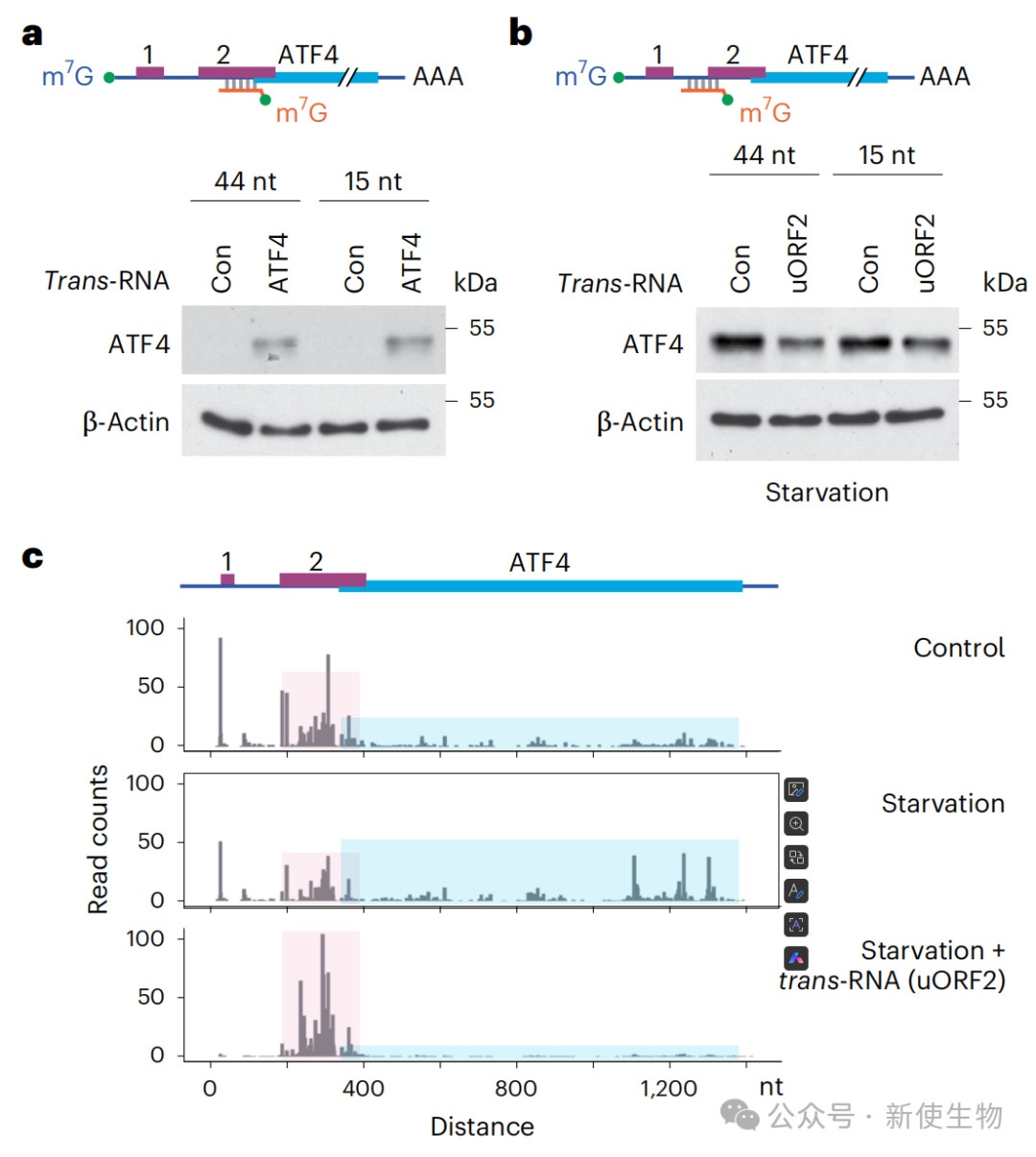
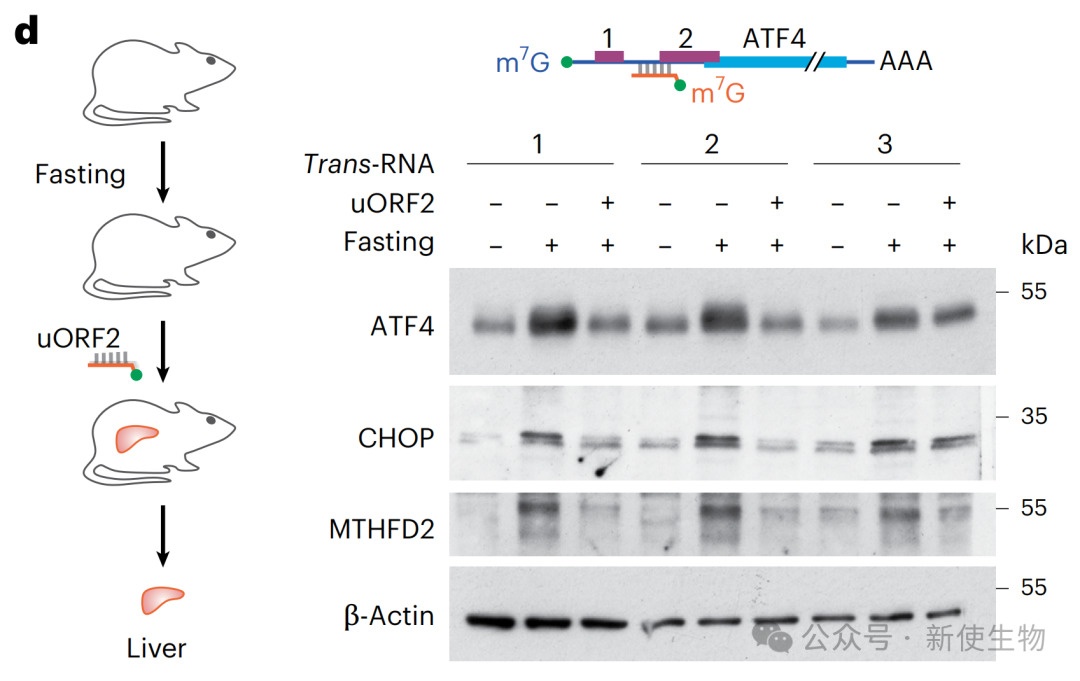
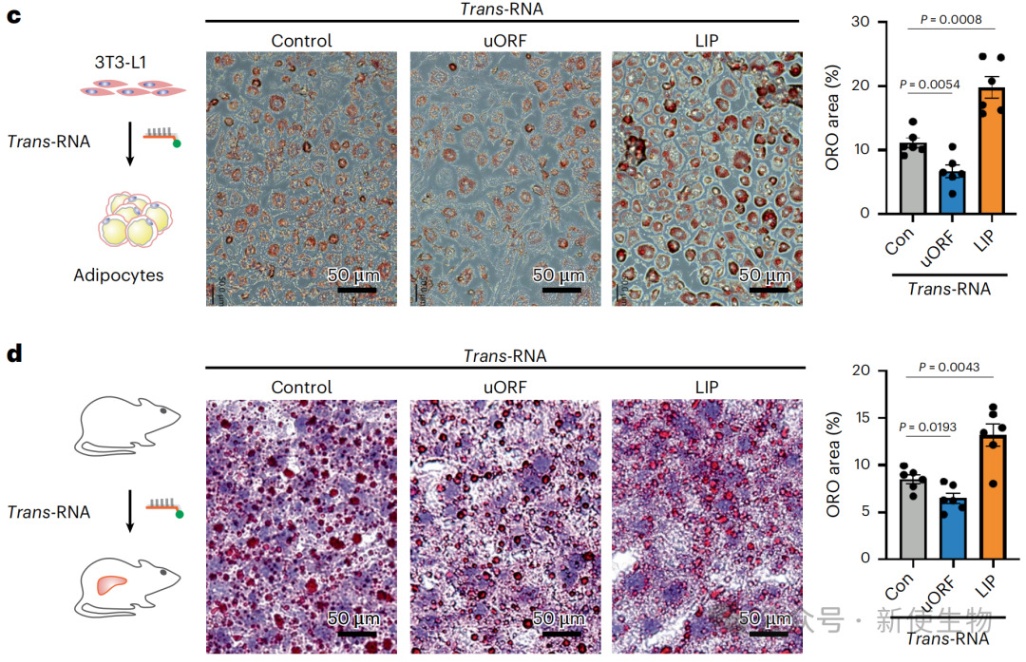
五、Trans-RNA实现对内源基因ATF4和C/EBPβ选择性翻译的调控
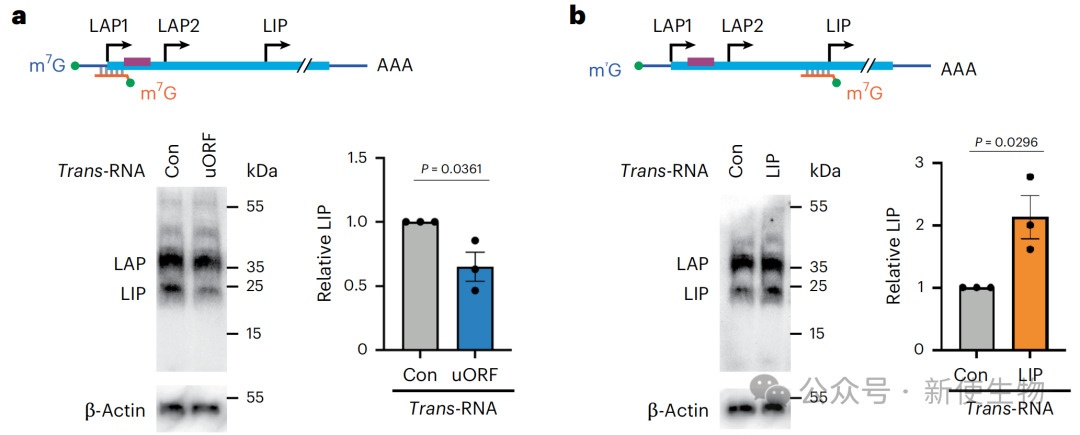
同样地,通过靶向C/EBPβ的不同起始密码子,可以精确调控其不同蛋白异构体(LAP和LIP)的比例,从而影响脂肪细胞分化和肝脏脂质代谢。
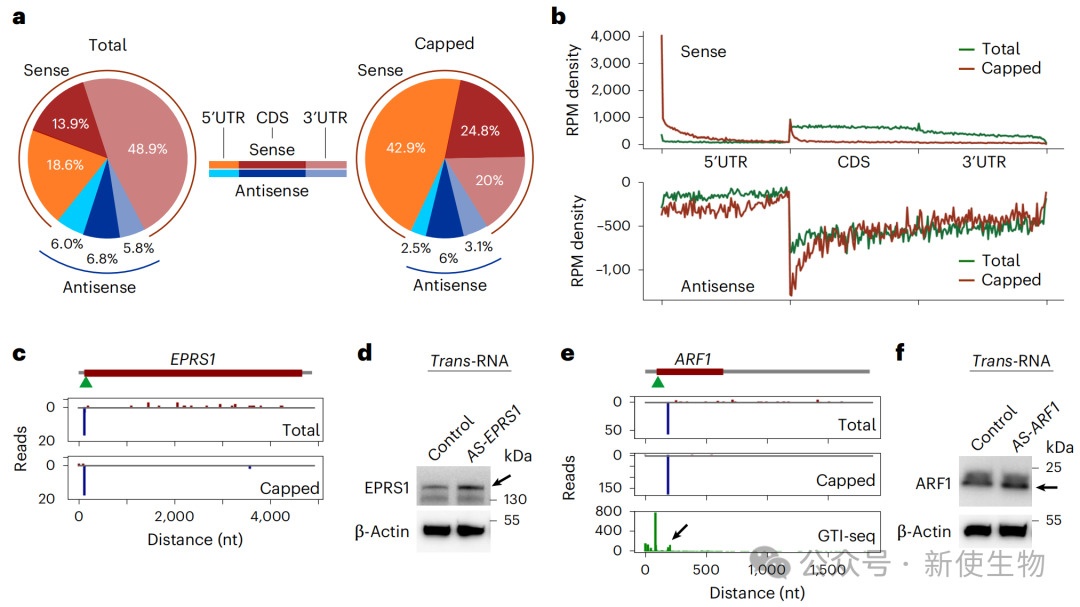
六、发现天然存在的trans-RNA作为内源性翻译调节因子
通过对细胞内带帽结构的小RNA进行测序(CapSeq),研究人员发现细胞内存在大量天然反义转录本(NATs)。
实验证明,其中一些NATs(如EPRS1-AS和ARF1-AS)能够像人工设计的trans-RNA一样,通过与同源mRNA结合来激活或调控其翻译,揭示了一种新的内源性翻译调控机制。
总结
本研究开发了一种创新的trans-RNA技术,首次实现了对细胞内单个mRNA翻译起始的可编程控制。该技术不仅为研究选择性翻译起始提供了强大的工具,还通过激活环状RNA翻译和调控内源基因功能,为RNA疗法带来了巨大的应用潜力,并揭示了天然存在的反义转录本可能作为内源性trans-RNA发挥着广泛的翻译调控作用。
| 新使生物专业翻译组一站式服务平台 |
| 产品名称 |
我们能够针对微量细胞或组织,如卵母细胞、卵巢、临床穿刺样品等产出高质量翻译组数据结果。
超高的准确性为研究非经典的开放阅读框(ORFs)提供极大便利,提高微肽(肿瘤新生抗原)的挖掘效率。
另外新使生物提供多物种多聚核糖体分析(Polysome profiling),了解更多翻译组技术信息可登录 www.neoribo.com。
点击图片查看
点击图片查看


 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们
