Poly(A)尾(pA)和PABP(酵母中为Pab1)可促进翻译起始,可能通过eIF4E、eIF4G和PABP介导的闭环mRNP形成。在哺乳动物细胞,PABP缺失削弱eIF4F结合并抑制翻译,但对单个mRNA的翻译效率(TE)影响有限,可能因PABP丰度高或短pA尾mRNA选择性降解。
酵母中TE与pA尾长度无关,Pab1–eIF4G相互作用非必需,仅部分mRNA富集eIF4E/eIF4G/Pab1,影响翻译效率差异。
PABP亦调控mRNA降解,可促进去腺苷化,也能防止mRNA去帽降解。在酵母中,Pab1缺失导致未去腺苷化mRNA经Xrn1降解。PABP缺失降低哺乳动物mRNA总量,如果酵母也是如此,那可能会影响mRNA与43S PIC或RBPs的平衡,进而调控翻译效率。

索引
【IF】16.97
研究结果
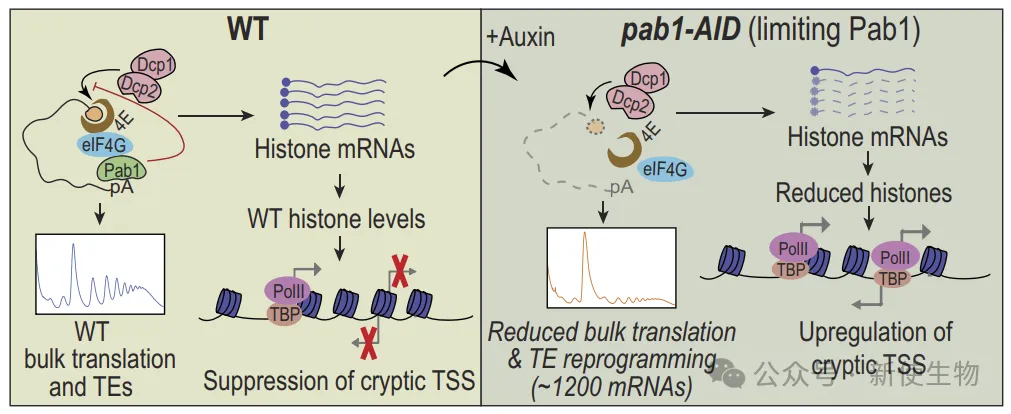
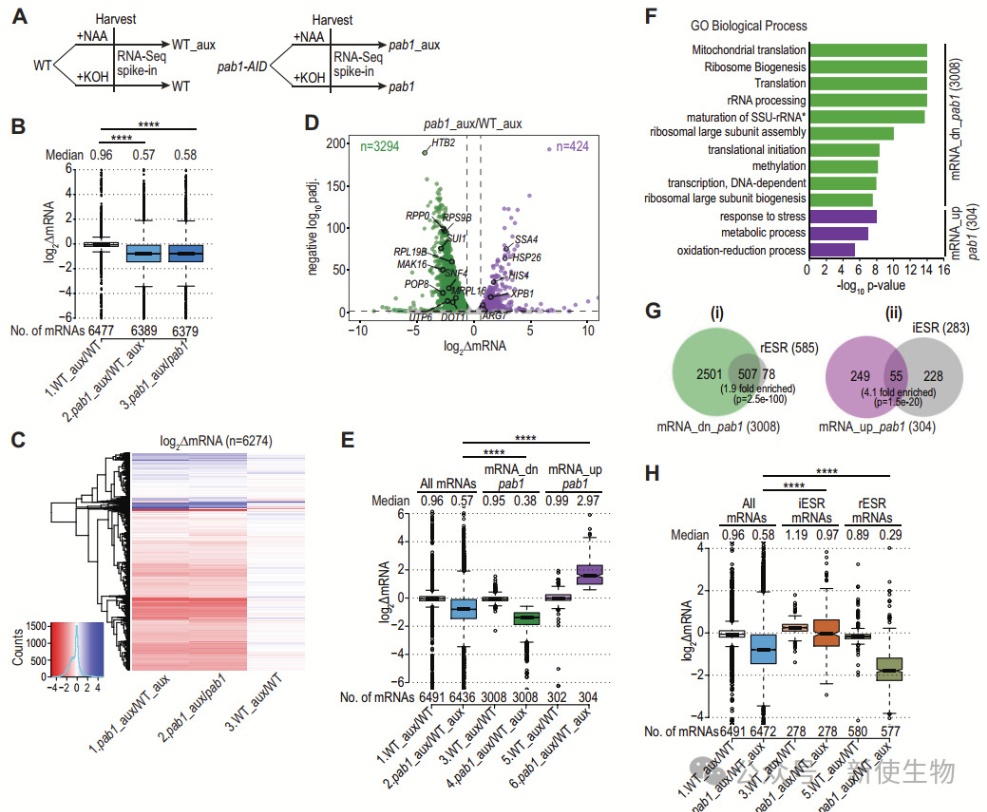
Pab1在酵母中维持mRNA稳定性。Pab1-AID耗竭后,整体mRNA丰度下降,大多数mRNA下调(3294种),少数上调(424种)。
GO分析显示,下调mRNA富集于翻译和核糖体生物合成,上调mRNA主要参与应激响应。Pab1-AID耗竭还降低核糖体丰度,并调控环境应激响应(ESR)相关mRNA。这些结果表明,Pab1在mRNA稳定性和基因表达调控中发挥广泛作用。
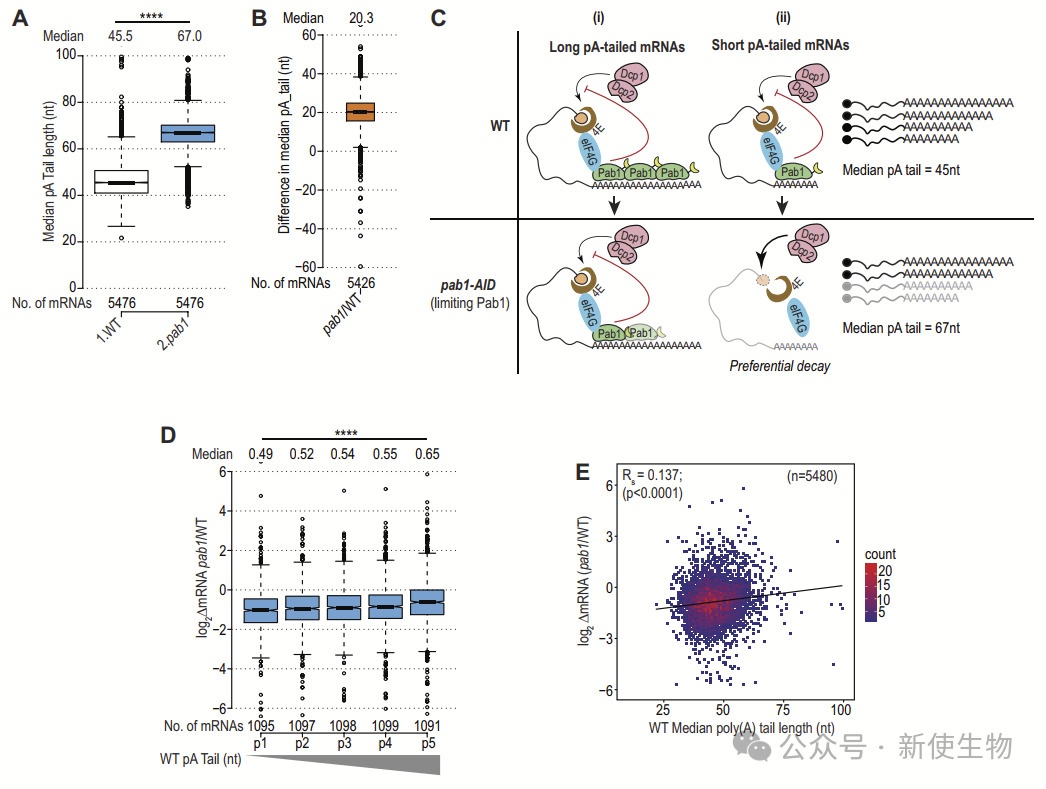
作者接下来探讨了Pab1-AID耗竭对pA尾长度的影响,通过对处理过生长素的pab1-AID和野生型细胞进行单分子pA尾序列分析(SM-PAT-Seq)。
结果显示,Pab1-AID的耗竭在整个转录组中导致pA尾长度显著增加。大多数基因的pA尾长度中位数增加了20个碱基对。这个变化可能是由于短尾mRNA的降解增加,尤其是短尾的转录本在Pab1耗竭时优先去帽和降解。
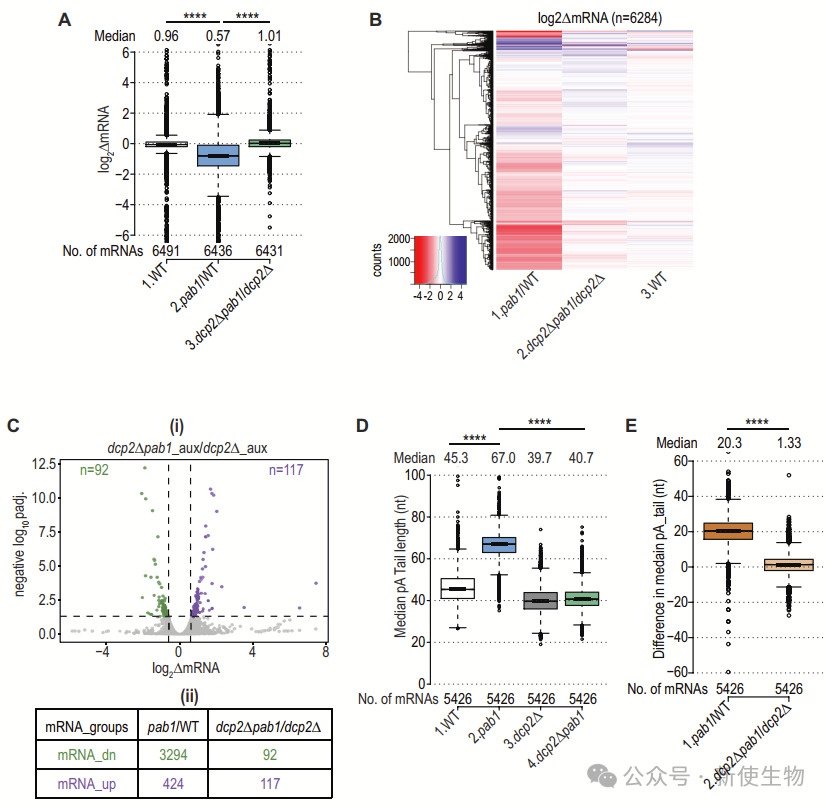
此外,通过在缺失Dcp2的突变体中观察Pab1-AID的耗竭效果,他们发现Pab1-AID的耗竭对pA尾长度的增加在dcp2Δ突变体中消失,进一步支持了Pab1通过促进短尾转录本的去帽和降解来调控pA尾的长度。
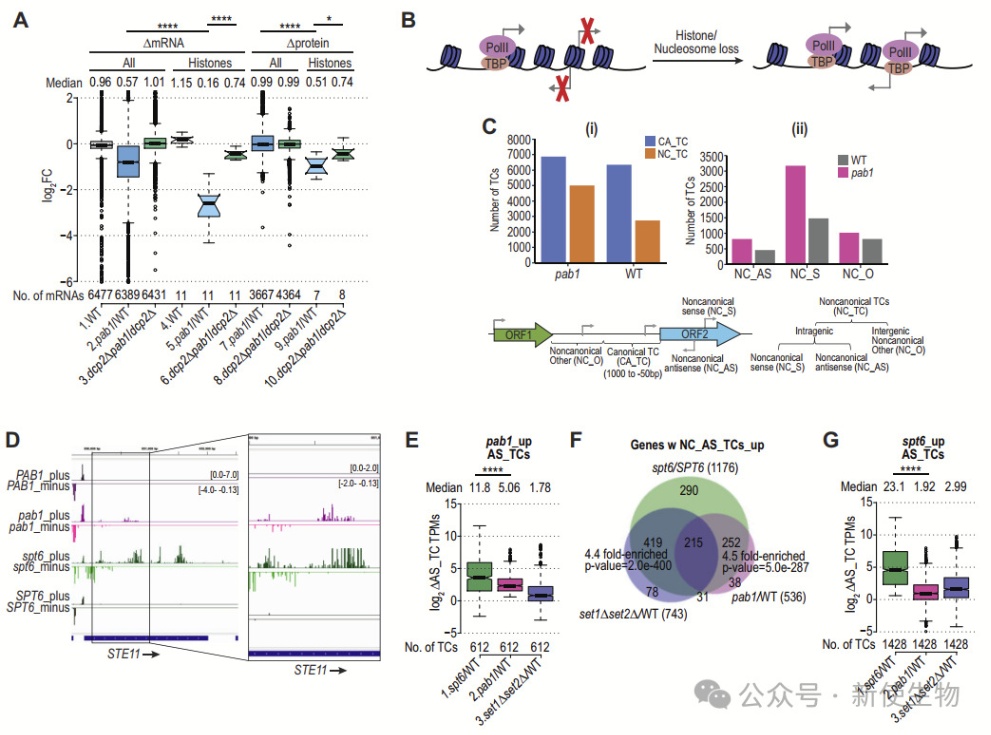
Pab1-AID缺失导致组蛋白mRNA和蛋白的表达显著减少,主要通过增加去帽和降解作用引起。
尽管S期时间未明显缩短,DNA含量略有增加,但核小体密度的减少激活了基因中的隐性启动子。这一过程与Spt6和Set1/Set2等组蛋白修饰因子相关,表明Pab1通过调控这些因子影响核小体稳定性和基因表达。
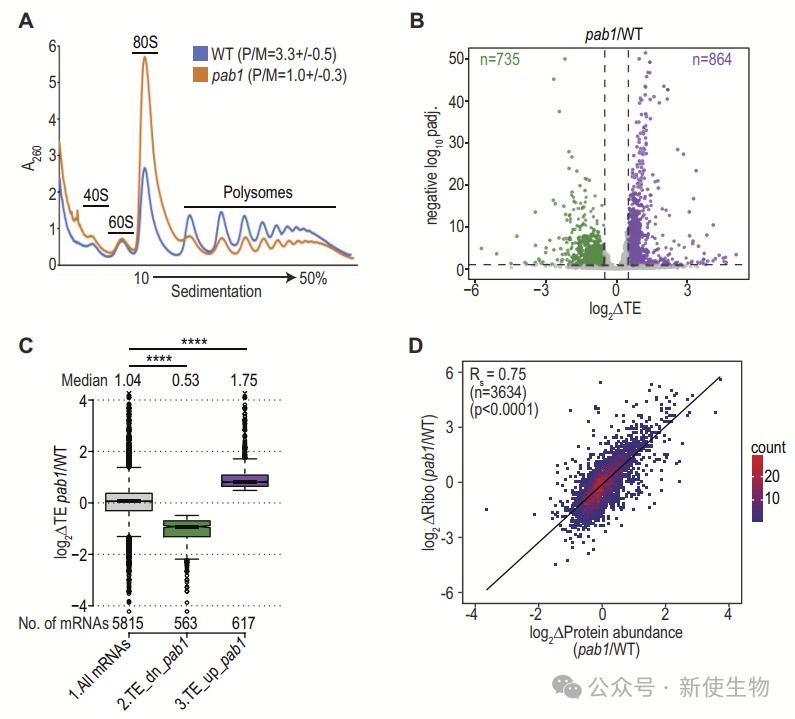
在分析Pab1缺失对翻译组的影响时,作者使用了Polysome profiling多聚核糖体分析和Ribo-seq核糖体印迹分析对pab1-AID突变体进行检测。
Polysome profiling多聚核糖体分析结果表明,Pab1缺失导致整体翻译显著下降,具体表现为多聚核糖体的减少和80S单核糖体的积累,多聚核糖体/核糖体单体(P/M)比率在经植物激素处理的pab1-AID细胞中下降约3倍。
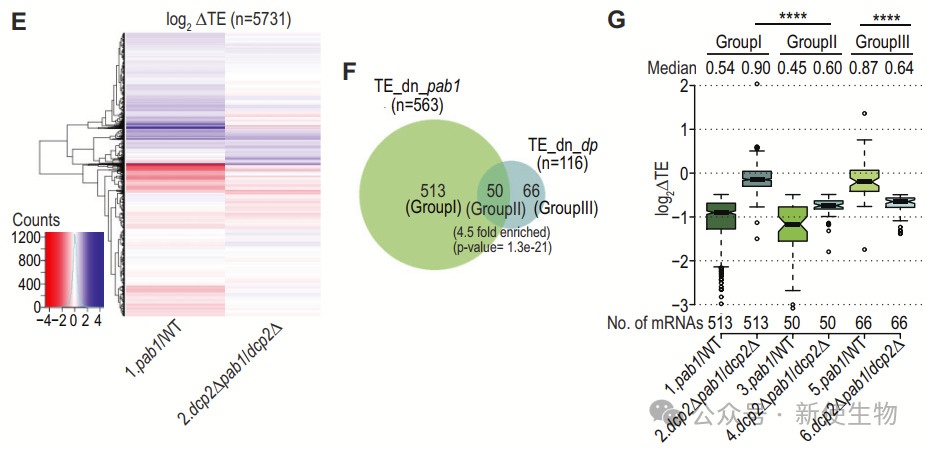
进一步的Ribo-seq核糖体印迹分析分析发现,Pab1缺失导致735种mRNA的翻译效率(TE)下降,而864种mRNA的翻译效率上升。此外,翻译效率变化与蛋白质合成速率的变化相关,TMT质谱数据表明,翻译效率的变化在稳态蛋白质丰度上也产生了相应的影响。
翻译效率下降的mRNA表现出较低的转录水平,而翻译效率上升的mRNA则显示出较高的相对转录水平。
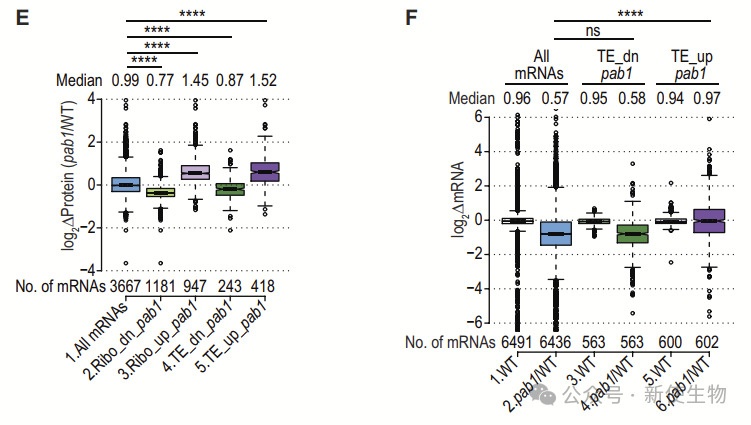
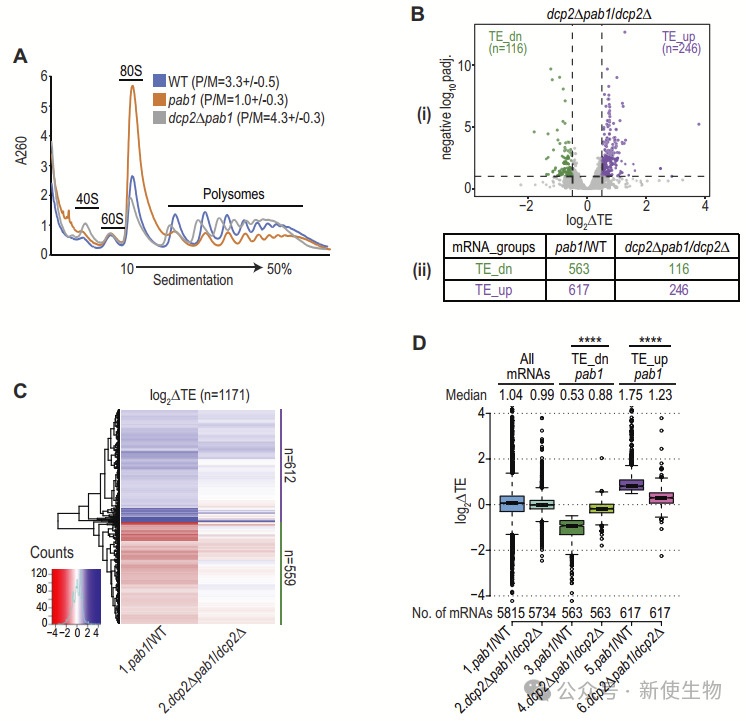
Pab1-AID缺失导致的多聚核糖体组装减少依赖于Dcp2的mRNA去帽作用,而非Pab1直接促进翻译启动的功能。
在dcp2Δ突变体中,Pab1-AID缺失未引起显著的翻译重编程,翻译效率变化较小,表明翻译变化主要是由于mRNA丰度的降低。此外,一些mRNAs在dcp2Δ细胞中表现出仅由Pab1直接调控的翻译变化。
TMT-MS分析显示,翻译变化与蛋白质表达变化高度相关,进一步支持Pab1在翻译重编程中的作用,独立于其在控制mRNA丰度中的功能。
本文研究表明,Pab1通过增强去帽和降解作用影响mRNA的丰度,进而改变翻译效率。Pab1缺失在Dcp2突变体中未观察到这种影响,表明mRNA丰度减少是翻译重编程的主要驱动力。Pab1还通过调控组蛋白基因的转录后表达,参与组蛋白mRNA和蛋白质的降解。
我们能够针对微量细胞或组织,如卵母细胞、卵巢、临床穿刺样品等产出高质量翻译组数据结果。
超高的准确性为研究非经典的开放阅读框(ORFs)提供极大便利,提高微肽(肿瘤新生抗原)的挖掘效率。
另外新使生物提供多物种多聚核糖体分析(Polysome profiling),了解更多翻译组技术信息可登录 www.neoribo.com
点击图片查看
点击图片查看


 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们
