
脊椎动物嗅觉系统遵循“每个神经元一个受体”和“每个嗅球小体一个受体”的原则,将嗅觉受体(OR)基因选择转化为轴突导向的特异性。OR的DNA、mRNA和蛋白质通过调控彼此的表达,确保这一过程的精确性。
OR蛋白通过内质网激活Perk信号,促进单一OR选择。尽管早期神经前体细胞会共同转录多个OR基因,Perk信号和神经活动无法精细调控轴突导向。
为了避免OR蛋白在此阶段过早影响轴突导向,必须通过后转录机制抑制共转录的OR基因的表达,直到单一OR转录完成。然而,这一机制尚未在发育中的嗅觉上皮中得到直接验证。
2025年7月20日,哥伦比亚大学Stavros Lomvardas团队在Cell Reports上发表了一篇题为“Mex3a-dependent post-transcriptional silencing ensures olfactory receptor diversity and axon guidance specificity”的论文,发现RNA结合蛋白Mex3a在未成熟的嗅觉神经元中有效阻止了多种OR mRNA的翻译。这一机制确保了神经元在最终确定表达单一OR之前不会产生混乱的蛋白质信号,从而保障了嗅觉受体基因选择的多样性。

文章索引
【发表期刊】Cell Reports
【发表日期】2025年7月20日
【作者及团队】哥伦比亚大学Stavros Lomvardas团队
【IF】7.5
研究结果
一、Mex3a使嗅觉神经元中的OR表达沉默
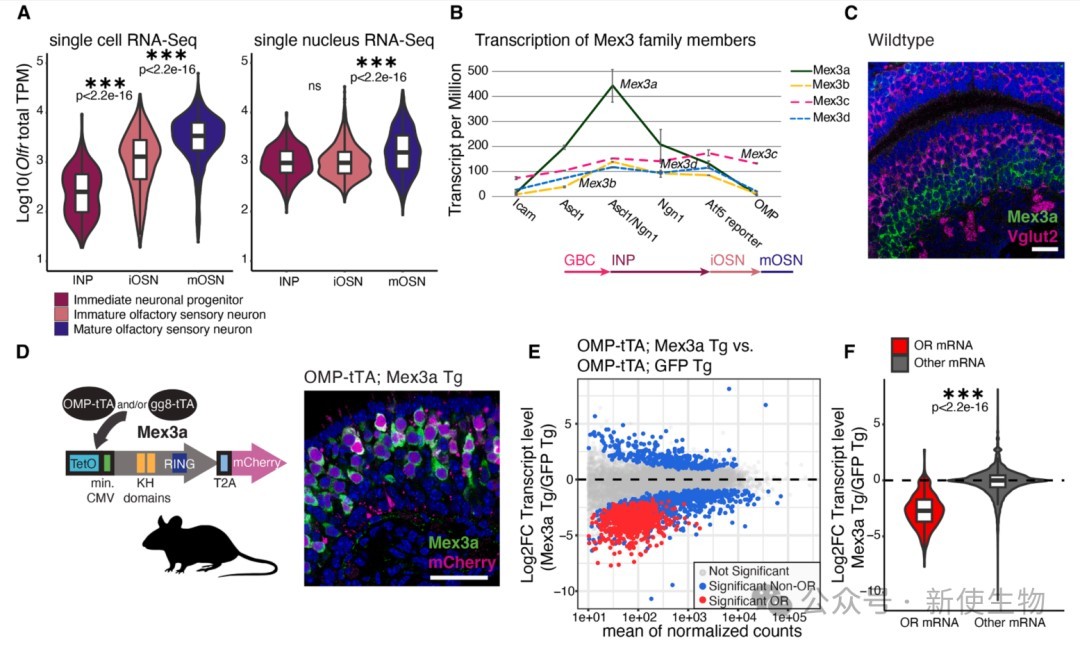
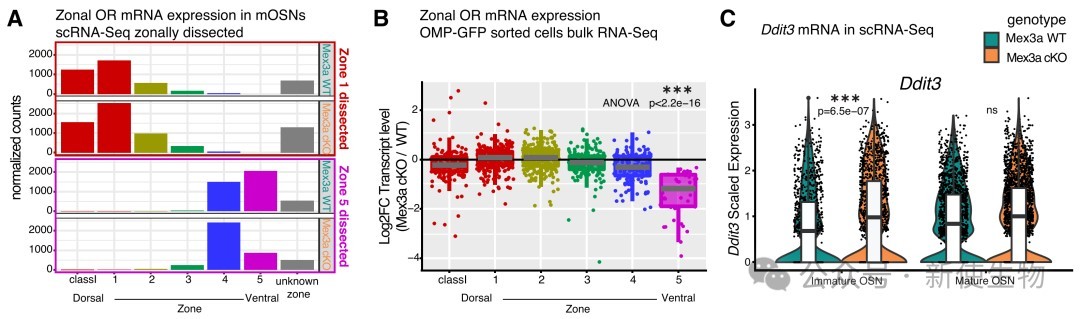
研究发现,Mex3a蛋白特异性地在表达多种OR的未成熟嗅觉神经元(OSN)中高表达,而在只表达单一OR的成熟OSN中则不表达。
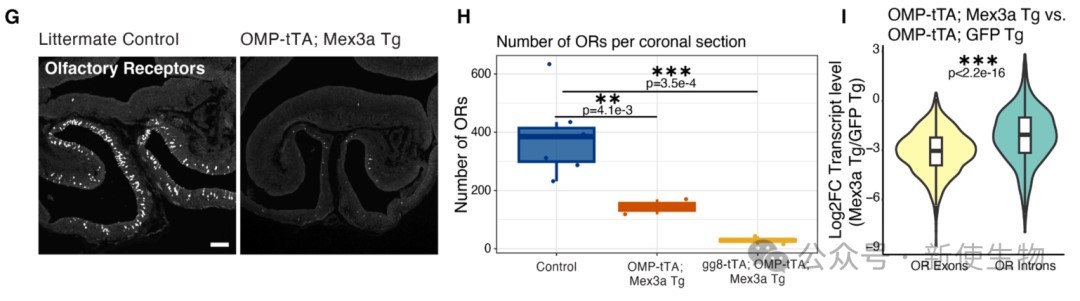
通过构建转基因小鼠,在成熟OSN中强制表达Mex3a,结果显示绝大多数OR的mRNA和蛋白水平均被显著抑制。
进一步分析发现,Mex3a对OR mRNA外显子的抑制效果远强于内含子,这有力地证明了其作用于转录后环节,即抑制已生成的mRNA。
二、Mex3a互作蛋白组鉴定已知后转录调控作用的蛋白
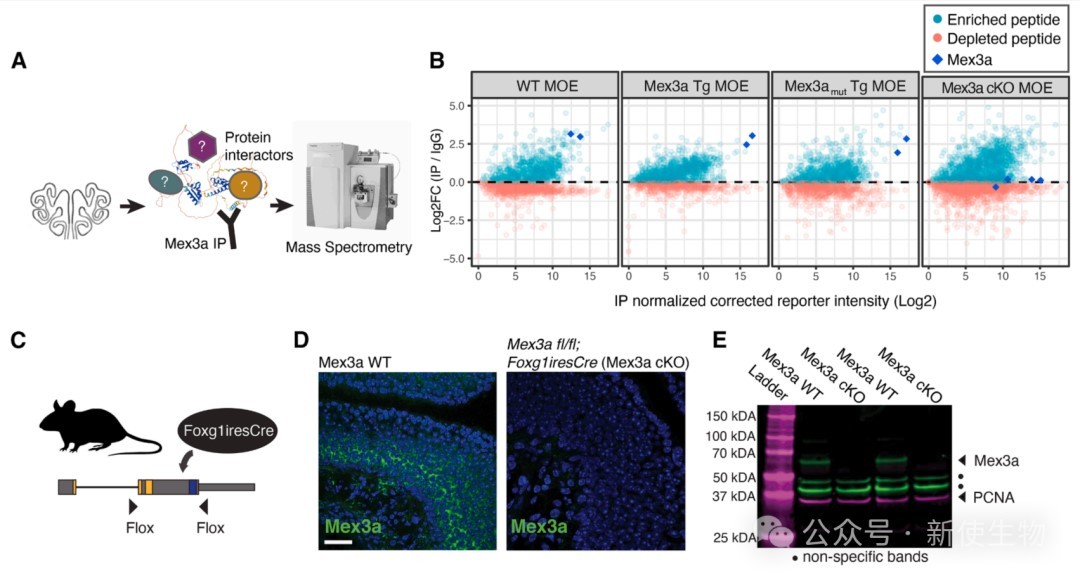
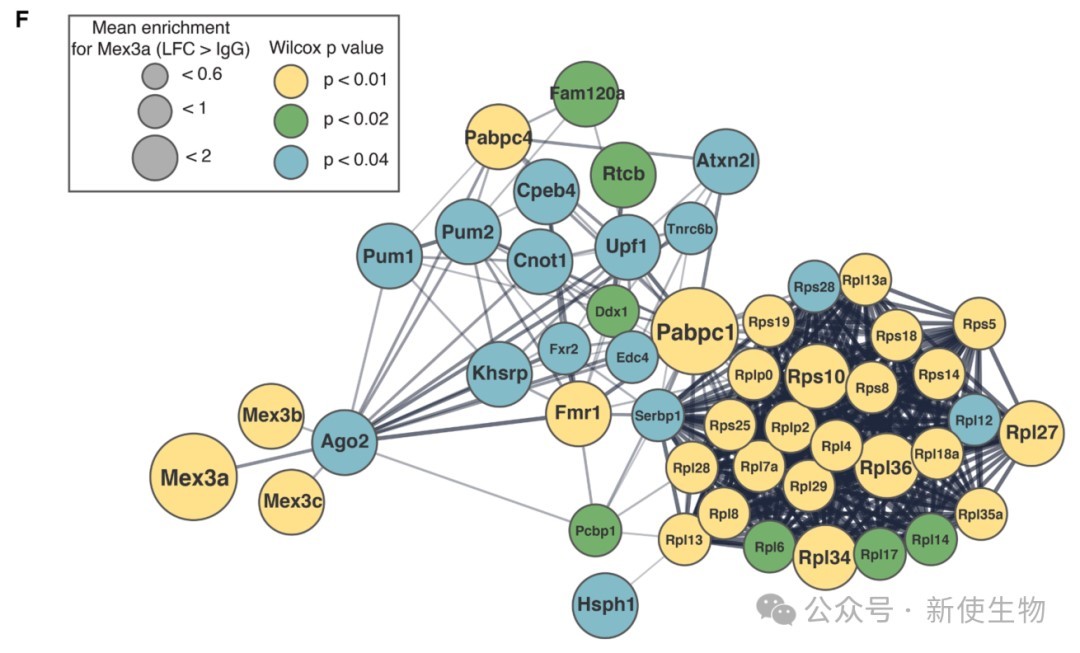
通过免疫沉淀-质谱(IP-MS)分析,研究团队发现在Mex3a的互作组中富集了大量已知参与转录后沉默、mRNA降解和翻译调控的RNA结合蛋白,以及核糖体蛋白。
这些发现与Mex3a作为一种转录后调控因子,通过影响OR mRNA的稳定性或翻译来沉默OR表达的假说一致。
三、利用Mex3a转基因小鼠实现对OR的转录后沉默
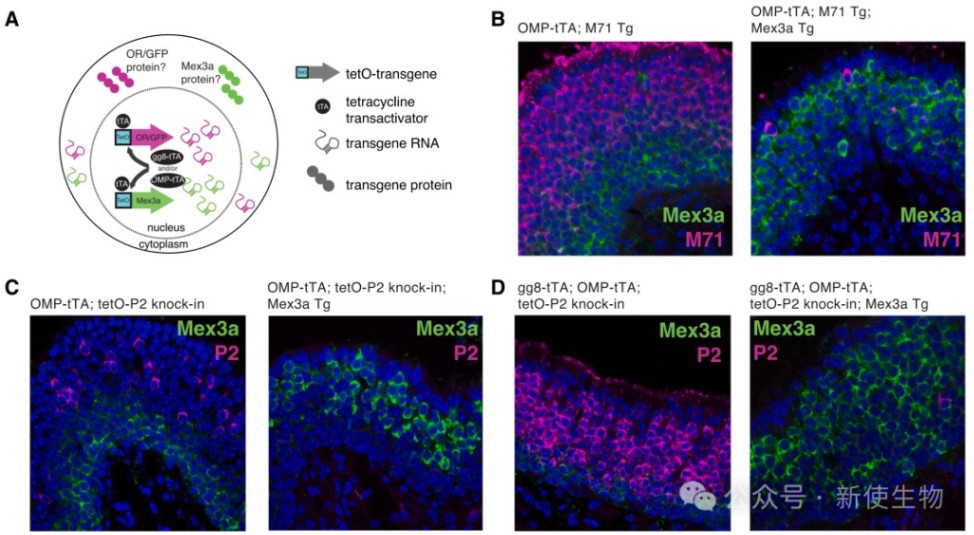
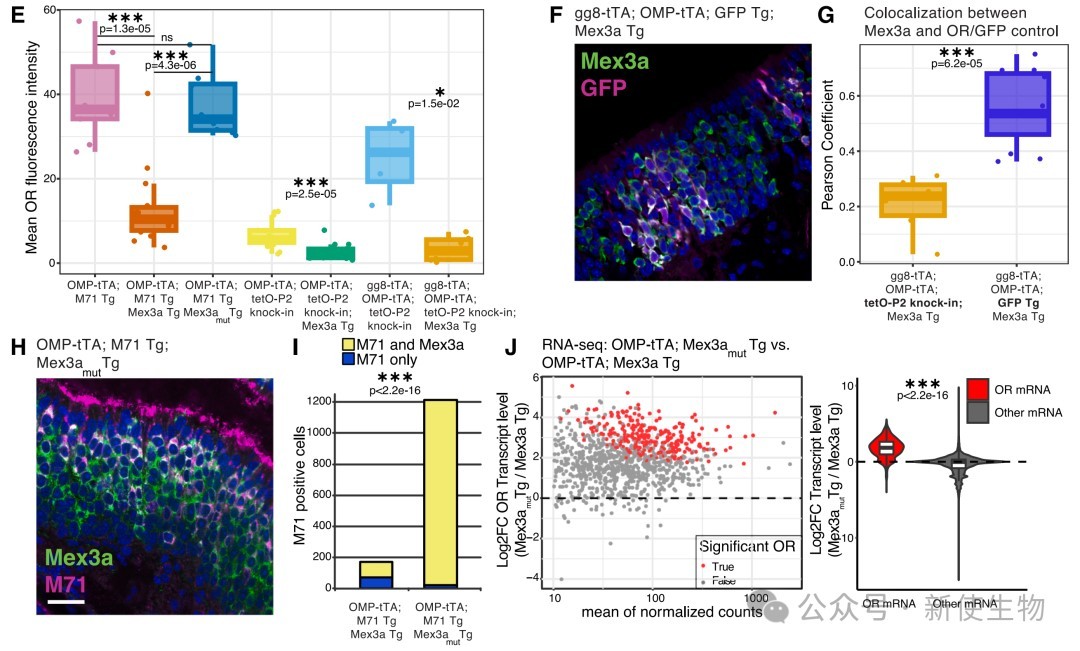
研究者通过将Mex3a转基因与表达特定OR(如M71或P2)的转基因相结合,构建了复合转基因小鼠。
结果显示,当Mex3a存在时,这些OR转基因的表达频率显著降低,证明Mex3a对OR基因的沉默作用是转录后层面的,并且选择性针对OR序列,而非其他非OR转基因。
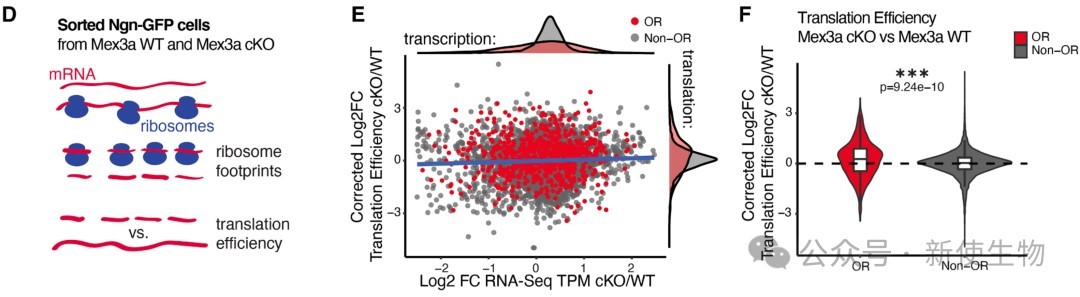
此外,Mex3a缺失会使OR mRNA翻译效率增加,且这种增加不影响其他非OR mRNA,进一步证实了Mex3a对OR mRNA的特异性转录后调控。
四、Mex3a缺失导致OR的过早表达
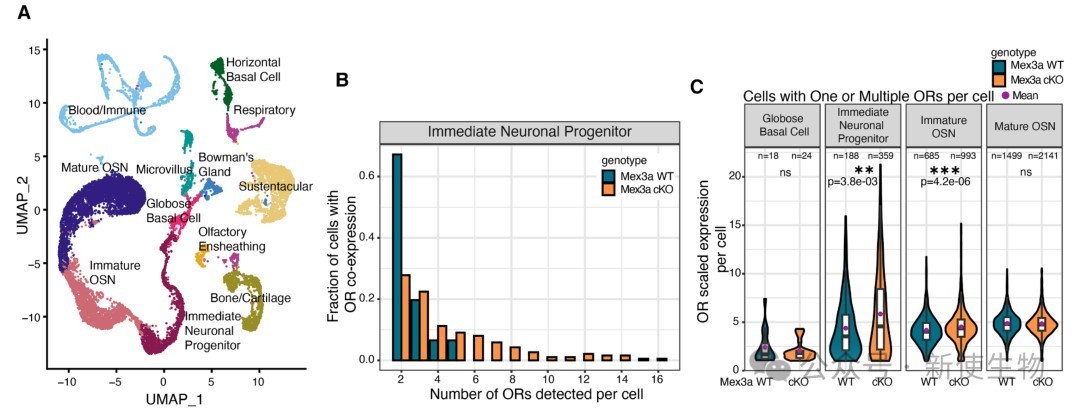
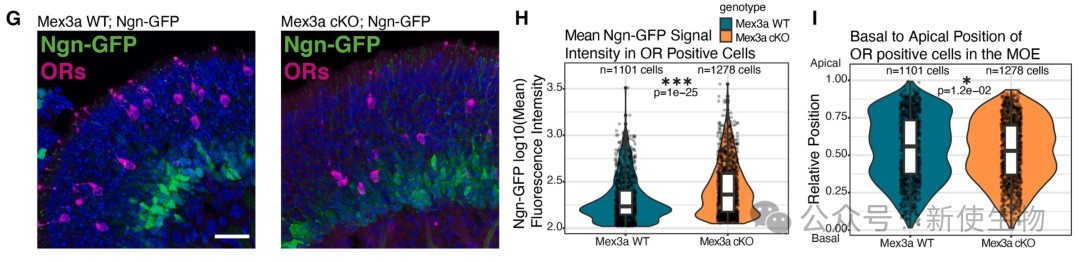
Ribo-seq核糖体印迹分析显示,在Mex3a条件性敲除(cKO)小鼠的OSN前体细胞中,OR mRNA的表达水平和翻译效率均显著升高。
OR的提前表达也导致了内质网应激标志物PERK信号通路激活因子Atf5的提前和增强表达,以及其下游靶基因的转录激活。
五、Perk诱导的转录因子Atf5及其靶标在Mex3a条件性敲除(cKO)小鼠中表达上调
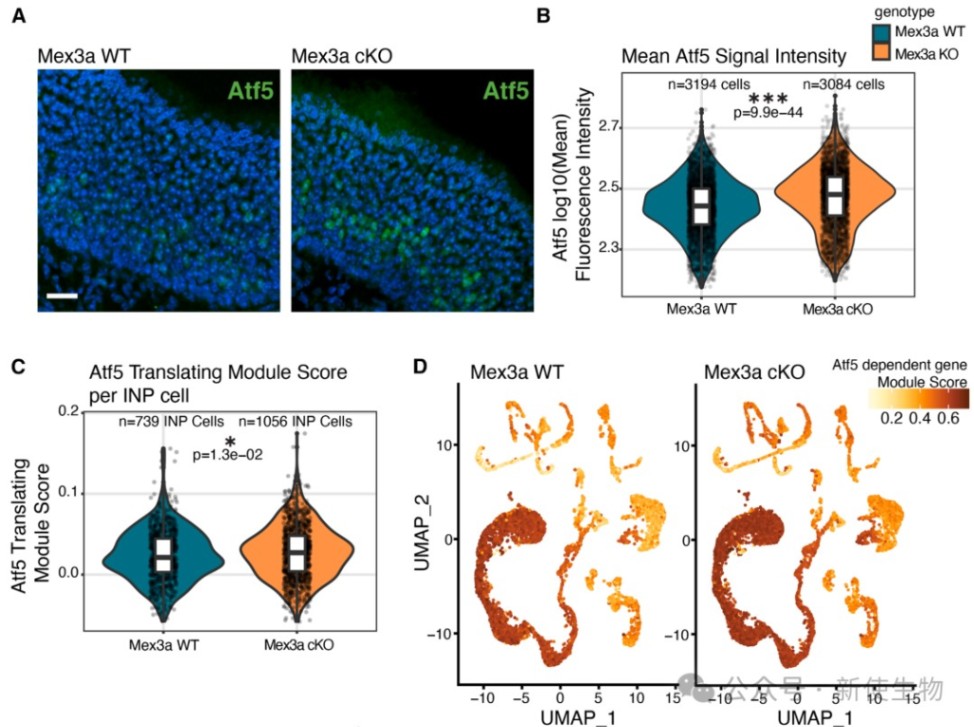
免疫荧光显示,在Mex3a cKO小鼠中,PERK信号通路的关键下游因子Atf5蛋白的表达量显著升高。
进一步通过单细胞RNA测序分析,发现在Mex3a cKO小鼠的OSN前体细胞(INPs)中,与Atf5翻译相关的基因模块评分也显著提高,表明PERK信号通路在更早的神经元发育阶段就被激活。
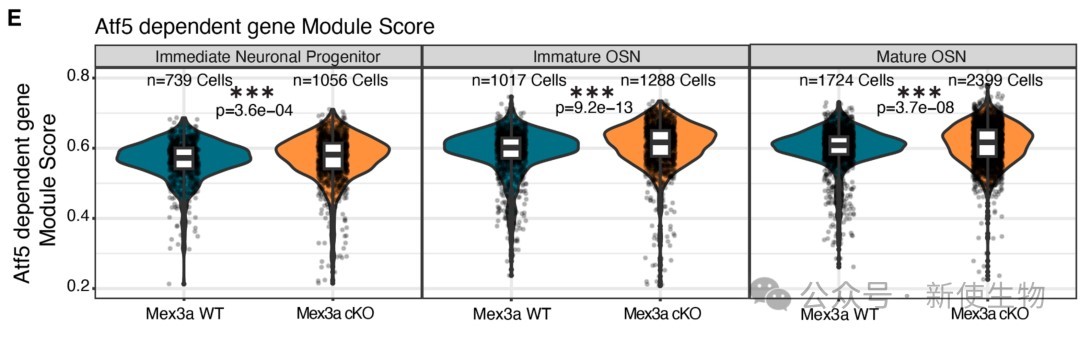
同时,定义为Atf5依赖性基因的表达也普遍升高,进一步印证了Mex3a缺失带来的PERK信号通路激活效应。
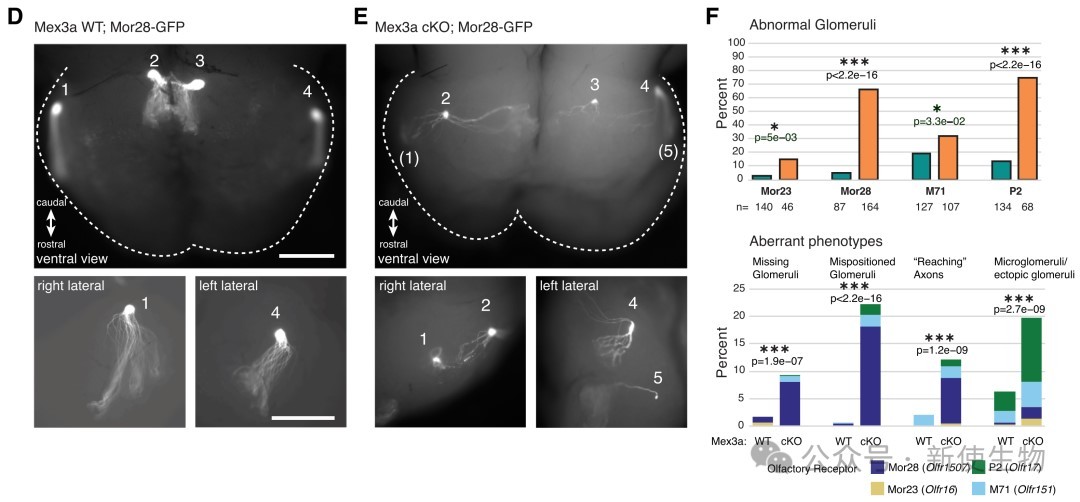
六、Mex3a缺失导致OR基因选择偏向并破坏轴突导向特异性
研究人员利用四种不同的OR-GFP报告小鼠与Mex3a敲除小鼠杂交,观察到其嗅脑球中的神经节球出现了大量布线错误。
这证明了Mex3a介导的转录后沉默对于确保嗅觉环路的精确构建极为重要。
总结
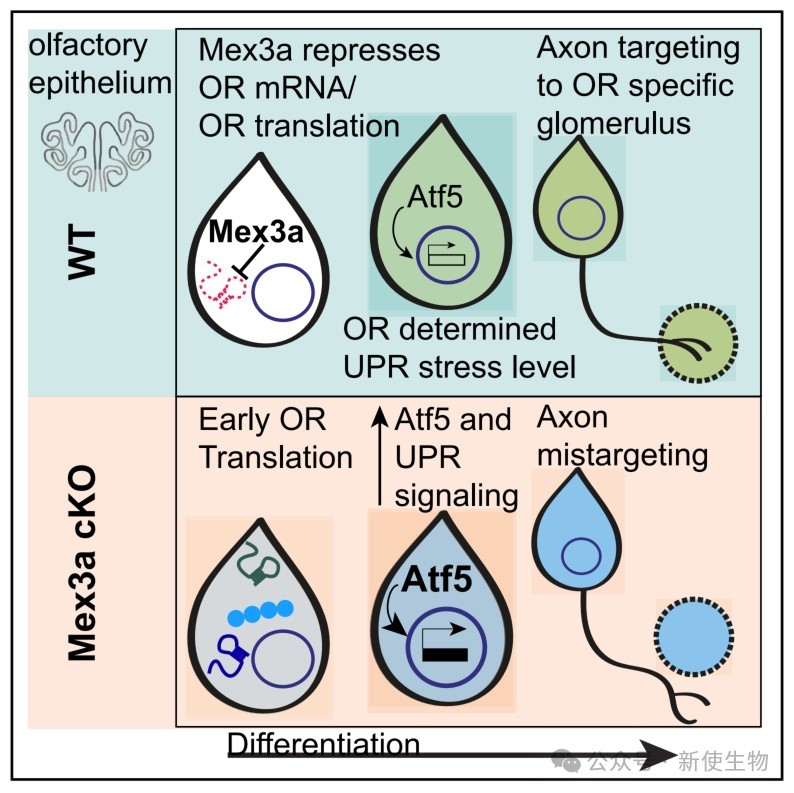
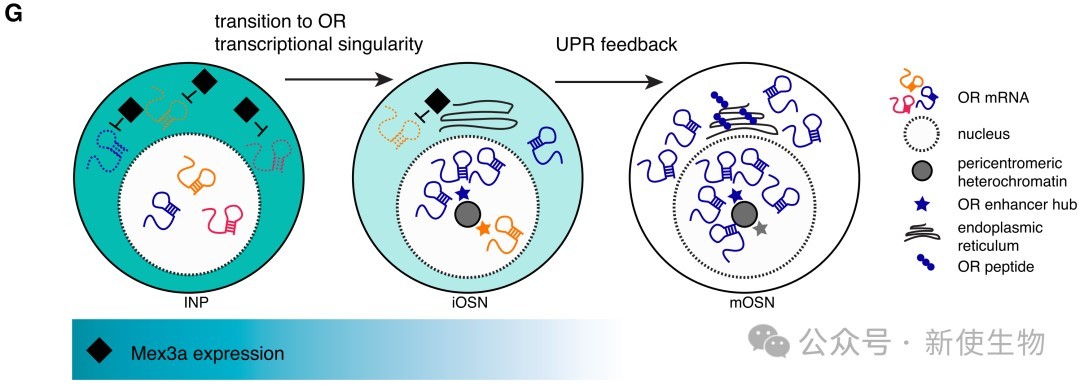
本研究发现Mex3a在未成熟嗅觉感觉神经元中通过转录后沉默机制抑制嗅觉受体(OR)基因的表达,防止过早的内质网应激信号干扰,确保单一OR选择和轴突引导的精确性。这一发现揭示了转录后基因调控在嗅觉系统发育和神经回路组装中的关键作用,为理解嗅觉受体多样性提供了新的分子机制。
我们能够针对微量细胞或组织,如卵母细胞、卵巢、临床穿刺样品等产出高质量翻译组数据结果。
超高的准确性为研究非经典的开放阅读框(ORFs)提供极大便利,提高微肽(肿瘤新生抗原)的挖掘效率。
另外新使生物提供多物种多聚核糖体分析(Polysome profiling),了解更多翻译组技术信息可登录 www.neoribo.com
点击图片查看
点击图片查看


 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们
