
导读
蛋白质翻译过程与mRNA降解紧密耦合,这一过程中的异常调控与炎症、神经功能障碍和癌症等多种病理状况相关。同义密码子的使用是影响蛋白质翻译和mRNA稳定性的关键因素,最优密码子(通常富含GC3)能促进翻译并延长mRNA寿命。
相反,含有大量非优密码子(通常富含AU3)的mRNA会被快速降解,导致翻译效率降低。在酵母中,非优密码子导致的核糖体减速会被Dhh1p和CCR4-NOT复合物感知,从而启动mRNA降解。
然而,在人类细胞中,CCR4-NOT复合物似乎更偏好性地靶向特定精氨酸密码子,这表明可能存在其他更普适性的因子参与监控和降解非优mRNA。因此,深入探究人类细胞中同义密码子使用影响mRNA周转的分子机制,对于揭示疾病机理和开发潜在治疗靶点至关重要。
2026年3月19日,日本京都大学Osamu Takeuchi与理化学研究所Takuhiro Ito和Masanori Yoshinaga团队合作,在Science上发表了一篇题为“Human DHX29 detects nonoptimal codon usage to regulate mRNA stability”的论文。该研究通过全基因组CRISPR筛选发现,RNA结合蛋白DHX29是人类细胞中调控密码子依赖性基因表达的关键因子。

文章索引
【标题】Human DHX29 detects nonoptimal codon usage to regulate mRNA stability
【发表期刊】Science
【发表日期】2026年3月19日
【作者及团队】日本京都大学Osamu Takeuchi与理化学研究所Takuhiro Ito和Masanori Yoshinaga团队
【IF】 45.8
研究结果
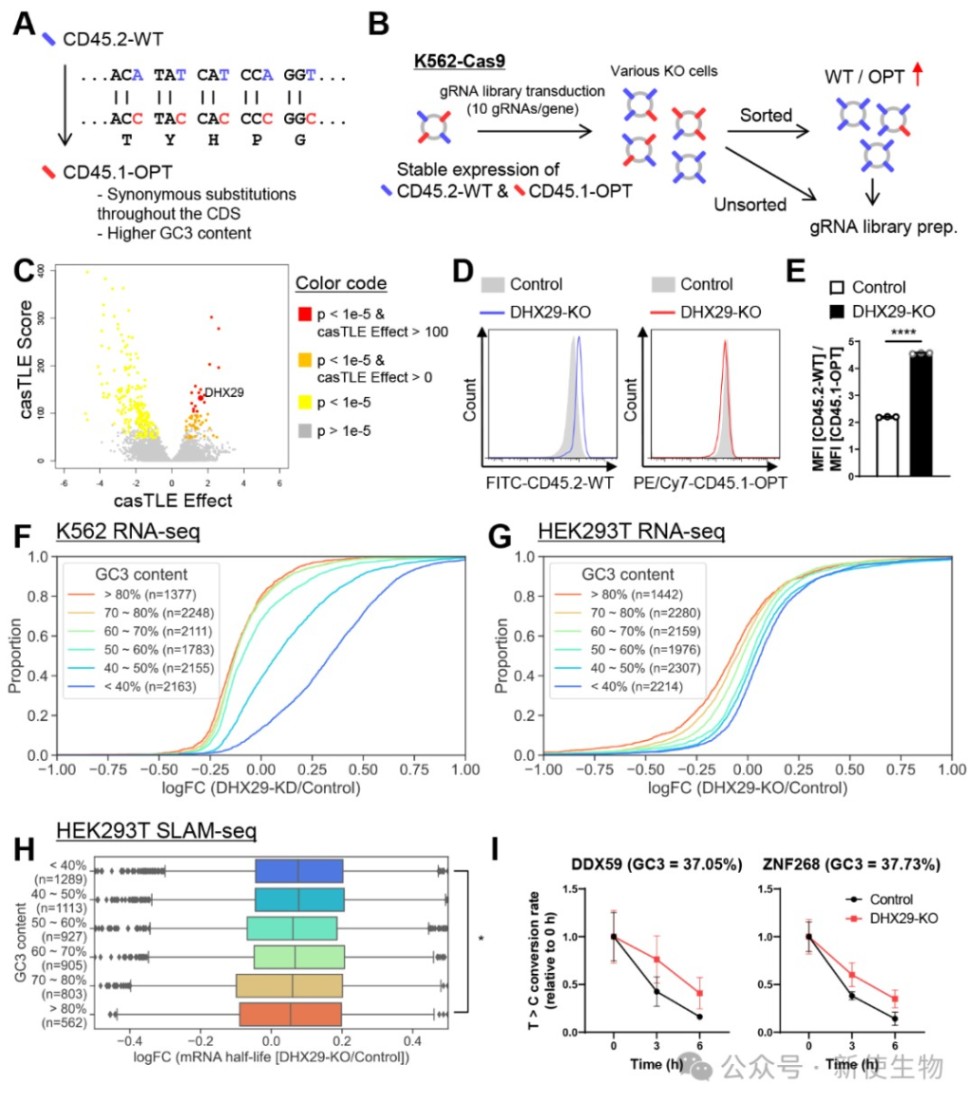
一、DHX29抑制非优密码子mRNA的表达
通过构建同义密码子报告系统并进行全基因组CRISPR筛选,研究人员发现DHX29是维持非优密码子mRNA低表达的关键蛋白。
进一步通过RNA-seq和SLAM-seq分析发现,在多种细胞系中敲低或敲除DHX29后,富含AU3密码子的非优mRNA表达水平显著上调,且其半衰期延长。
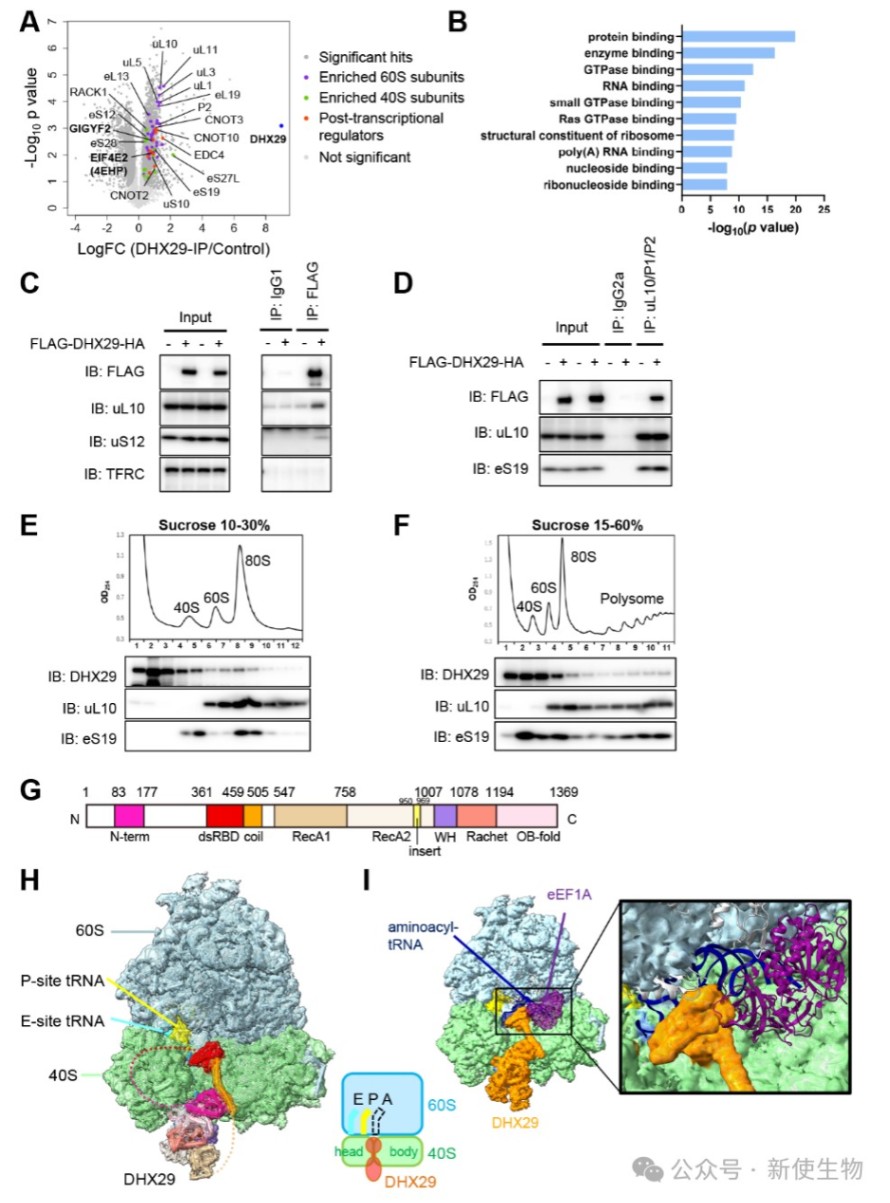
二、DHX29直接结合翻译中的80S核糖体
通过蛋白质组学和免疫共沉淀实验,证实DHX29与40S和60S核糖体亚基均有相互作用。
此外,Polysome profiling多聚核糖体分析表明,DHX29可与80S核糖体结合。
冷冻电镜(cryo-EM)结构解析进一步揭示,DHX29的dsRBD结构域精确地占据在翻译核糖体的A位点入口处,与进入的氨酰tRNA三元复合物(eEF1A•GTP•aminoacyl-tRNA)存在空间位阻,表明二者结合是相互排斥的。
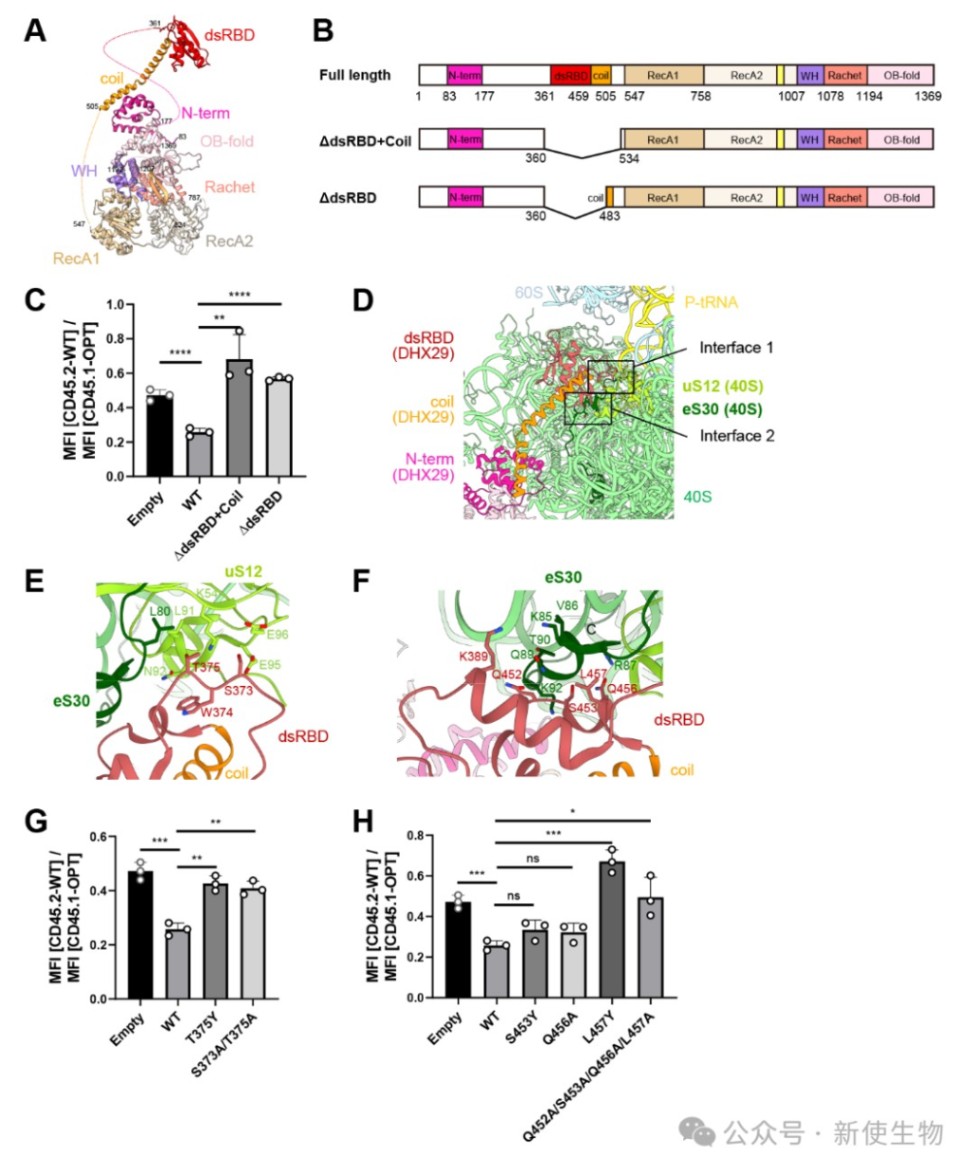
三、DHX29与A位点的相互作用是其抑制功能的关键
研究人员通过构建DHX29的结构域缺失和关键氨基酸突变体,并在DHX29敲除细胞中进行功能回补实验。
结果表明,删除与A位点入口相互作用的dsRBD结构域或破坏其与核糖体蛋白uS12和eS30的相互作用界面,均会使DHX29丧失抑制非优密码子mRNA表达的能力。
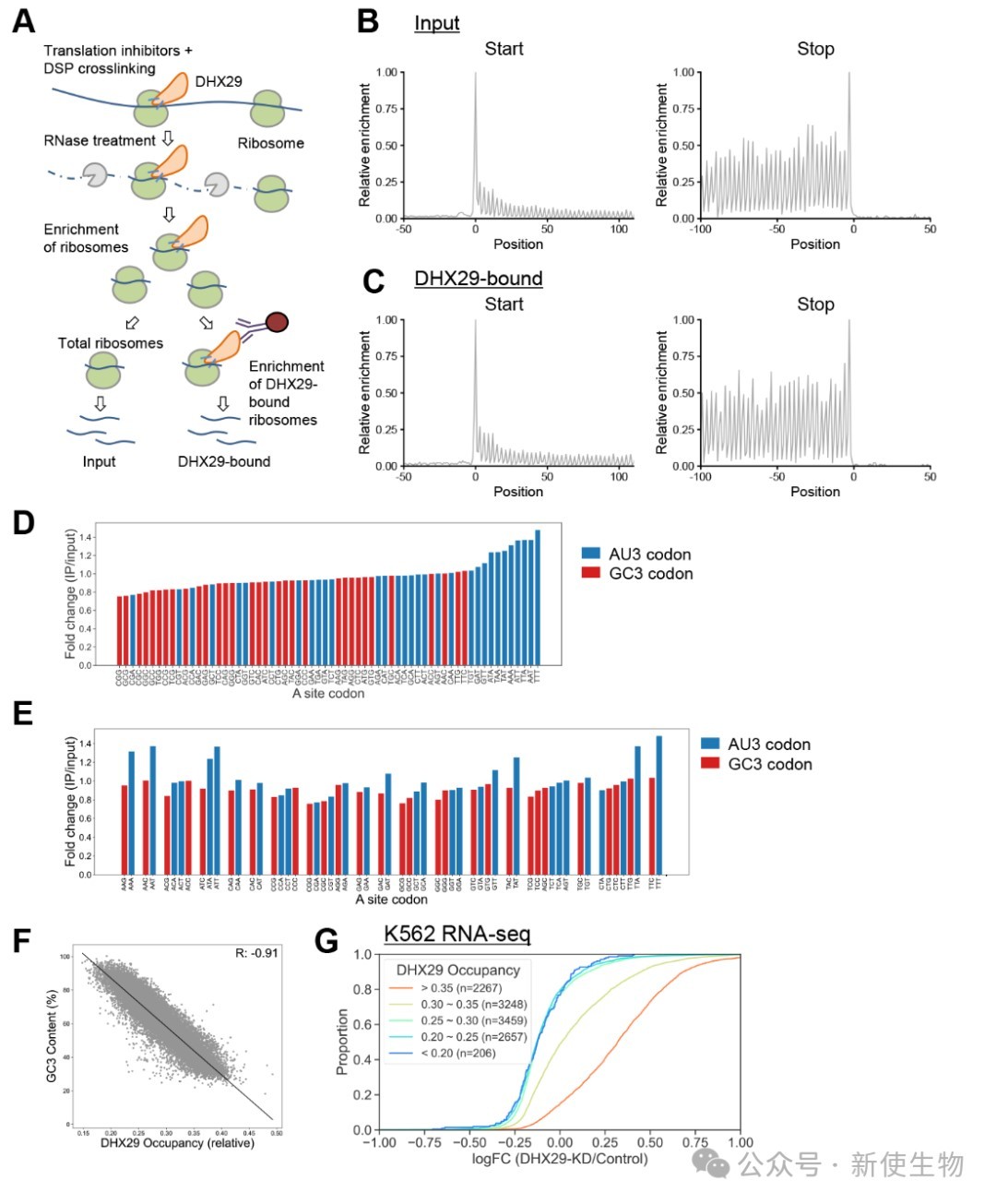
四、DHX29优先结合解码AU3密码子的核糖体
为了探究DHX29的密码子偏好性,研究人员开发了一种选择性Ribo-seq核糖体印迹分析技术,特异性富集与DHX29结合的核糖体。
分析发现,DHX29倾向于结合A位点正在解码AU3密码子(尤其是仅含AU的密码子)的核糖体,并且DHX29在mRNA上的占据率与mRNA的GC3含量呈负相关。
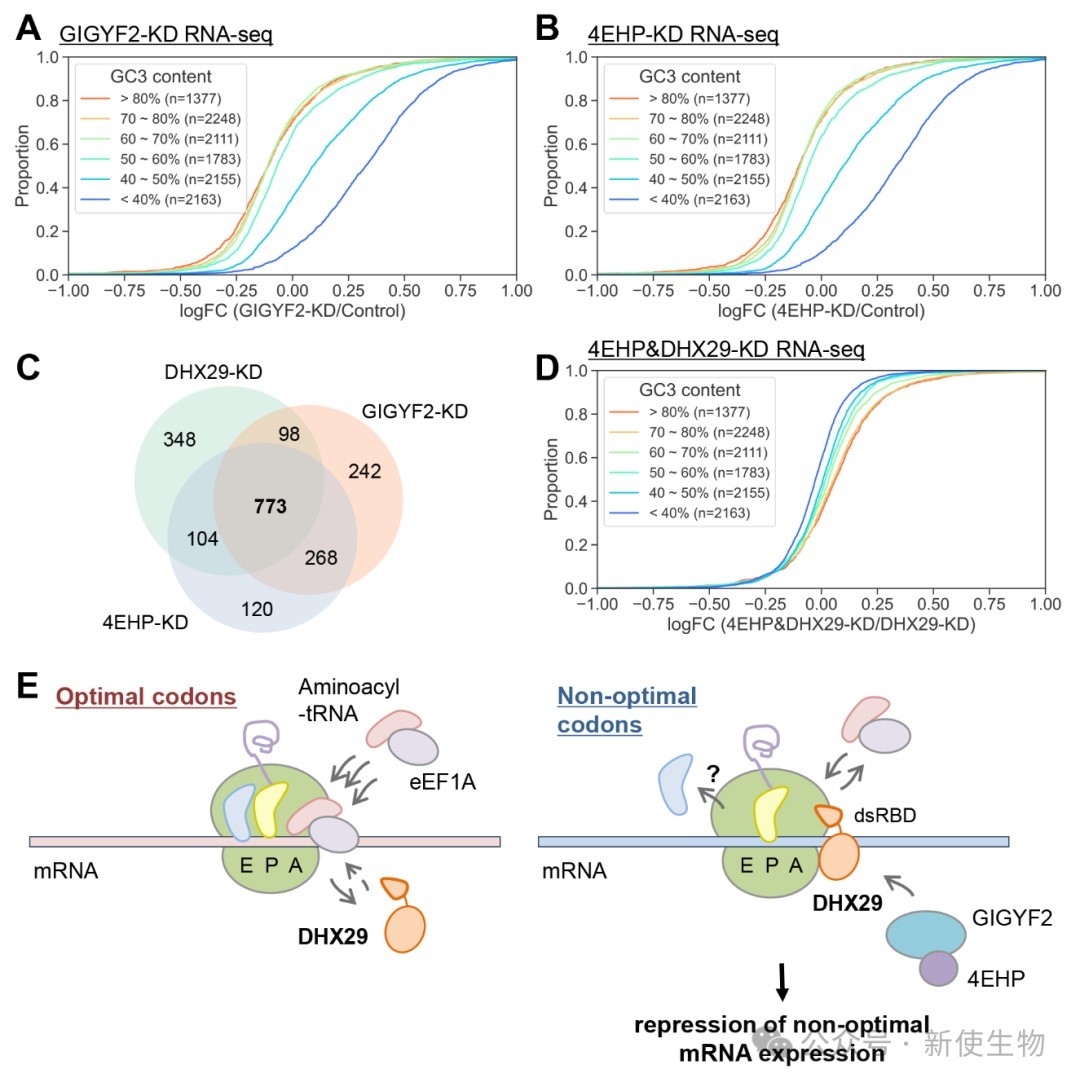
五、DHX29通过招募GIGYF2•4EHP复合体发挥抑制功能
蛋白质互作分析显示DHX29与GIGYF2•4EHP复合体相互作用,该复合体已知参与mRNA抑制。
功能实验表明,敲低GIGYF2或4EHP同样导致非优密码子mRNA上调,其效果与敲低DHX29相似。
此外,在DHX29敲低背景下再敲低4EHP,并未进一步加剧非优mRNA的上调,证明它们在同一条通路上发挥作用。
总结
本研究通过多组学与结构生物学手段,阐明了DHX29作为一种新型翻译延伸调节因子,能够感知核糖体A位点的翻译状态并特异性识别非最优密码子。该研究不仅确立了DHX29在mRNA质量控制中的核心地位,还揭示了其与GIGYF2•4EHP复合物协同作用的分子机制,为相关疾病的治疗提供了潜在靶点。
| 新使生物专业翻译组一站式服务平台 |
| 产品名称 |
我们能够针对微量细胞或组织,如卵母细胞、卵巢、临床穿刺样品等产出高质量翻译组数据结果。
超高的准确性为研究非经典的开放阅读框(ORFs)提供极大便利,提高微肽(肿瘤新生抗原)的挖掘效率。
另外新使生物提供多物种多聚核糖体分析(Polysome profiling),了解更多翻译组技术信息可登录 www.neoribo.com。
点击图片查看
点击图片查看


 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们
