
导读
核糖核酸(RNA)作为一种高分子聚合物,既是遗传信息的载体,也是生命活动中动态的调控者。由于其多样的化学修饰、高度构象灵活性以及明确的分子识别原则,RNA成为功能干预的理想靶点。
近年来,化学生物学的飞速发展极大地扩展了识别和操控RNA分子的方法,这些技术不仅推动了基础研究的深入,也为临床治疗开辟了新途径。
近期,北京大学伊成器团队在SCIENCE CHINA Chemistry上发表了题为“Chemical biology of precise RNA targeting and intervention: advances and perspectives”的综述文章。该文系统总结了当前用于精准RNA靶向的化学与分子工具,涵盖了基于寡核苷酸、小分子、CRISPR和工程化RNA结合蛋白等多种策略。

综述整理
一、RNA精准靶向的生化策略
精准的RNA靶向是所有功能干预的基础。近年来,化学生物学领域涌现出多种高效、特异且适应性强的RNA靶向工具。
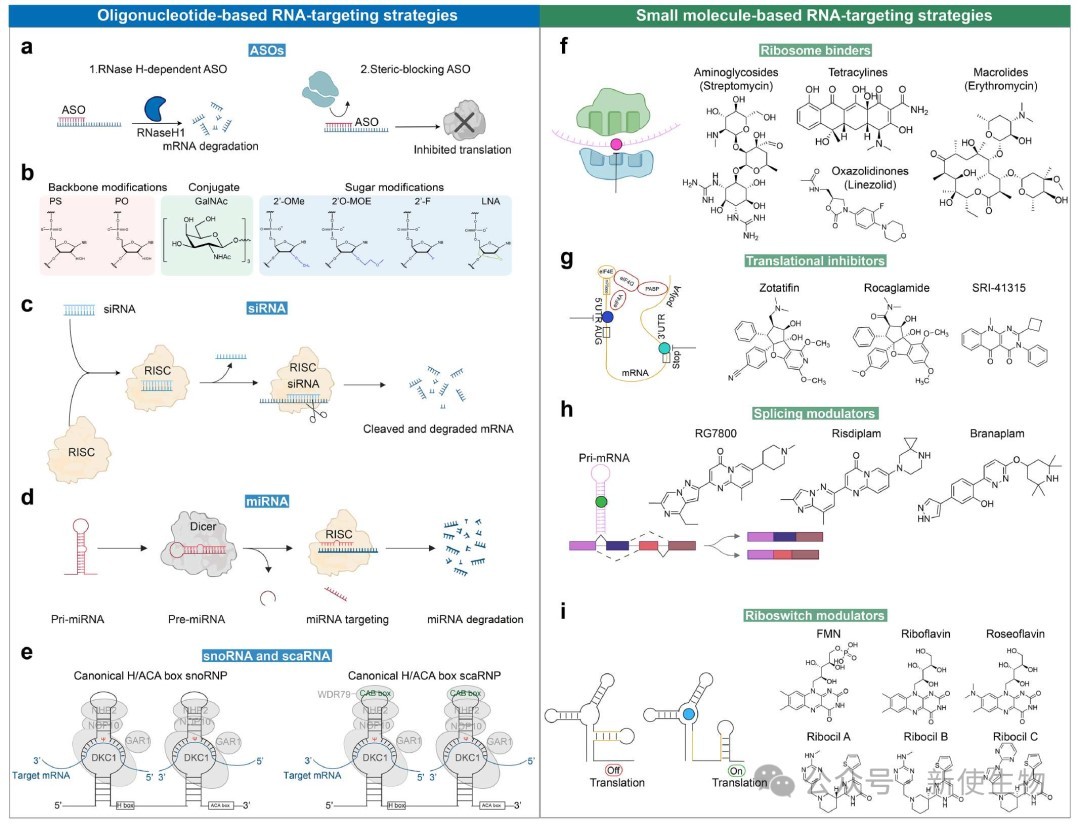
1.1) 基于寡核苷酸的靶向策略
这类策略利用碱基互补配对原则,是最成熟和应用最广泛的RNA靶向方法。
反义寡核苷酸 (ASOs): 短的单链核酸通过与靶标mRNA结合,或招募RNase H降解mRNA,或通过空间位阻调控剪接和翻译。目前已有12款ASO药物获FDA批准,用于治疗遗传性疾病、神经退行性疾病和代谢病等。
小干扰RNA (siRNAs): 短的双链RNA,通过引导RISC复合物切割靶标mRNA,实现高效的基因沉默。已有7款siRNA药物获批,主要通过GalNAc偶联靶向肝脏。
microRNA (miRNAs): 内源性小RNA,通过不完全互补结合靶标mRNA的3' UTR,调控基因表达网络。Antagomirs(抑制剂)和miRNA mimics(模拟物)是主要的治疗策略。
snoRNA/scaRNA: 作为天然的RNA修饰引导模块,工程化的snoRNA/scaRNA可被用于引导内源性酶到特定位点进行修饰(如假尿苷化),或调控剪接。
1.2) 基于小分子的靶向策略
与依赖序列的寡核苷酸不同,小分子通过识别RNA复杂的三维结构(如凸起、环、假结)来发挥作用,具有良好的细胞渗透性和口服给药潜力。
核糖体结合剂: 许多抗生素(如氨基糖苷类、四环素)通过结合细菌rRNA的关键功能位点来抑制蛋白质合成。
翻译抑制剂: 靶向mRNA 5' UTR的结构元件,阻断核糖体扫描,选择性抑制癌基因(如KRAS、MYC)的翻译。
剪接调节剂: 通过稳定或破坏pre-mRNA上的调控结构,改变剪接结果。FDA批准的Risdiplam即为此类药物。
核糖开关调节剂: 模拟天然代谢物,结合细菌mRNA的核糖开关,从而调控基因表达,具有抗菌潜力。
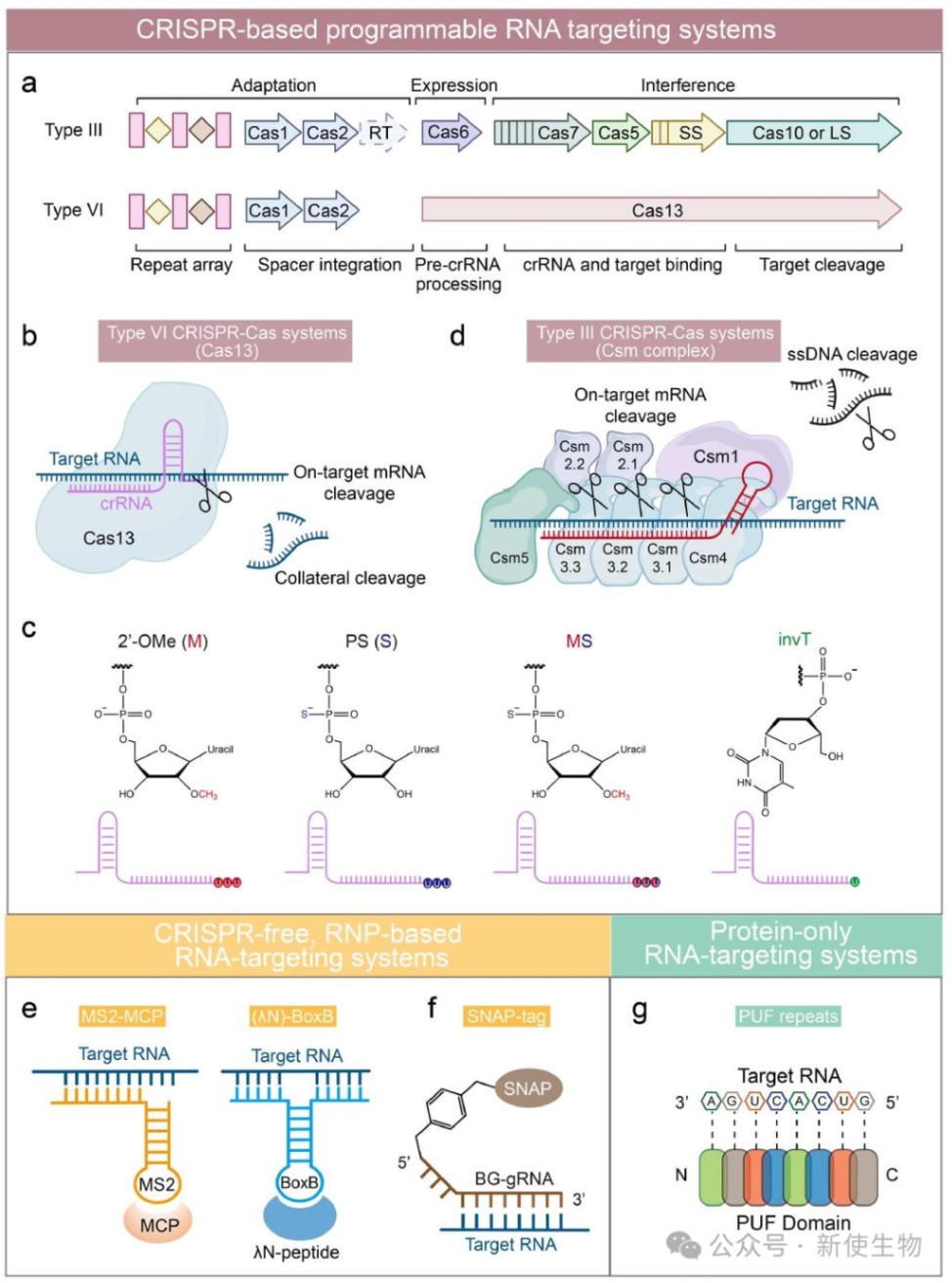
1.3) 基于CRISPR的可编程RNA靶向系统
CRISPR系统被改造后,可实现高度可编程的RNA靶向和功能干预。
VI型CRISPR-Cas13系统: Cas13蛋白在crRNA引导下,特异性结合并切割单链RNA。其多个亚型(如Cas13a, b, d, X, Y)各有特点,其中紧凑的Cas13X/Y更适合病毒载体递送。
III型CRISPR-Cas系统: 如Csm复合物和Cas7-11,通过多亚基复合物识别并切割RNA。与Cas13相比,III型系统通常没有“附带切割”活性,特异性更高、更安全。
1.4) 无CRISPR的、基于RNP的靶向系统
MS2-MCP和λN-BoxB系统: 通过在靶标RNA上插入特定的发夹结构(MBS或BoxB),招募与之结合的蛋白(MCP或λN)及其融合的效应蛋白。
SNAP-tag和HaloTag系统: 利用化学诱导的共价连接,将效应蛋白招募到带有特定化学标签的RNA上。
1.5) 纯蛋白的RNA靶向系统
这类系统完全不依赖gRNA,仅通过蛋白质自身实现序列特异性识别。
PUF蛋白: 由多个重复模块组成,每个模块识别一个RNA碱基。通过组合不同的模块,可设计出能识别特定8-nt序列的蛋白。
PPR蛋白: 主要存在于植物中,具有更长的识别序列(10-20个或更多),尤其适用于靶向线粒体等细胞器内的RNA。
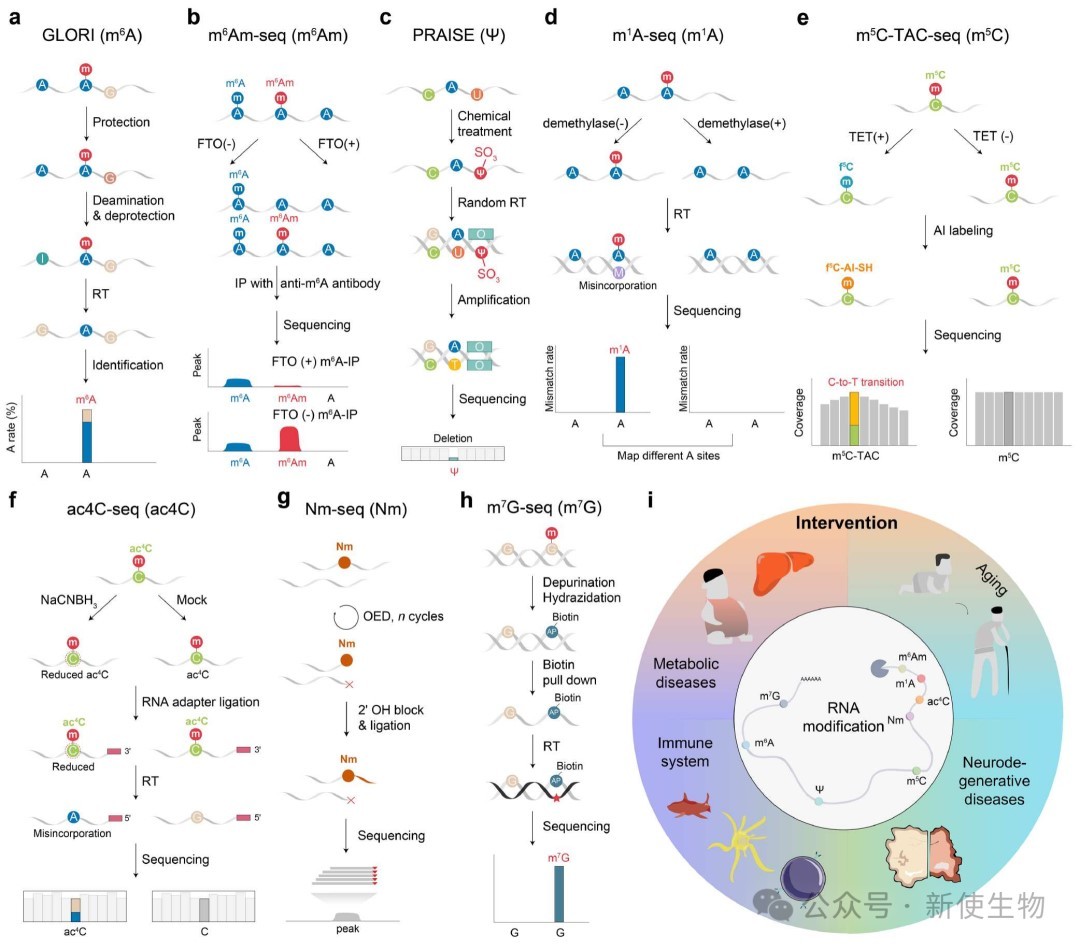
二、RNA功能的化学修饰与干预
在精准靶向的基础上,研究人员开发了多种功能干预技术,实现了在RNA水平上对基因表达的精确调控。
2.1) RNA修饰的干预
RNA修饰(表观转录组)是调控RNA命运的关键,干预其“写入”、“擦除”和“读取”过程,已成为重要的治疗策略。
检测技术: m⁶A-seq、GLORI、DART-seq等高通量测序技术实现了对m⁶A、Ψ、m⁵C等多种修饰的单碱基、定量检测,为精准干预奠定了基础。
干预策略:
i.小分子抑制剂: 针对m⁶A去甲基化酶FTO和ALKBH5或甲基转移酶METTL3的抑制剂,已在AML、胶质母细胞瘤等临床前模型中显示出显著的抗肿瘤效果。
ii. 可编程修饰编辑: 将dCas13与修饰酶(写入器或擦除器)融合,可实现对特定转录本上特定位点的m⁶A、m⁵C等修饰的精准添加或去除。
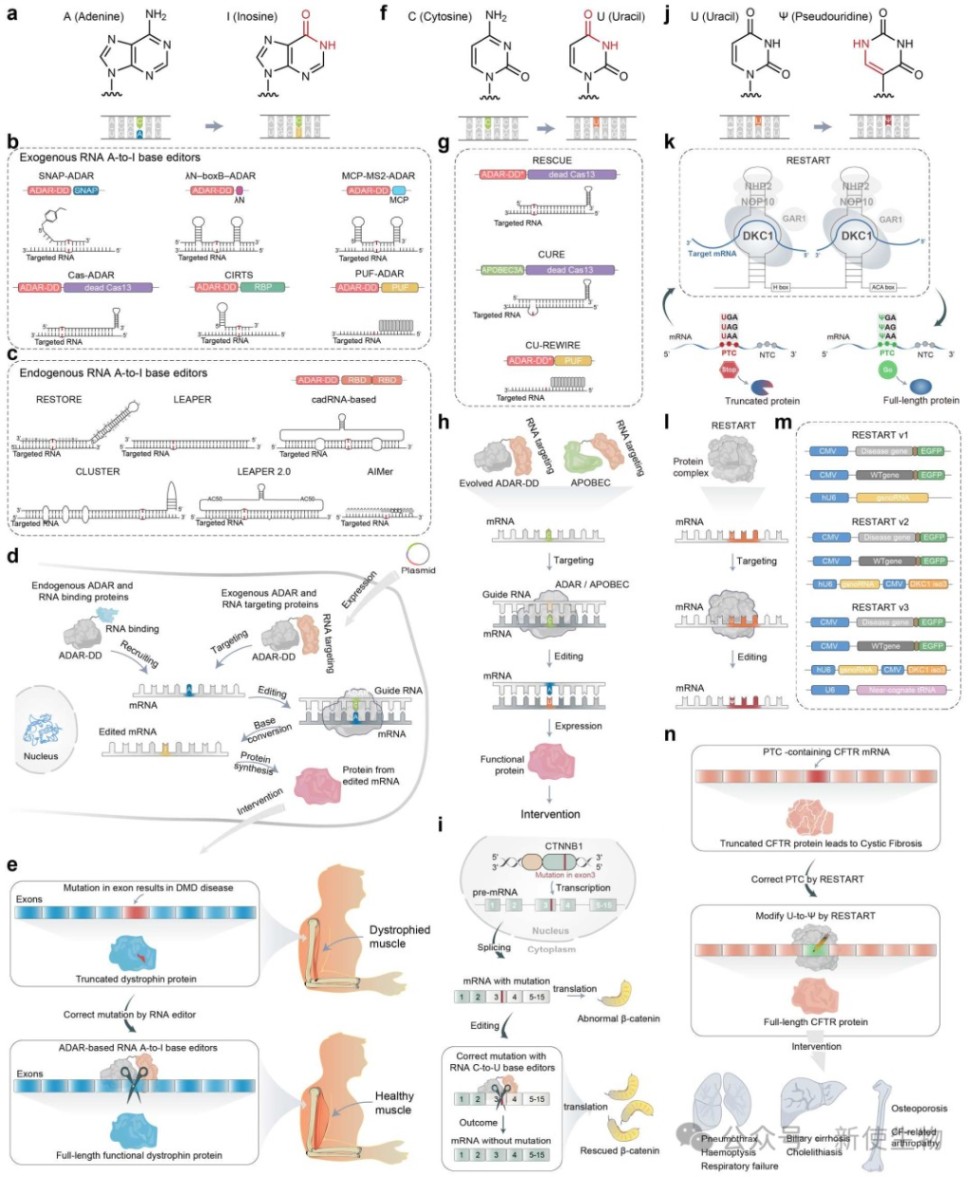
2.2) 基于RNA碱基编辑的功能干预
RNA碱基编辑技术能够在不改变基因组DNA的情况下,对RNA序列进行精确的纠错或改写。
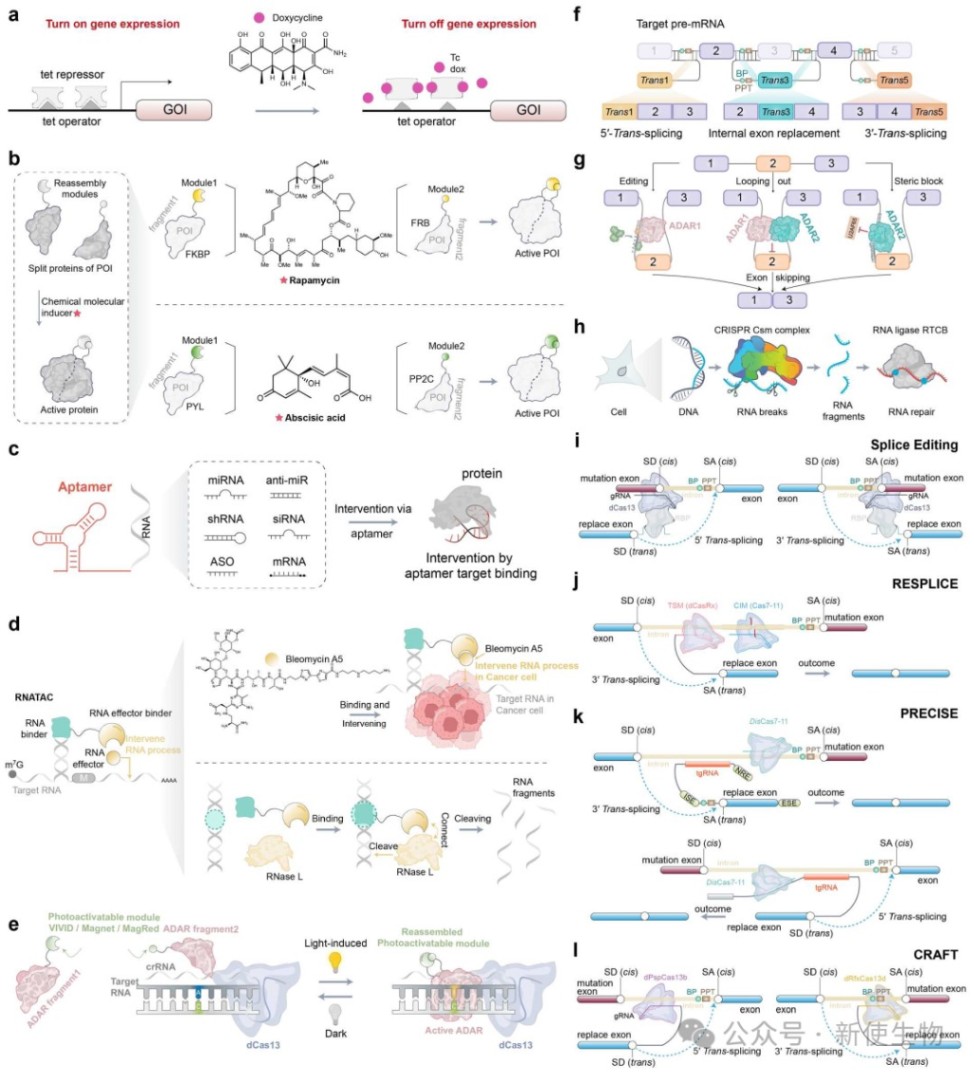
A-to-I编辑: 利用内源或外源的ADAR酶将腺嘌呤(A)编辑为肌苷(I),后者在翻译中被识别为鸟嘌呤(G)。基于dCas13-ADAR融合蛋白的REPAIR系统,以及招募内源ADAR的LEAPER和RESTORE系统,已成功用于在动物模型中纠正杜氏肌营养不良(DMD)和α1-抗胰蛋白酶缺乏症等疾病的致病突变。
C-to-U编辑: 利用dCas13融合APOBEC等胞嘧啶脱氨酶,实现胞嘧啶(C)到尿苷(U)的转换。RESCUE系统已成功用于编辑癌基因CTNNB1。
U-to-Ψ编辑: 利用工程化的snoRNA招募内源性酶,将过早终止密码子(PTC)中的尿苷(U)转换为假尿苷(Ψ),从而抑制翻译终止,实现通读,恢复全长蛋白的合成。RESTART系统已在囊性纤维化等模型中验证了其治疗潜力。
2.3) 长片段RNA的操控
针对长基因或复杂突变,研究者们开发了在RNA水平直接修复或替换缺陷片段的技术。
Splice Editing、RESPLICE和CRAFT等系统利用dCas13引导一个外部提供的修复模板,通过反式剪接将错误的外显子替换掉。
2.4) 化学诱导与光激活的RNA碱基编辑
为实现对RNA干预时空的精准控制,开发了多种诱导系统。
化学诱导: 利用四环素或雷帕霉素等小分子,控制编辑工具的表达或通过诱导蛋白二聚化来激活其功能。
光激活: 利用光敏保护基团锁住引导RNA或编辑酶的活性,通过特定波长的光照实现定点、定时的解锁和激活,提供了无与伦比的时空分辨率。
总结与展望
RNA靶向与干预的化学生物学领域正在以前所未有的速度发展。从ASO、siRNA的临床成功,到CRISPR-Cas13、RNA碱基编辑器的强大功能,再到化学诱导系统的精妙控制,我们已经拥有了日益丰富的工具箱来精确调控RNA。当前的主要挑战仍在于递送效率和脱靶效应,高效、组织特异性的递送系统是所有RNA疗法成功的基石。
未来的发展方向将集中于:1) 开发更安全、高效的递送载体(如新型LNP、工程化AAV);2) 利用AI和深度学习优化工具设计,提高靶向特异性;3) 整合合成生物学,构建能够响应内源性疾病信号的“智能”RNA干预系统。通过融合化学生物学、分子工程和人工智能,RNA靶向干预技术正从基础研究工具走向临床现实,有望为癌症、遗传病和神经退行性疾病等多种顽疾提供革命性的治疗方案。
| 新使生物专业翻译组一站式服务平台 |
| 产品名称 |
点击图片查看
点击图片查看


 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们
