
导读
真核生物的核糖体RNA(rRNA)上存在着位点特异性的2'-O-甲基化(Nm)修饰,这种修饰主要富集在核糖体的关键功能域。与原核生物相比,真核生物rRNA上的Nm修饰数量要多得多,这暗示了其在核糖体功能进化中的重要性。
已有研究表明,这些修饰的缺失会损害细胞生长,降低翻译的效率和保真性,并改变对抗生素的敏感性。Nm修饰位点在多种人类癌细胞中的高度保守性也凸显了其广泛的生物学功能。
这些修饰由C/D框小核仁核糖核蛋白复合物(snoRNPs)催化形成,其中核心蛋白Nop1是关键的甲基转移酶。尽管已知Nm修饰参与核糖体生物合成和功能调控,但其如何通过影响rRNA折叠、动态变化和分子相互作用来发挥作用的具体结构与分子机制仍有待阐明。
2026年4月3日,美国范安德尔研究所Hong Li团队在Molecular Cell上发表了一篇题为“2'-O-Methylation maintains ribosome structural and translation integrity”的论文。该研究通过对rRNA 2'-O-甲基化缺失的酵母核糖体进行高分辨率结构和功能分析,发现该修饰对于维持翻译的效率和保真性至关重要。

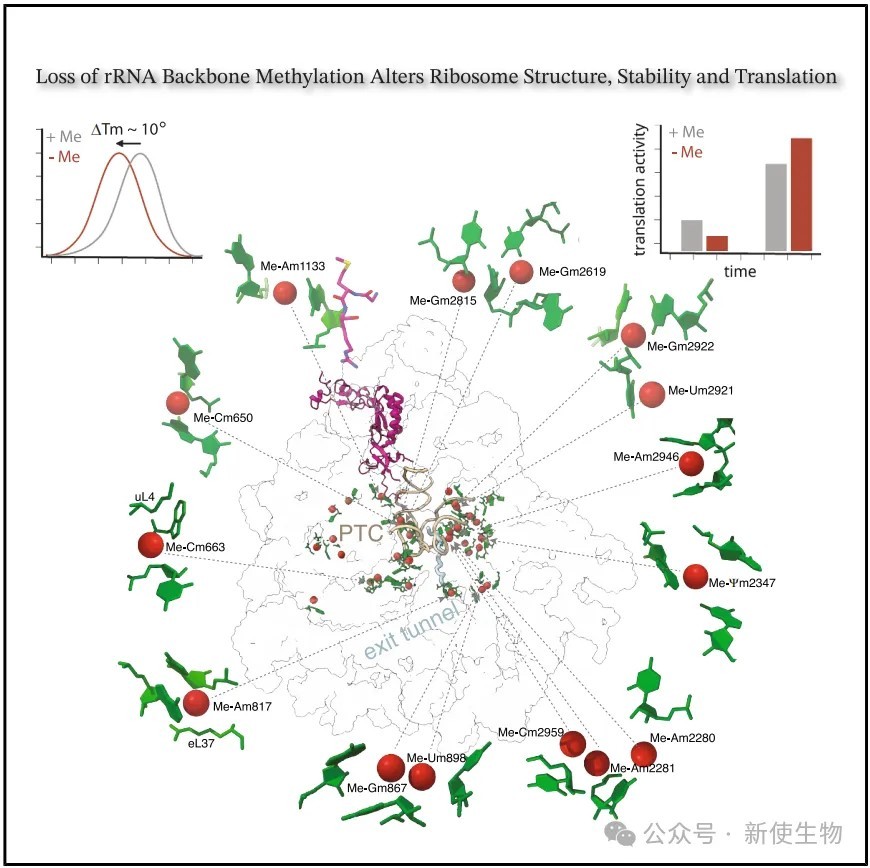
研究结果
一、F2细胞中Nm修饰缺失,并导致翻译活性与保真性受损
通过RiboMethSeq技术证实,表达突变Nop1蛋白的F2酵母细胞中,snoRNA指导的rRNA 2'-O-甲基化几乎完全丧失。
细胞水平的翻译活性检测表明,F2细胞的整体蛋白质合成速率降低,但翻译过程中的移码错误和对非标准起始密码子的识别率却显著增加,表明其翻译保真性下降。
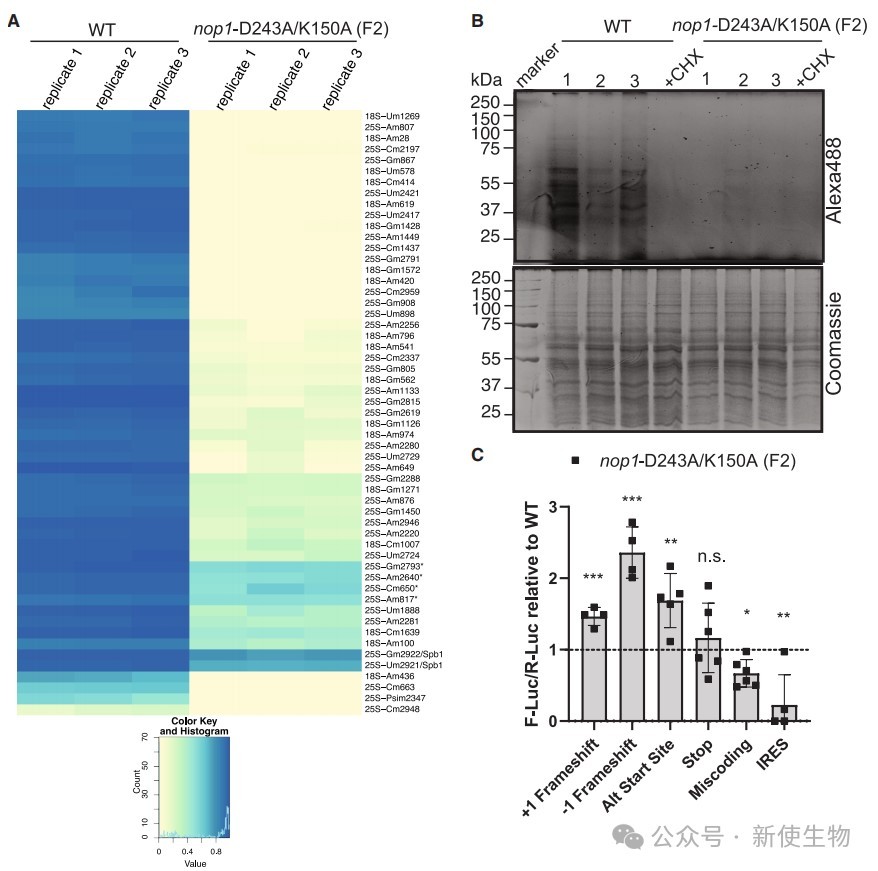
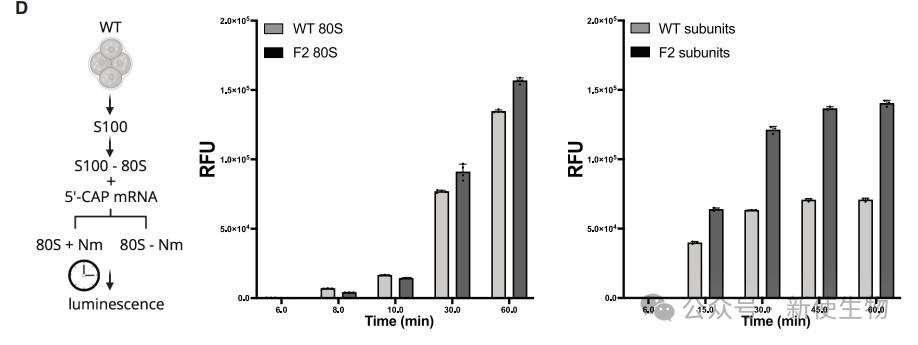
二、Nm修饰维持核糖体的结构完整性与热稳定性
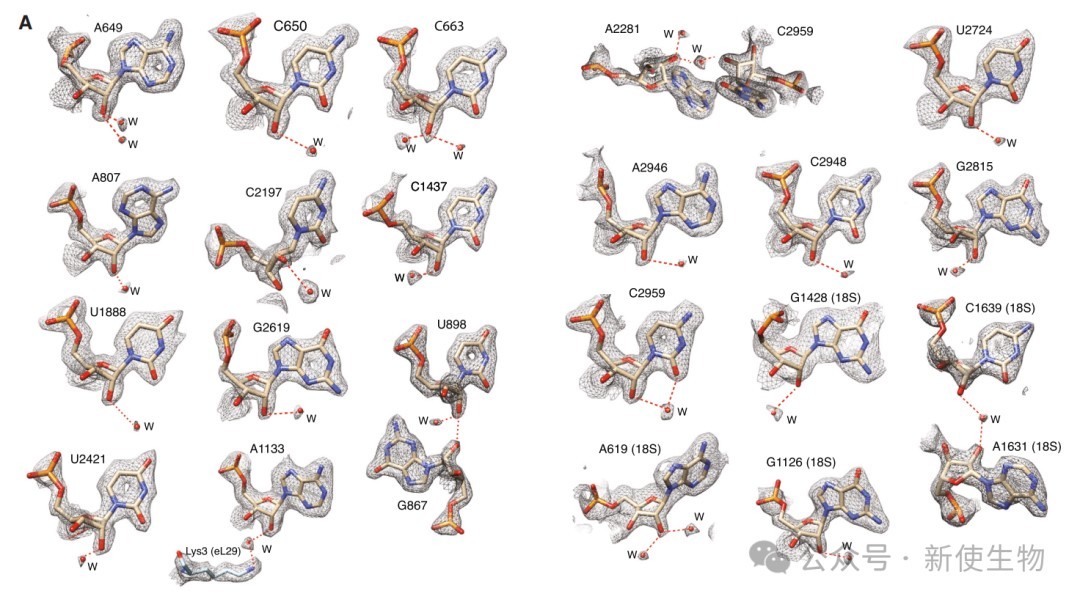
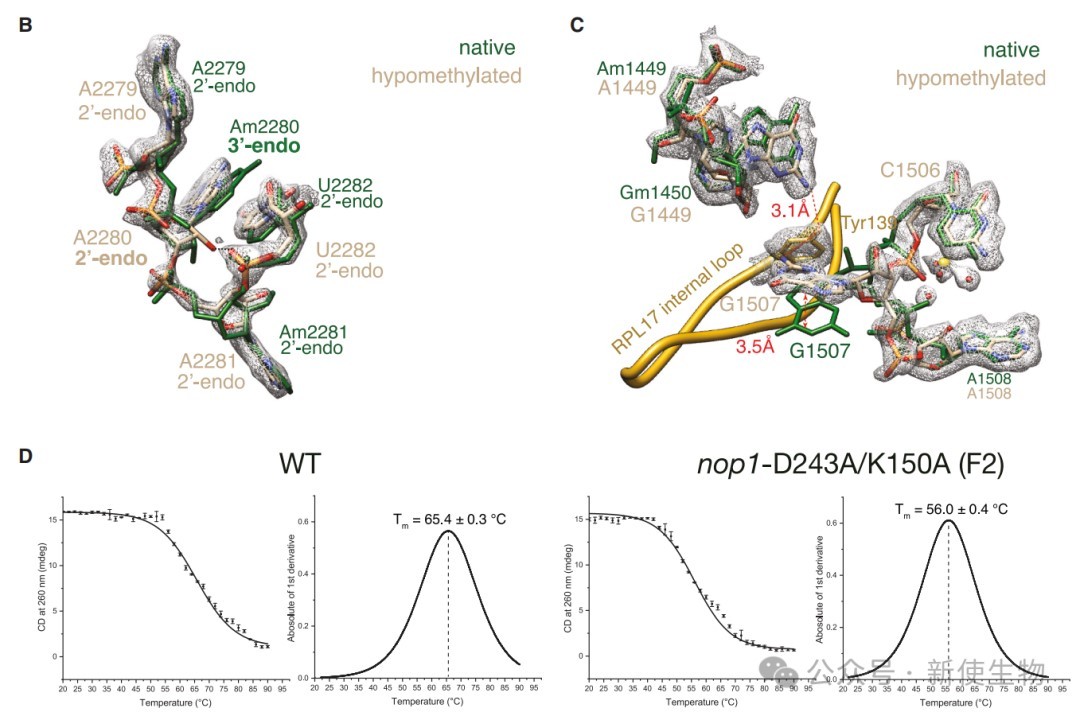
利用冷冻电镜(cryo-EM)技术解析了低甲基化核糖体的高分辨率结构,发现甲基基团的缺失导致其周围形成新的有序水分子网络,并引起rRNA骨架上关键位点(如A2280)的糖环构象从C3'-endo转变为C2'-endo。
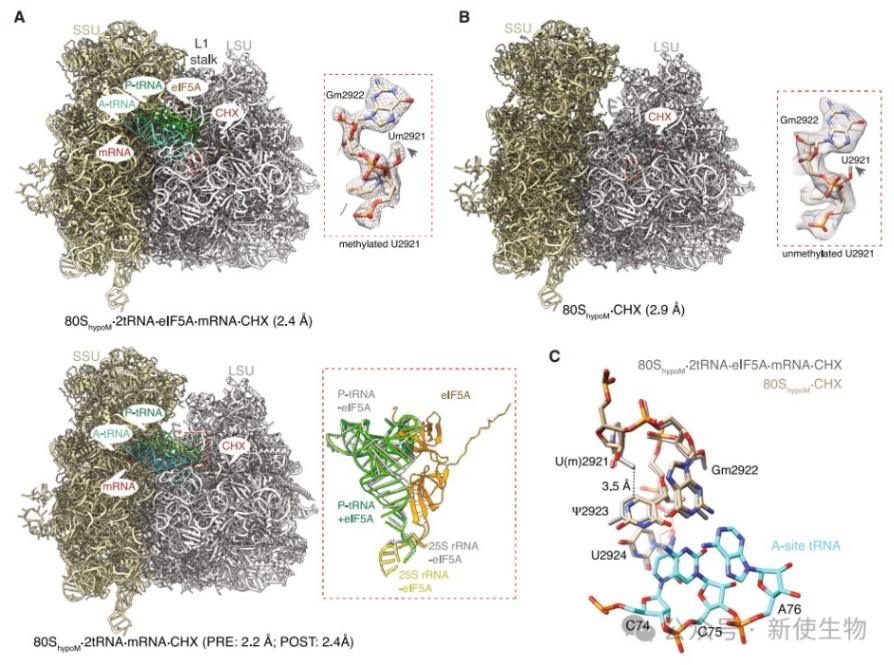
圆二色谱(CD)热变性实验进一步证明,与野生型相比,低甲基化核糖体的热稳定性显著降低,熔解温度(Tm)下降了约10℃。
三、Nm修饰优化多肽链输出通道并影响亚基动态
结构分析显示,多肽链输出通道内A1449和G1450位点串联甲基化的缺失,引起了该区域rRNA和核糖体蛋白RPL17(uL22)的显著结构重排。
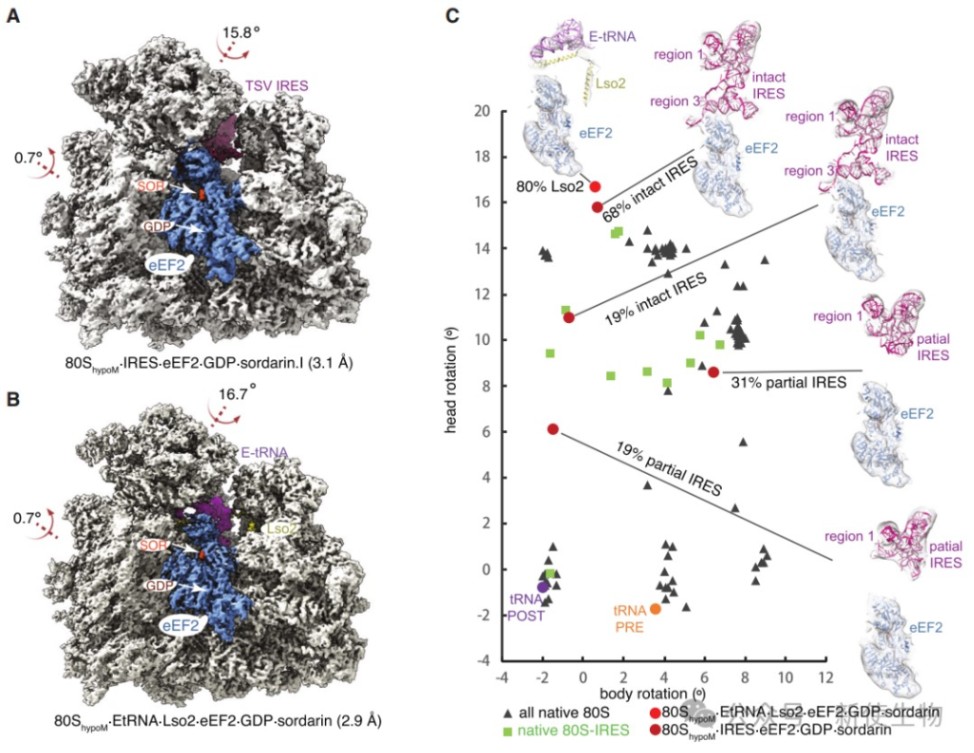
在研究IRES介导的翻译起始过程中,冷冻电镜重构发现低甲基化核糖体倾向于锁定在一种非典型的超旋转构象,这表明Nm修饰的缺失改变了核糖体大小亚基的相对运动动态。
四、Nm修饰缺失选择性地影响核糖体蛋白的翻译
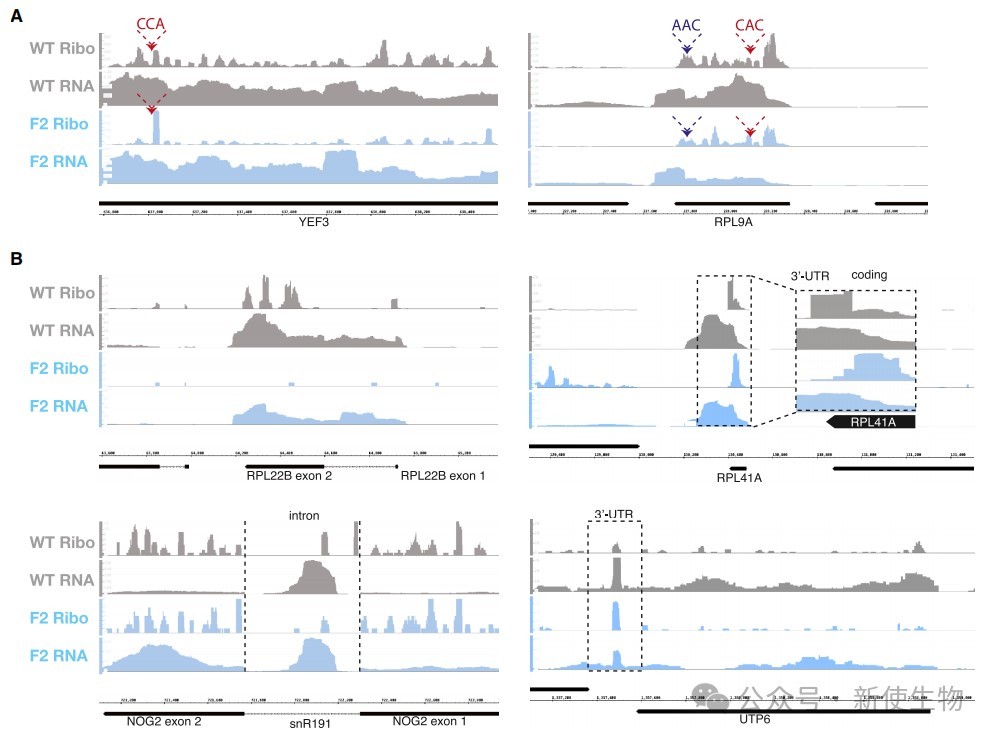
通过Ribo-seq核糖体印迹分析结合RNA测序分析,作者发现Nm修饰的缺失不成比例地降低了编码核糖体蛋白的mRNA的翻译效率。
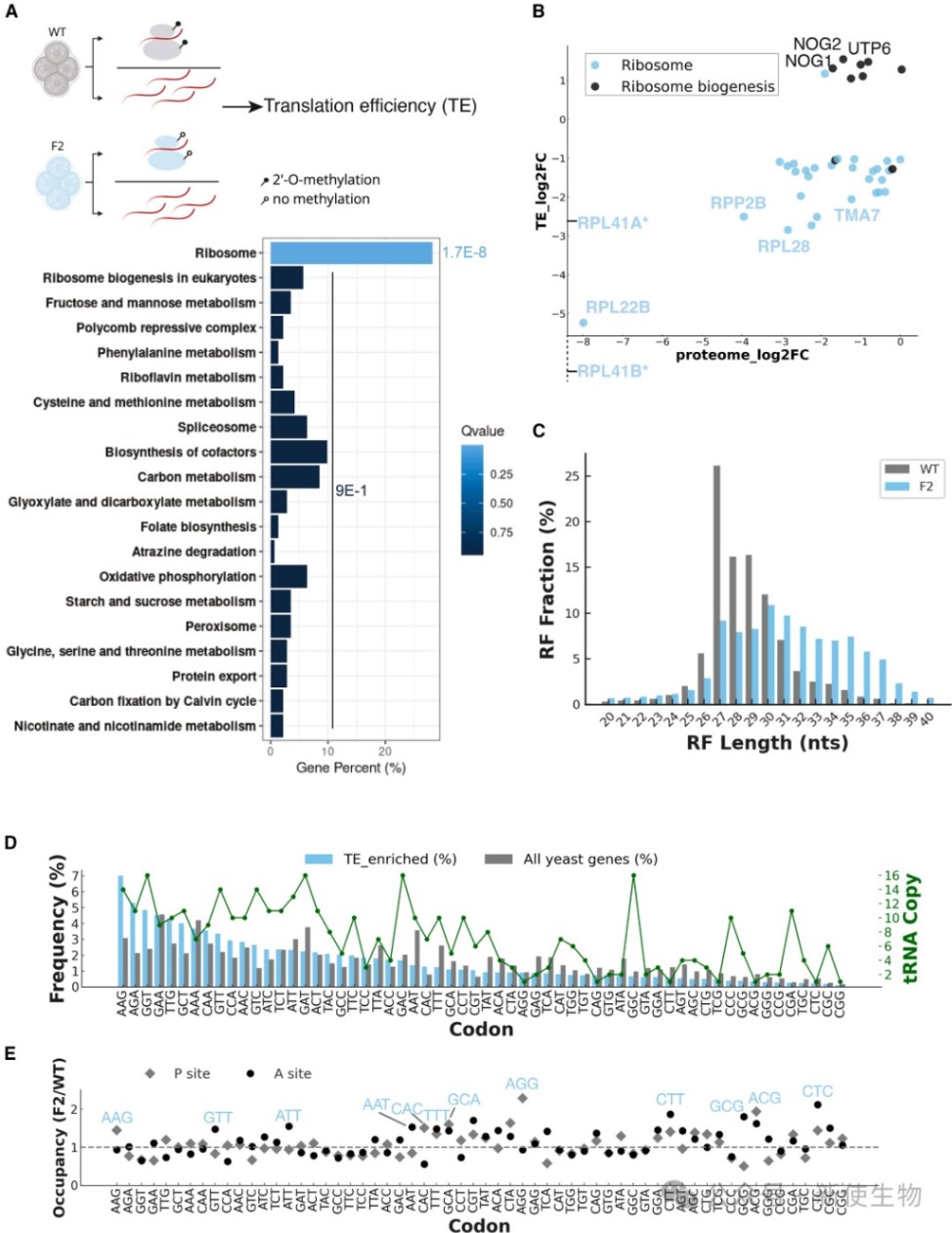
进一步分析表明,这种选择性调控与低甲基化核糖体对特定密码子的敏感性改变、翻译暂停模式的差异以及对mRNA编码区和5' UTR或3' UTR区域结构识别能力的改变有关。
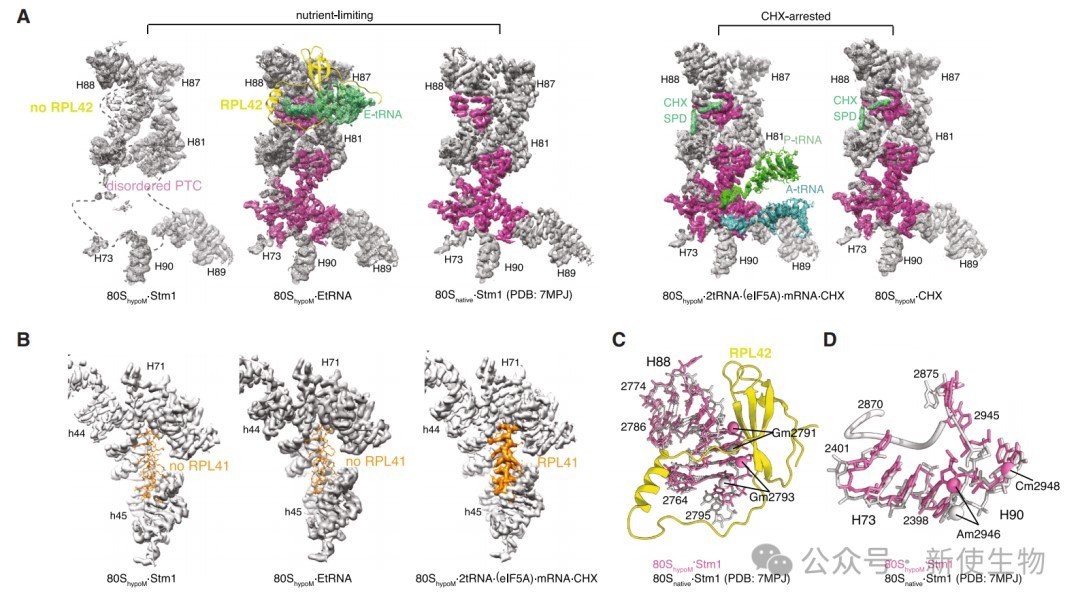
五、低甲基化在细胞应激下损害肽基转移酶中心(PTC)的形成和蛋白质组装
在营养限制等应激条件下,对低甲基化核糖体的结构分析发现,其肽基转移酶中心(PTC)的RNA折叠出现缺陷,并且缺失了关键的核糖体蛋白RPL42(eL42)和RPL41。
这表明在应激状态下,2'-O-甲基化的缺失会加剧核糖体组装的缺陷,尤其影响核心功能区域的稳定性。
总结
本研究综合运用结构生物学、翻译组学和蛋白质组学等前沿技术,系统地揭示了rRNA 2'-O-甲基化是微调核糖体功能的关键机制。该修饰通过稳定核糖体的高分辨率三维结构、维持其周围的溶剂网络和调控其构象动态,进而确保翻译过程的高保真性和高效率,并选择性地调控核糖体蛋白等关键基因的表达,最终对维持细胞稳态和应激响应能力至关重要。
| 新使生物专业翻译组一站式服务平台 |
| 产品名称 |
点击图片查看
点击图片查看


 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们
