
导读
核酸的完整性是所有生命过程的基础。然而,细胞不断暴露于损伤DNA和RNA的内外源性物质中。
尽管RNA损伤不像DNA损伤那样会导致遗传信息的永久性改变,但它具有强烈的细胞毒性并能引发复杂的应激反应。当延伸中的核糖体在mRNA的损伤位点停滞并相互碰撞时,多种应激反应和质量控制途径就会被激活。
例如,核糖体碰撞会激活整合应激反应(ISR)和核糖体毒性应激反应(RSR)。然而,在特定情况下,细胞如何限制这些可能致命的RNA损伤应答的激活,目前仍知之甚少。
2026年4月2日,慕尼黑大学Julian Stingele团队与英国剑桥大学Stephen P. Jackson团队合作,在Molecular Cell上发表了一篇题为“RNF25 confers mRNA damage tolerance by curbing activation of the integrated stress response”的论文。该研究发现化疗药物阿扎胞苷的细胞毒性主要通过其掺入mRNA引发,这会触发有害的整合应激反应(ISR)。

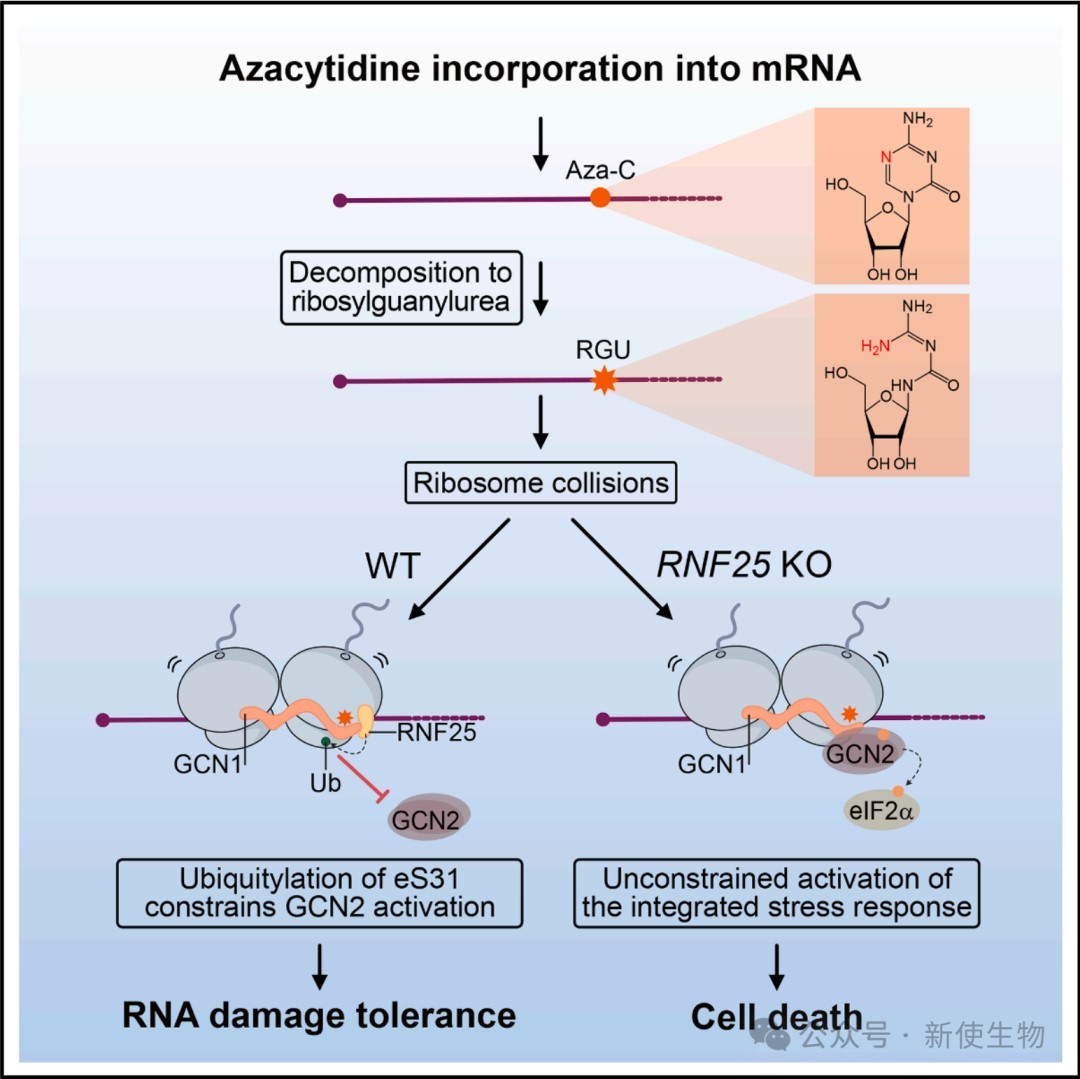
文章索引
【标题】RNF25 confers mRNA damage tolerance by curbing activation of the integrated stress response
【发表期刊】Molecular Cell
【发表日期】2026年4月2日
【作者及团队】慕尼黑大学Julian Stingele团队和剑桥大学Stephen P. Jackson团队等
【IF】16.6
研究结果
一、核糖体关联泛素连接酶提供对阿扎胞苷的抗性
通过CRISPR筛选,研究发现泛素连接酶RNF25和ZNF598的缺失使细胞对阿扎胞苷(aza-C)而非地西他滨(aza-dC)的敏感性增加。
进一步研究表明,RNF25通过其RING结构域和RWD结构域,在GCN1的辅助下泛素化核糖体蛋白eS31的K113位点,从而赋予细胞对aza-C的耐药性。
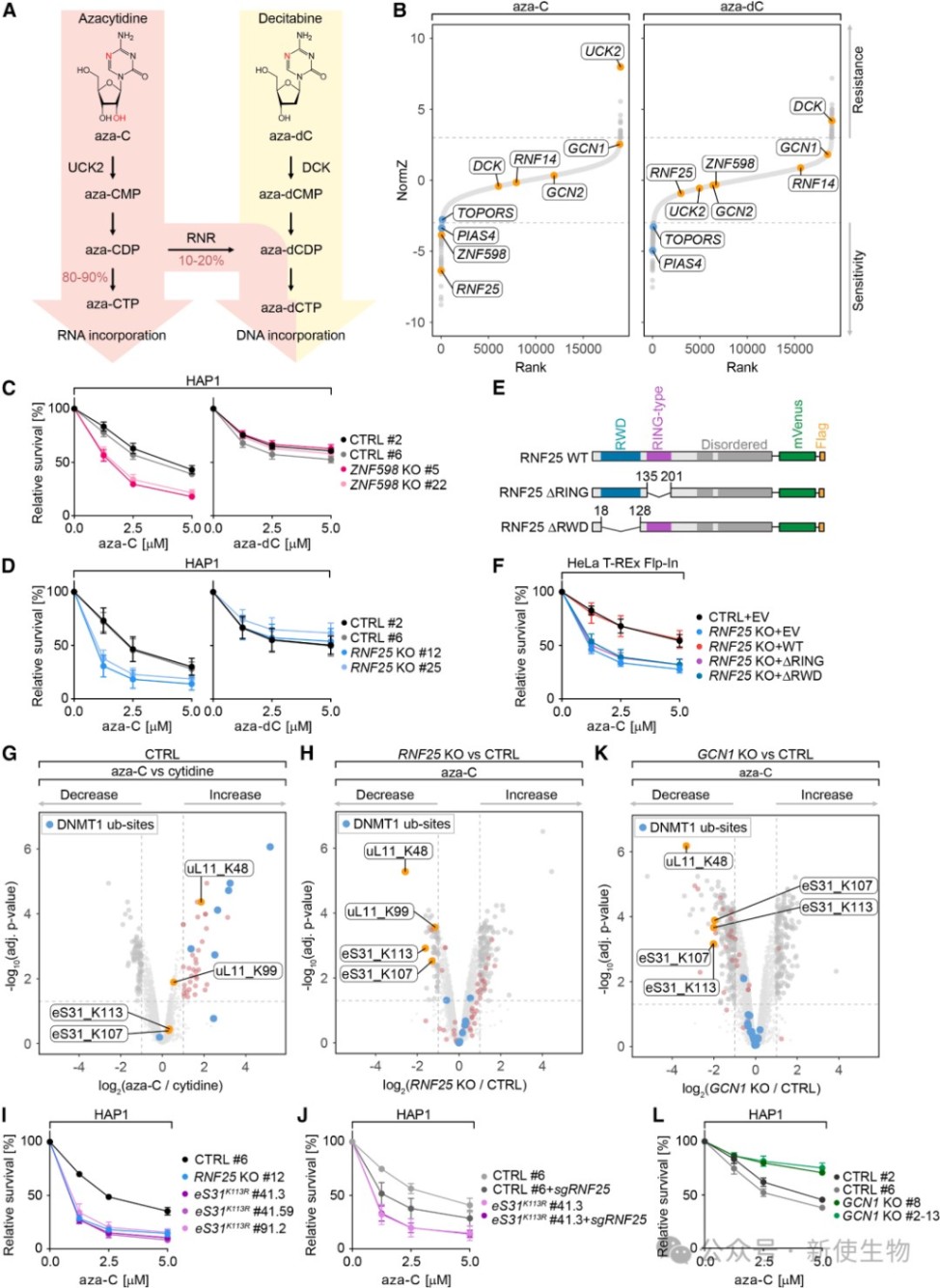
二、CRISPR筛选区分急性和慢性阿扎胞苷毒性响应
通过在野生型、RNF25敲除和ZNF598敲除细胞中进行急性和慢性aza-C处理的CRISPR筛选,发现RNF25和ZNF598通过不同但互补的机制提供耐药性。
此外,GCN1或GCN2的缺失能够完全抑制RNF25或ZNF598敲除细胞对aza-C的超敏性,表明aza-C的细胞毒性由GCN1/GCN2依赖的整合应激反应(ISR)介导。
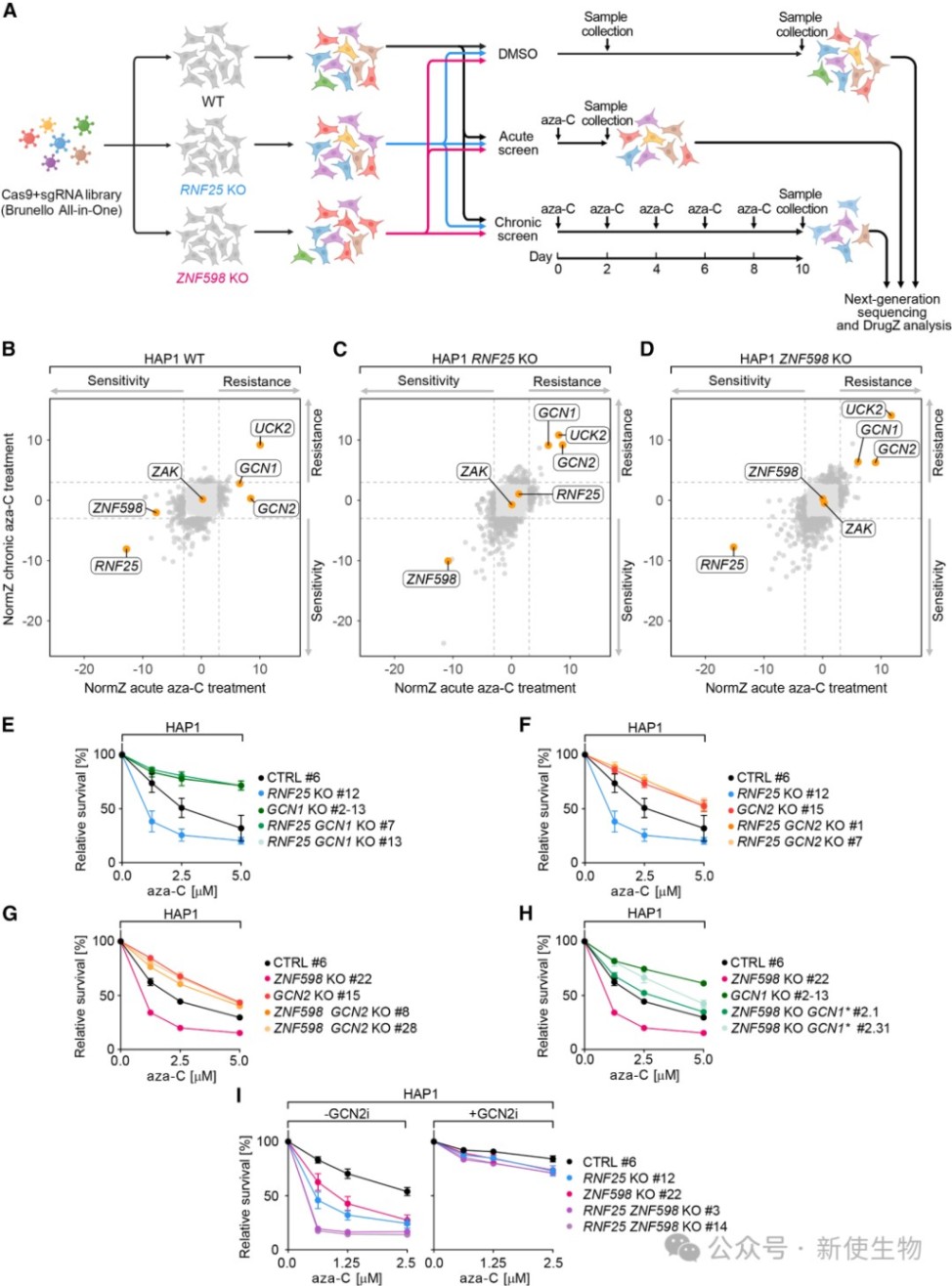
三、阿扎胞苷诱导整合应激响应激活
研究通过磷酸化蛋白质组学和Western blot证实,aza-C能够激活GCN2激酶并磷酸化其下游的eIF2α,这在多种细胞系和原代AML患者细胞中都得到了验证。
通过Polysome profiling多聚核糖体分析和嘌呤霉素掺入实验,研究发现aza-C会诱导GCN2依赖性的翻译抑制,并且在抑制GCN2后能观察到核糖体碰撞的迹象。
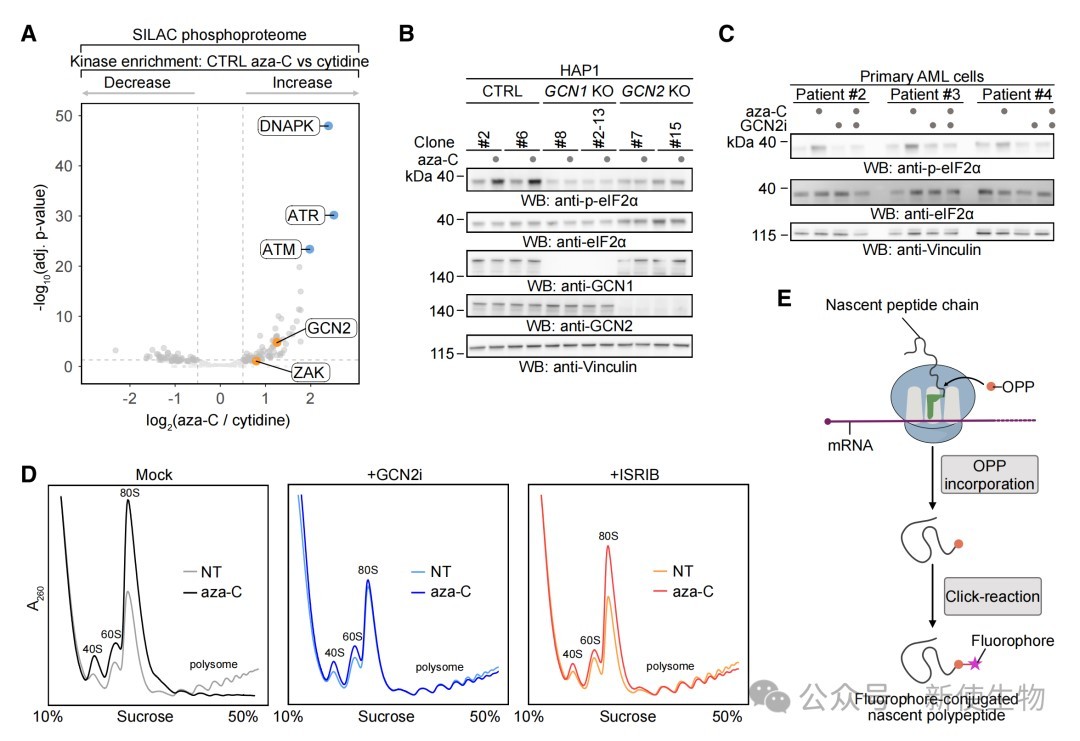
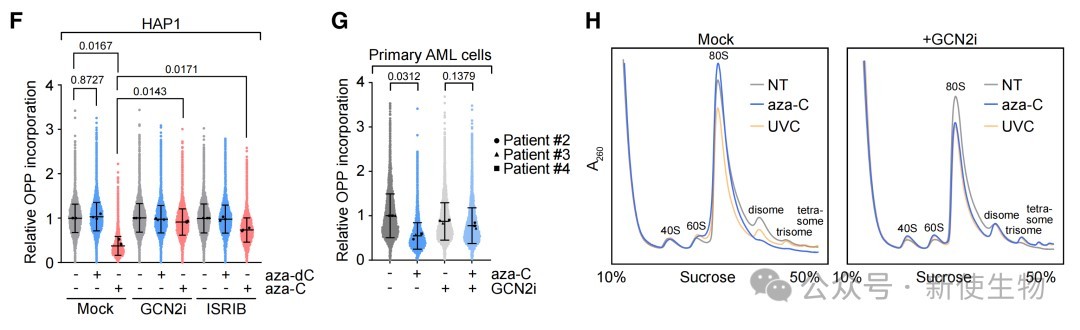
四、RNF25抑制整合应激响应的过度激活
在RNF25缺失或eS31 K113R突变的细胞中,aza-C诱导的翻译抑制和ISR下游基因(如ATF3、CHOP)的表达均显著增强。
这种增强的ISR激活依赖于GCN1和GCN2,表明RNF25的功能是遏制GCN2依赖的ISR,防止其在RNA损伤后被过度激活。
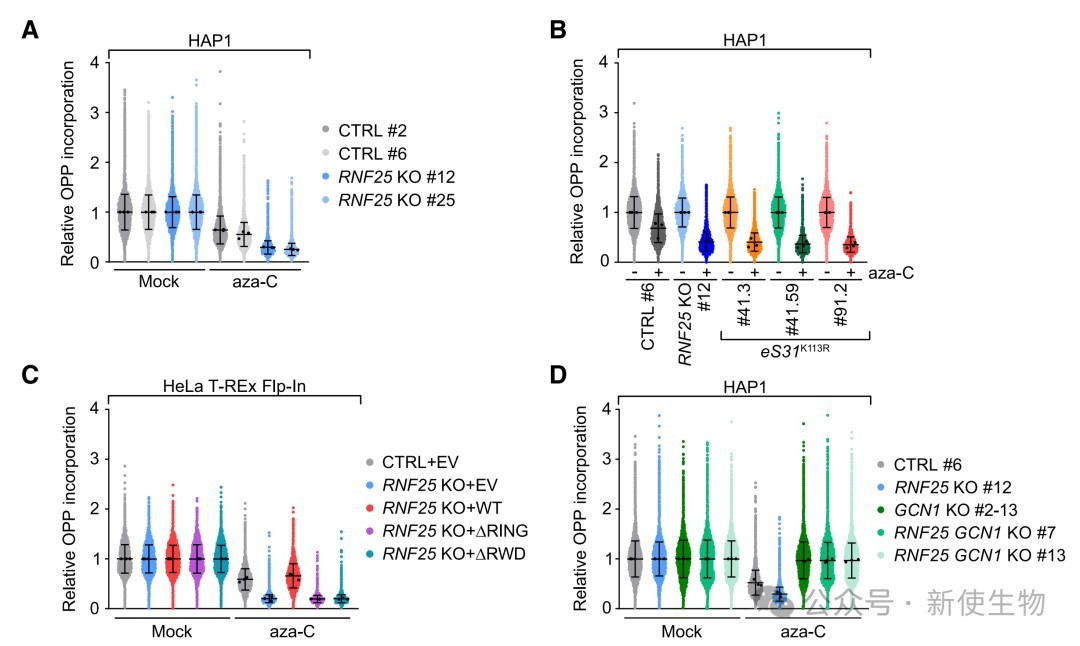
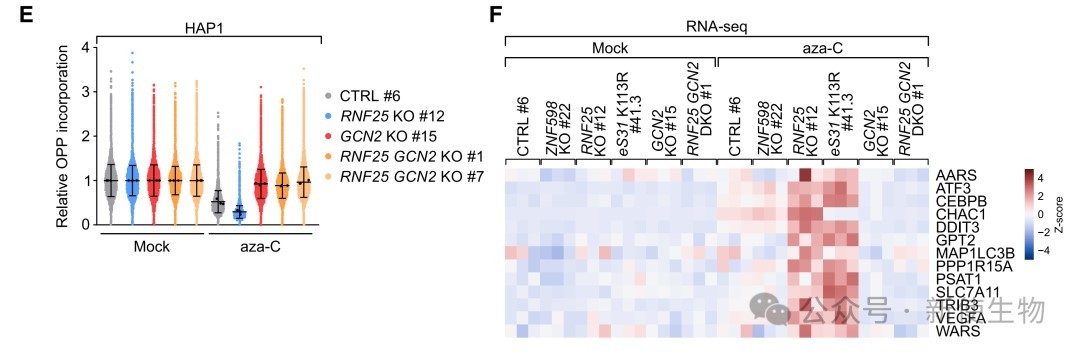
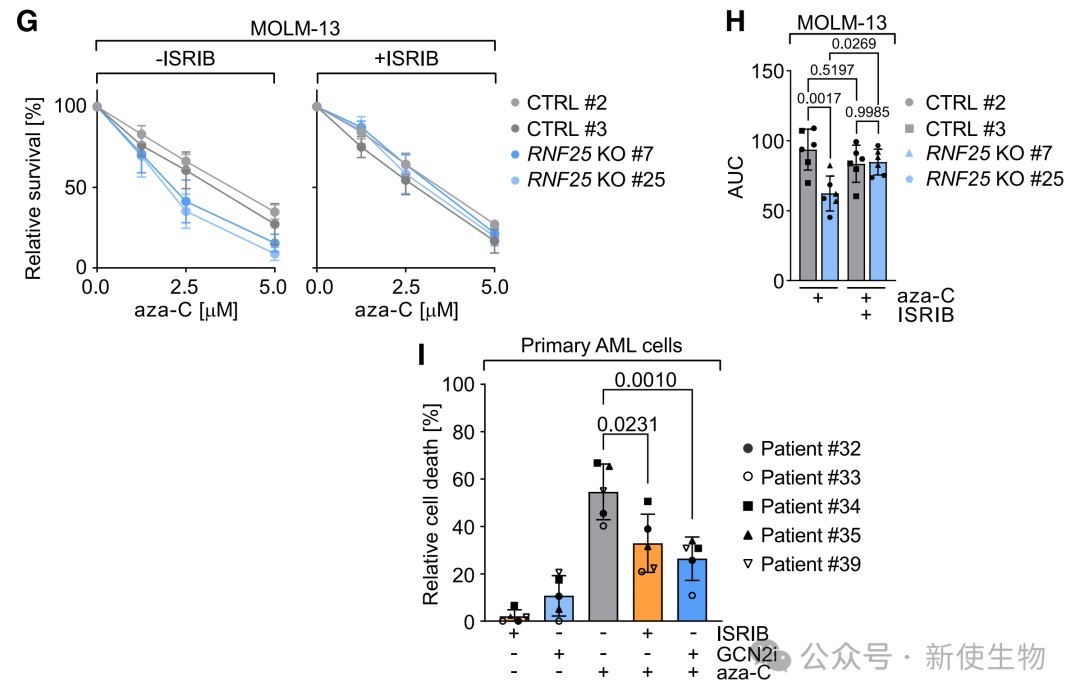
五、ISR调节AML细胞对阿扎胞苷的化疗敏感性
通过使用ISR抑制剂ISRIB或GCN2抑制剂,研究发现抑制ISR能够显著降低aza-C对HAP1细胞、多种AML细胞系以及原代AML患者细胞的细胞毒性。
这一结果表明,aza-C诱导的ISR是其抗肿瘤疗效的重要组成部分,尤其是在RNF25功能缺失的情况下。
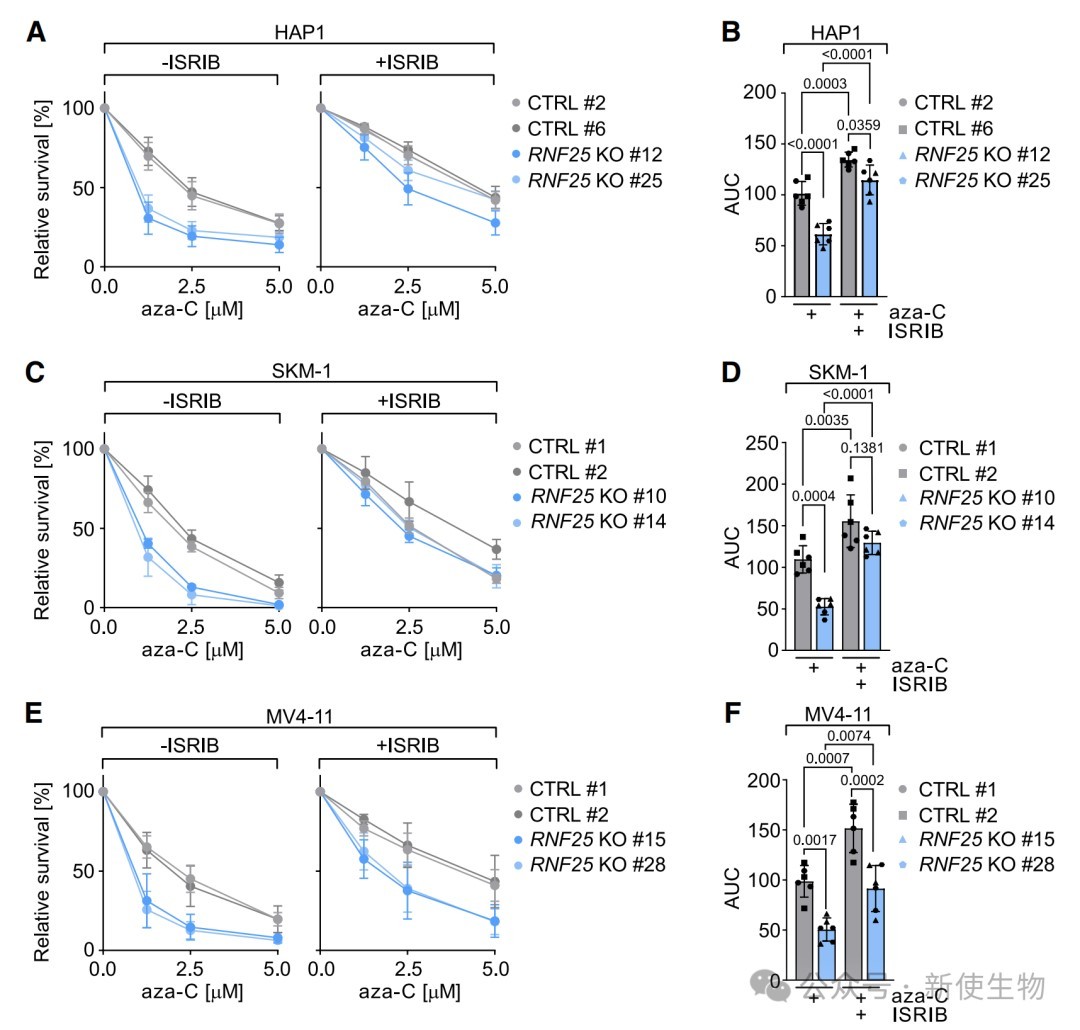
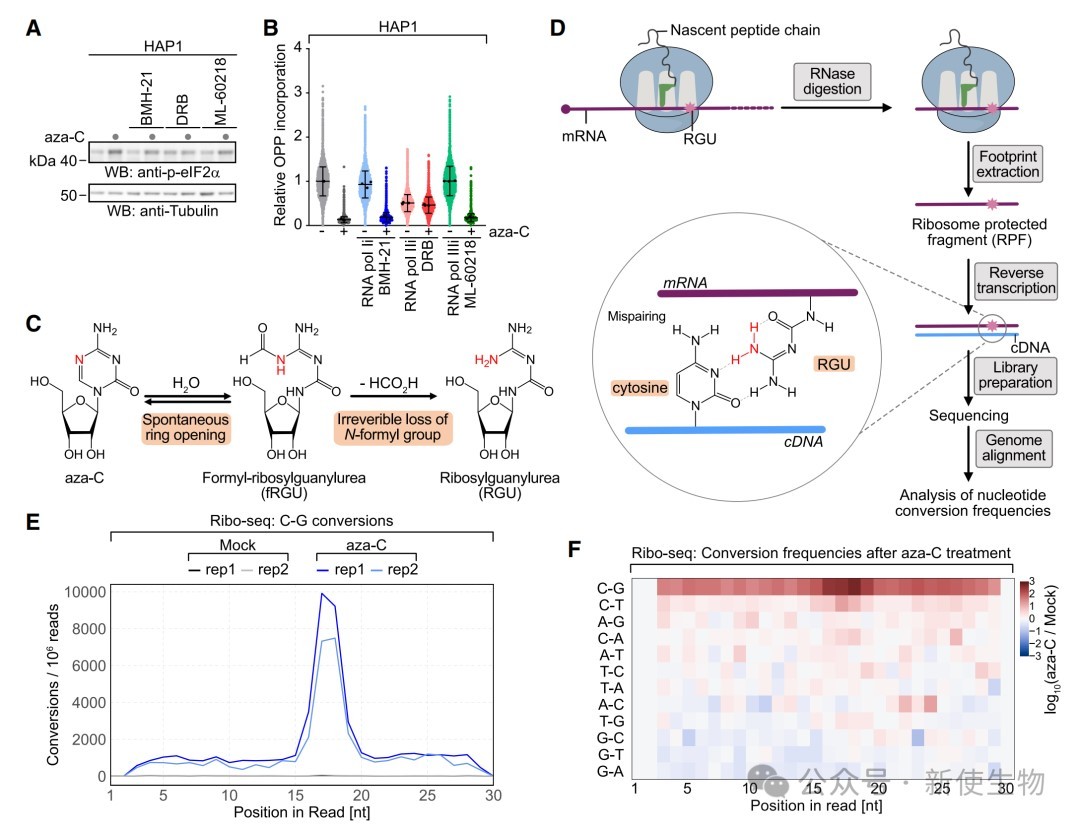
六、阿扎胞苷诱导的mRNA损伤阻碍核糖体延伸
通过使用特异性RNA聚合酶抑制剂,研究证明aza-C需要被RNA聚合酶II掺入到mRNA中才能激活ISR。
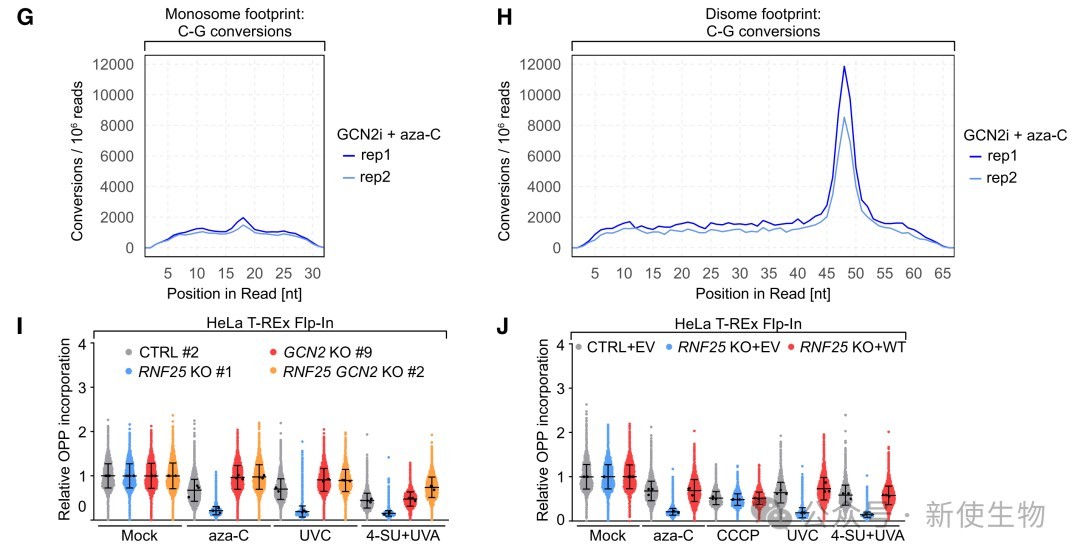
Ribo-seq核糖体印迹分析结果显示,在aza-C处理后,核糖体足迹内出现了显著的C到G的转换,这表明掺入mRNA的aza-C可能分解为RGU(核糖基胍基脲),这种损伤在核糖体A位点处导致翻译停滞和碰撞。
总结
本研究揭示了化疗药物阿扎胞苷的一种新作用机制,即通过其在mRNA中的掺入造成RNA损伤,进而激活有害的整合应激反应来发挥细胞毒性。研究同时发现了一条由泛素连接酶RNF25介导的mRNA损伤耐受通路,它通过限制ISR的激活来保护细胞,为理解化疗耐药性及开发新靶点提供了重要见解。
| 新使生物专业翻译组一站式服务平台 |
| 产品名称 |
点击图片查看
点击图片查看


 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们
