
导读
转运RNA(tRNA)是蛋白质合成的核心解码器。传统观点认为tRNA仅是被动参与翻译的“接头分子”,但近年来,我们对tRNA生物学的复杂性有了全新的认识。
tRNA不仅是动态的调控中枢,深刻影响着翻译速度、蛋白质折叠保真度和细胞稳态,其生物合成与功能的失调还与神经退行性疾病、癌症等多种人类病理密切相关。
新兴研究揭示,组织特异性的tRNA丰度能够精细调控翻译节律,tRNA还在核糖体相关质量控制(RQC)和整合应激反应(ISR)等细胞监视和应激信号通路中扮演着核心角色。
2026年4月21日,德国汉堡大学的Zoya Ignatova团队在Nature Reviews Molecular Cell Biology上发表了题为“The regulation, function and disease relevance of cytoplasmic tRNAs”的综述文章。该文系统阐述了人类细胞质tRNA的基因组组织与时空表达调控,详述了其成熟与功能监控的质量控制通路,并深入探讨了tRNA作为治疗靶点的巨大潜力,为我们全面理解这一古老而又充满活力的分子提供了前沿视角。

综述整理
一、tRNA表达的时空调控
tRNA的表达并非一成不变,而是受到基因组位置、表观遗传状态和细胞环境的精细调控,以满足不同组织和发育阶段的特定翻译需求。
1.1) tRNA的基因组与表观遗传特征
基因组分布: 人类基因组中注释有429个高可信度的tRNA基因,它们并非随机分布,而是在1号和6号染色体上形成大的基因簇。值得注意的是,6号染色体上的tRNA基因簇与主要组织相容性复合体(MHC)区域紧邻,这种关联在哺乳动物中高度保守,暗示tRNA可能与免疫系统存在调控联系。
拷贝数变异 (CNV): tRNA基因,特别是位于1号染色体上的串联重复序列,表现出广泛的个体间拷贝数差异,这种变异可能影响个体的表型或在特定压力下对疾病的易感性。
表观遗传调控: 大规模染色质状态分析表明,绝大多数(超过80%)的tRNA基因座受到严格的调控或抑制,挑战了tRNA被组成性表达的传统观点。其表达活性具有高度的细胞类型和组织特异性。
1.2) 组织依赖性表达
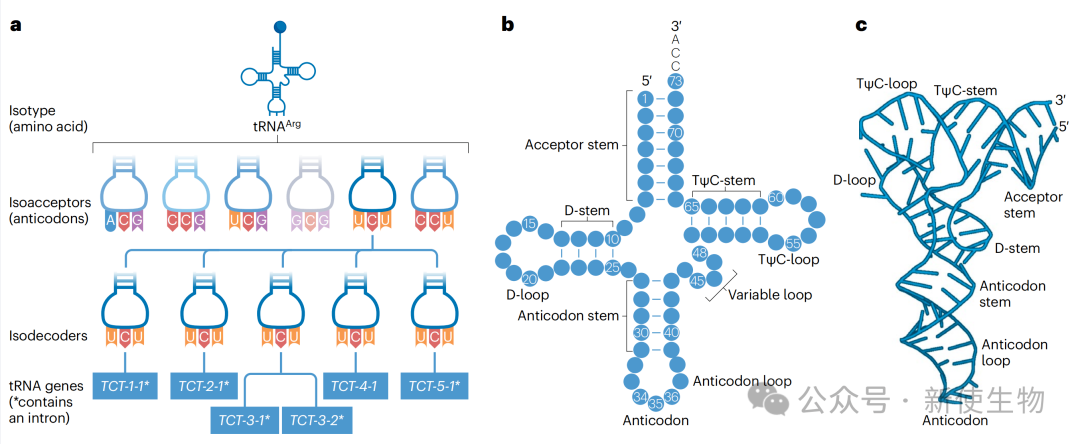
Isodecoder库的多样性: tRNA-seq等高通量测序技术揭示,不同细胞类型和组织间的同功解码tRNA(isodecoder)库组成差异巨大。
Isoacceptor库的稳定性: 令人惊讶的是,尽管isodecoder库多样,但同功受体tRNA(isoacceptor)库在不同组织间却保持着惊人的稳定。
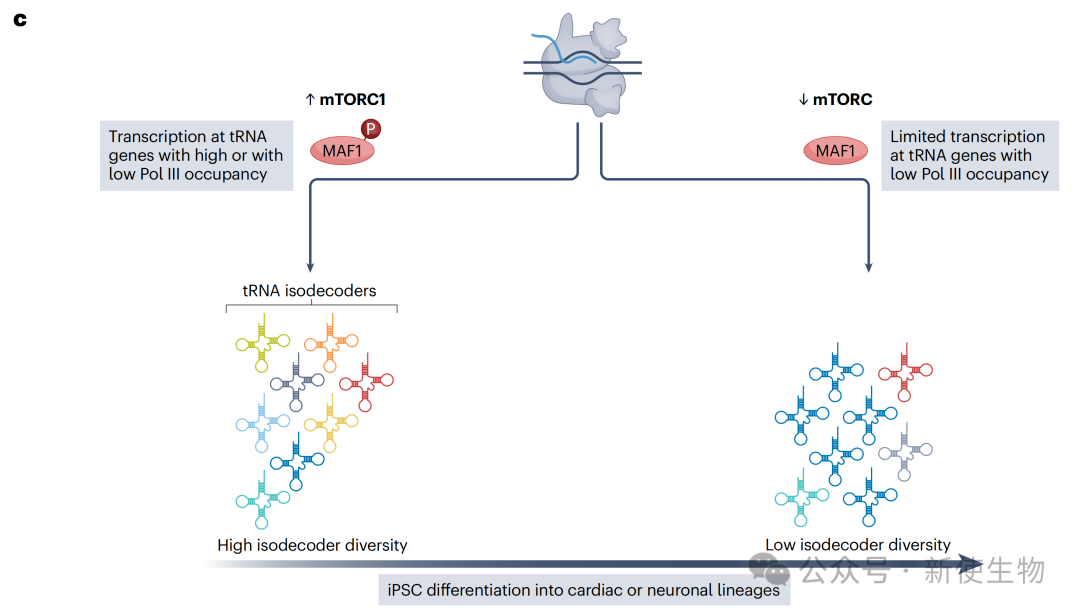
分化过程中的调控: 在细胞分化过程中,mTORC1信号通路的减弱会激活RNA聚合酶III(Pol III)的抑制因子MAF1,从而优先沉默那些在增殖状态下低表达的tRNA基因。这导致分化后细胞的isodecoder多样性降低,但整体反密码子库保持平衡。
二、tRNA的生物合成、氨酰化与质量控制
tRNA从转录到成为功能分子,需经历加工、折叠、修饰和氨酰化等一系列复杂步骤,并受到严格的质量控制。
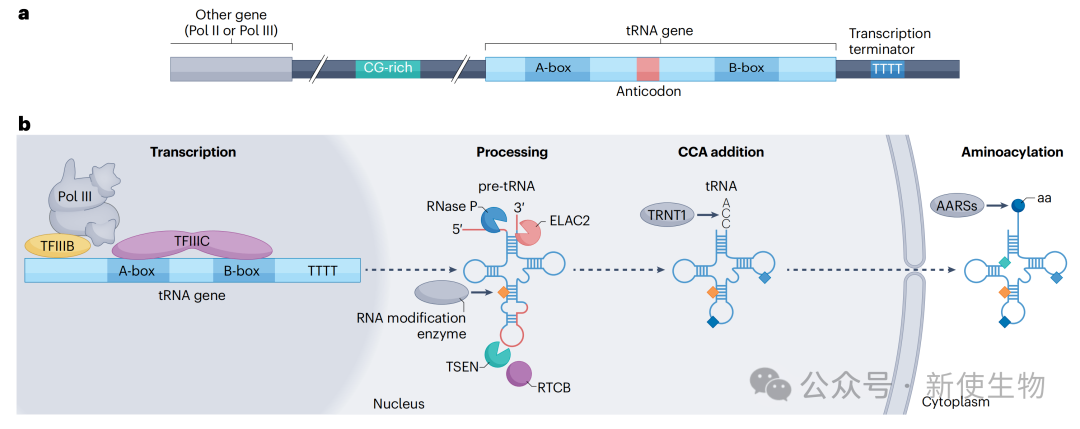
2.1) 转录、加工与折叠
转录: 由Pol III及其转录因子TFIIIC和TFIIIB负责。
加工: nascent pre-tRNA经过多步剪切:RNase P切除5'端前导序列,ELAC2切除3'端尾随序列,TSEN复合物切除内含子,最后由TRNT1在3'末端加上保守的CCA尾巴。
折叠: La蛋白等RNA分子伴侣帮助pre-tRNA正确折叠成L型三维结构,这是后续所有加工步骤正确进行的前提。
2.2) tRNA质量控制通路:多重保障机制
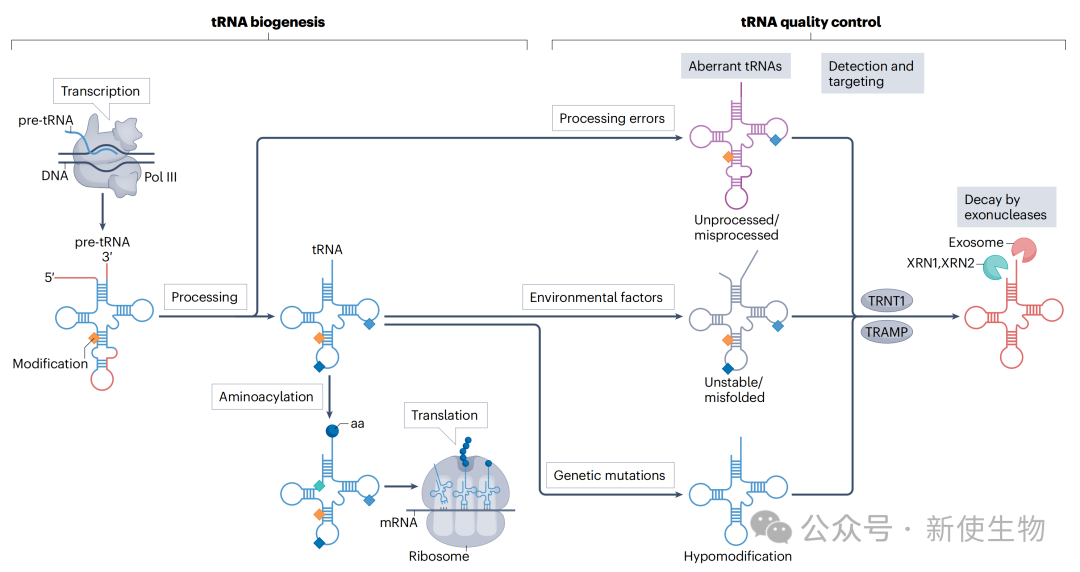
为防止有缺陷的tRNA进入翻译机器造成灾难性后果,细胞进化出多重监视系统。
TRNT1的“质检”功能: TRNT1不仅负责添加CCA,还能感知tRNA的结构稳定性。对于不稳定或错误折叠的tRNA,它会添加一个非标准的CCACCA标签,标记该tRNA由核酸外切酶降解。
TRAMP复合物介导的降解: TRAMP复合物能识别未被正确修饰的tRNA,并通过多聚腺苷酸化作用将其标记,引导Exosome进行3'→5'方向的降解。
XRN1/XRN2介导的降解: 当tRNA特定位置的修饰缺失导致其结构不稳定时,其5'末端会暴露,从而被XRN1/XRN2核酸外切酶识别并进行5'→3'方向的降解。
三、tRNA在翻译调控中的功能
除了作为解码器,tRNA还是调节翻译动态和细胞应激反应的主动参与者。
3.1) 翻译速度的决定者
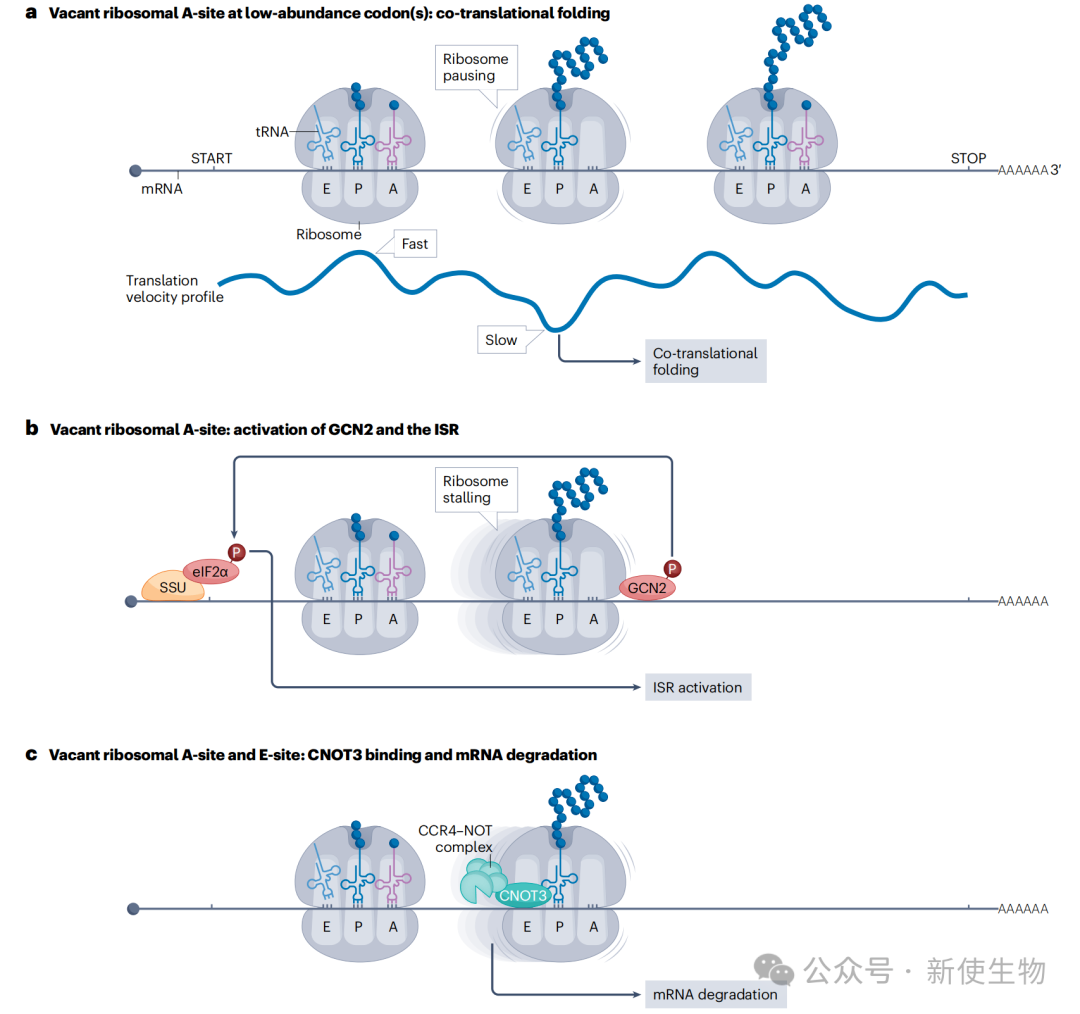
密码子速度: 细胞内不同tRNA的丰度差异巨大(可达一个数量级),导致不同密码子的翻译速度也相差悬殊。低丰度tRNA对应的密码子会造成核糖体短暂暂停,从而形成一种独特的翻译“节律”。
协同翻译折叠: 这种速度变化并非随机,而是具有重要的生理意义,如调控新生肽链的共翻译折叠、招募蛋白因子、促进蛋白复合物组装等。
同义突变的非沉默效应: 由于同义密码子对应的tRNA丰度不同,同义单核苷酸多态性(sSNP)可以改变翻译速度。一个经典例子是CFTR基因中的一个常见sSNP,它将一个快密码子变为慢密码子,导致在支气管组织中CFTR蛋白表达量降低约30%,影响其通道功能。
3.2) 细胞质量控制的感知中枢
tRNA是细胞感知翻译压力和营养状况的关键传感器。
激活整合应激反应 (ISR):在氨基酸匮乏时,未被氨酰化的tRNA会积累,并激活GCN2激酶。GCN2通过磷酸化eIF2α来抑制全局翻译起始,同时选择性地翻译应激相关蛋白,启动ISR。
触发mRNA降解:当核糖体因稀有tRNA不足而停滞时,其A位点和E位点会同时空出。这种状态能被CCR4-NOT复合物的亚基CNOT3识别,后者结合到E位点,并招募整个复合物来降解该mRNA。
四、tRNA相关的病理与治疗
tRNA生物合成或功能的失调与多种人类疾病,特别是神经系统疾病和癌症,密切相关。
4.1) tRNA相关病理
遗传性疾病: tRNA基因本身高度保守,突变罕见。但其加工酶(如Pol III、TSEN)或氨酰-tRNA合成酶(aaRSs)的突变是多种神经退行性疾病(如脊髓小脑性共济失调)的常见原因。
癌症: 癌细胞为满足其旺盛的增殖需求,常常上调特定tRNA的表达,以加速翻译富含相应氨基酸的蛋白质。
4.2) 新兴tRNA疗法
利用tRNA作为药物,为治疗由基因突变引起的疾病提供了革命性的新思路。
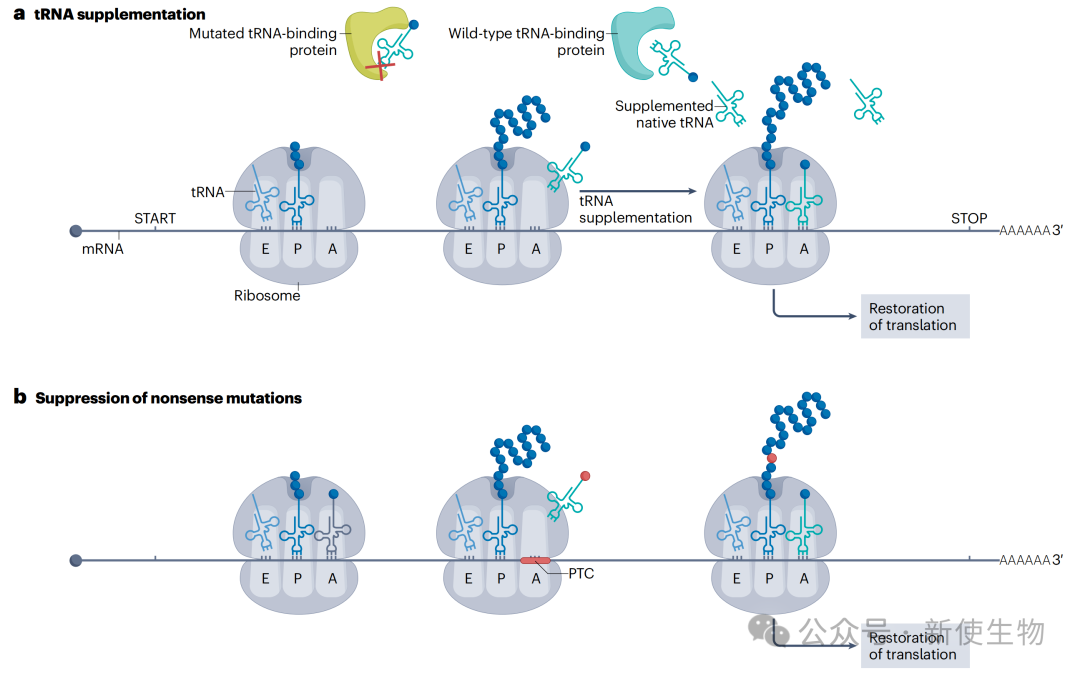
tRNA补充疗法: 对于因aaRS突变导致tRNA被错误“扣押”而引发的疾病(如腓骨肌萎缩症CMT),通过外源补充相应的正常tRNA,可以恢复细胞内tRNA供需平衡,缓解核糖体停滞和神经退行性病变。
抑制性tRNA(sup-tRNA)疗法: 通过基因工程改造tRNA的反密码子,使其能够识别并“通读”由无义突变产生的提前终止密码子(PTC)。这种“PTC抑制”策略能够恢复全长功能蛋白的合成,为囊性纤维化、杜氏肌营养不良等约11%的单基因遗传病提供了全新的治疗希望。临床前研究已通过AAV或LNP递送sup-tRNA,在动物模型中验证了其有效性。
总结
综上所述,tRNA早已超越了传统意义上静态解码器的角色,转而作为高度动态的调控因子全面参与基因表达的时空控制和细胞监控机制。深入解析tRNA复杂的生理与病理网络,将为未来靶向tRNA系统治疗各类遗传性及代谢性疾病提供革命性的精准医疗思路。


 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们
