
导读
无义介导的mRNA降解(Nonsense-mediated mRNA decay, NMD)是一种重要的细胞内mRNA质量监视机制。它能够识别并降解含有提前终止密码子(PTC)的异常转录本,从而防止潜在有害的截短蛋白的产生。
RNA解旋酶UPF1是NMD通路的核心因子,在维持转录组稳态中扮演着极为重要的角色。然而,UPF1在人类细胞中是维持生存所必需的,这使得通过传统基因敲除方法研究其直接调控的靶标和分子功能变得极为困难。
以往的研究多依赖于RNA干扰(siRNA)技术,但该方法降解效率有限且耗时长,难以区分直接与间接效应。
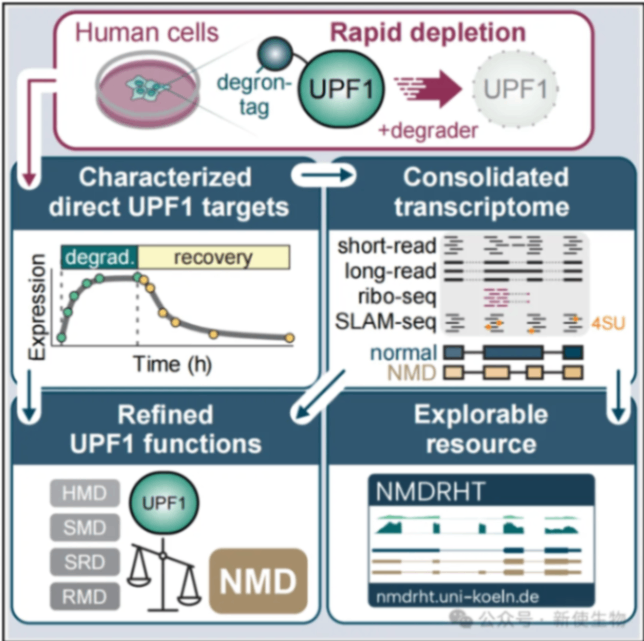
2025年9月18日,德国科隆大学Niels H. Gehring团队与马克思·德尔布吕克分子医学中心Markus Landthaler团队合作,在Molecular Cell上发表了题为“Rapid UPF1 depletion illuminates the temporal dynamics of the NMD-regulated human transcriptome”的论文。该研究通过开发可快速降解内源性UPF1蛋白的细胞系,结合多组学分析,以前所未有的时间分辨率揭示了NMD的直接靶标及其动态调控规律。

文章索引
【标题】Rapid UPF1 depletion illuminates the temporal dynamics of the NMD-regulated human transcriptome
【发表期刊】Molecular Cell
【发表日期】2025年9月18日
【作者及团队】德国科隆大学Niels H. Gehring团队与马克思·德尔布吕克分子医学中心Markus Landthaler团队
【IF】16.6
研究结果
一、快速UPF1降解系统的构建与验证
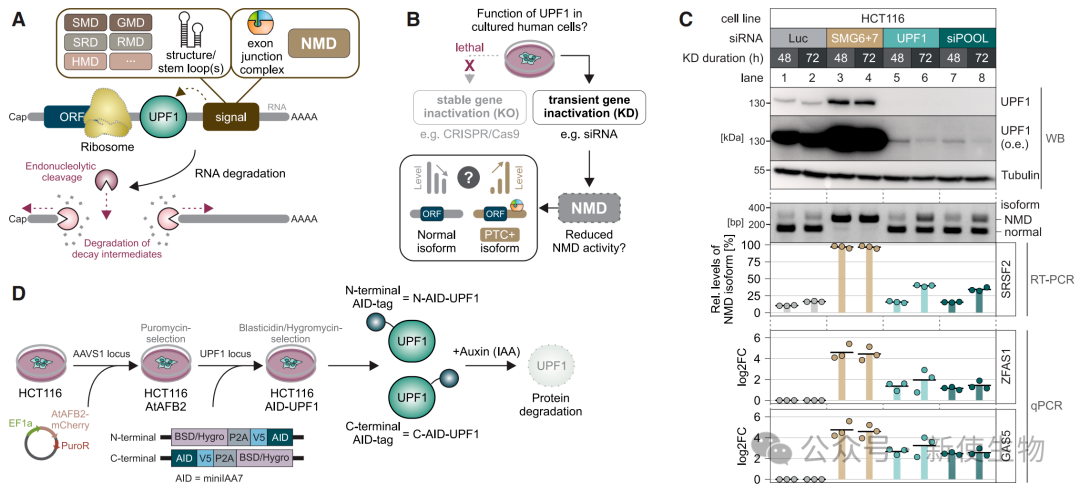
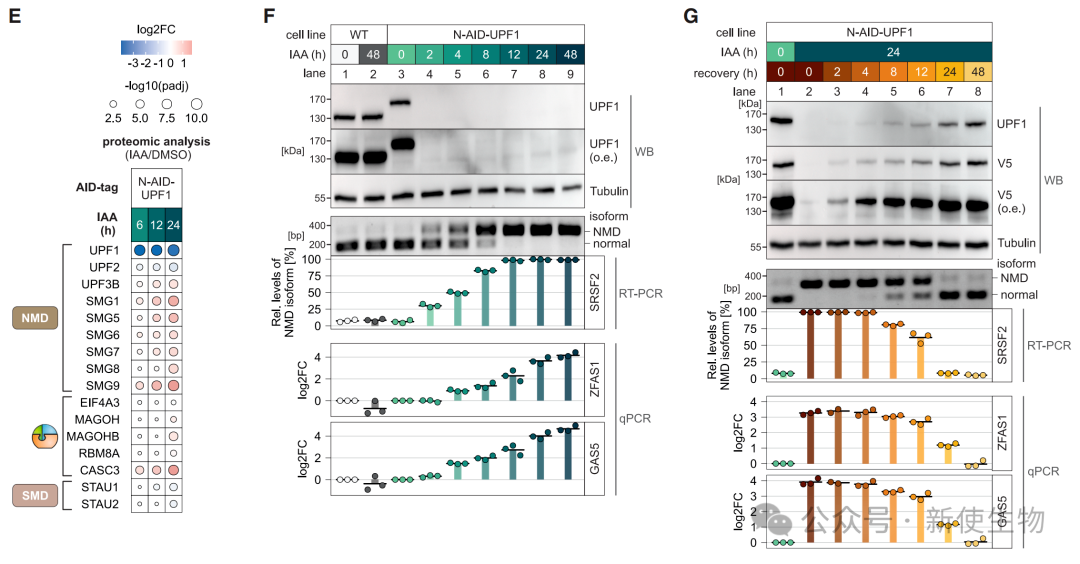
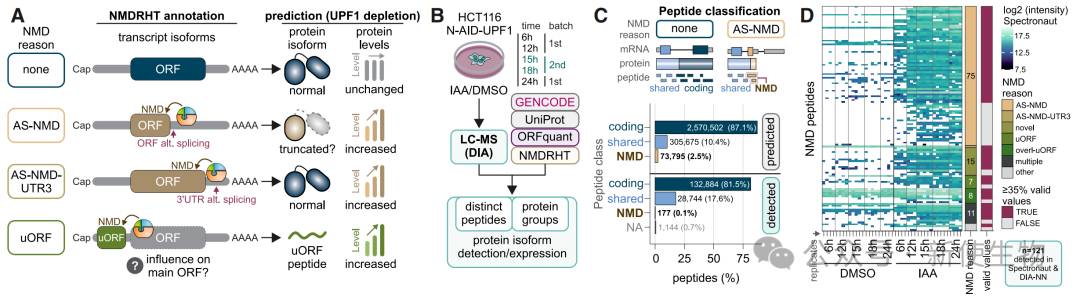
研究团队利用Auxin-inducible degron (AID) 和dTAG两种条件性蛋白质降解系统,在人类细胞中对内源性UPF1蛋白进行标记。
结果表明,这两种系统均能在数小时内快速、特异性地降解UPF1蛋白,引发了比传统siRNA更强烈的NMD抑制效应,并且该过程是可逆的。
二、时间分辨转录组学鉴定出NMD的直接靶标
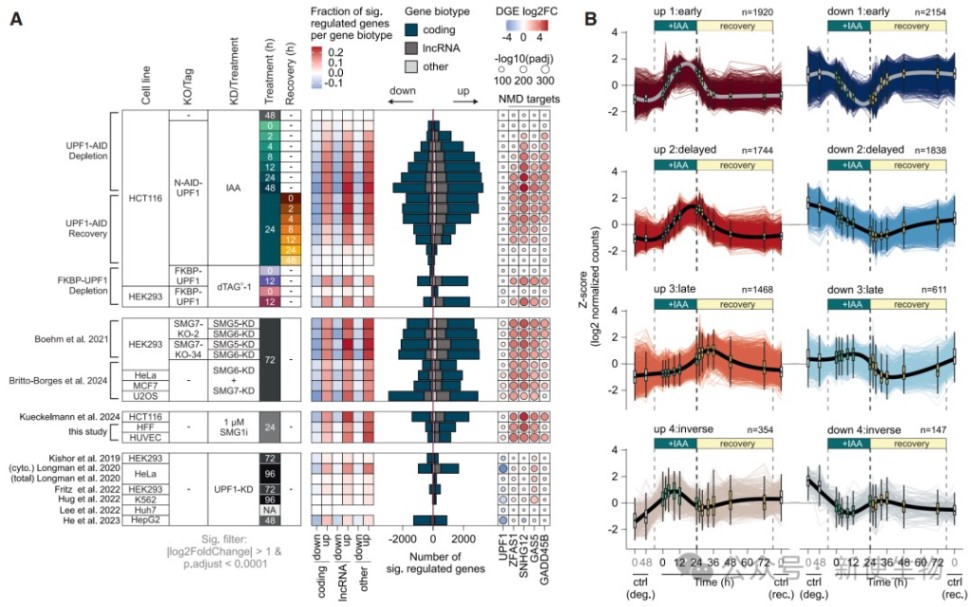
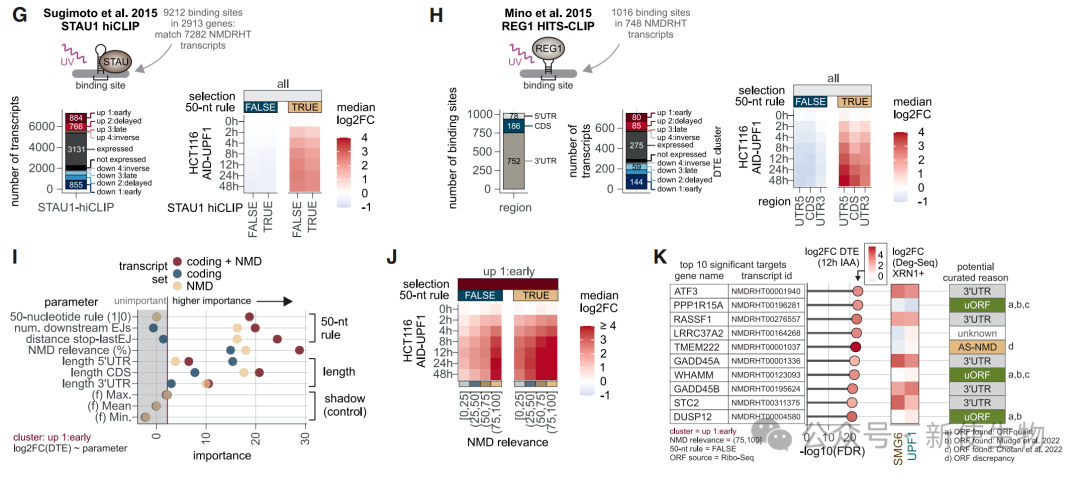
通过时间序列RNA-seq分析,研究人员将UPF1调控的转录本分为“早期响应”、“延迟响应”、“晚期响应”和“反向调控”四类。
早期和延迟响应类转录本富集于已知NMD靶标,且具有较高的“NMD相关性”,表明它们是UPF1的直接降解靶标。
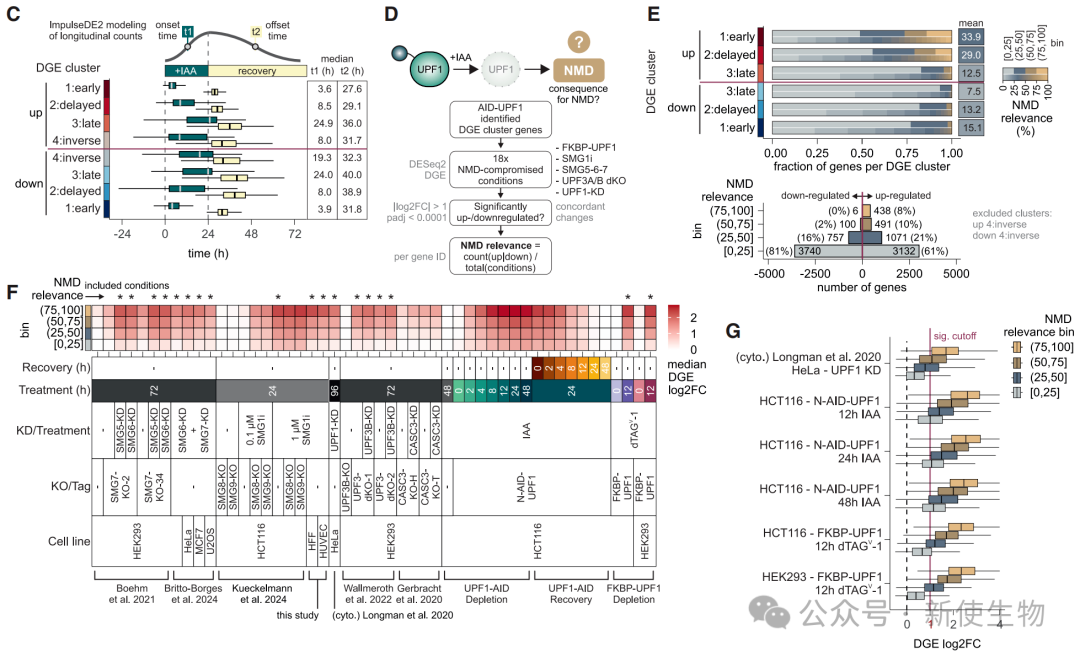
三、UPF1通过促进mRNA降解来调控靶标转录本
结合SLAM-seq和Ribo-seq核糖体印迹分析,研究发现UPF1缺失导致大量转录本稳定性增加,降解速率下降,而合成速率变化较小。
进一步实验证实,UPF1主要通过翻译依赖的降解机制调控其靶标。
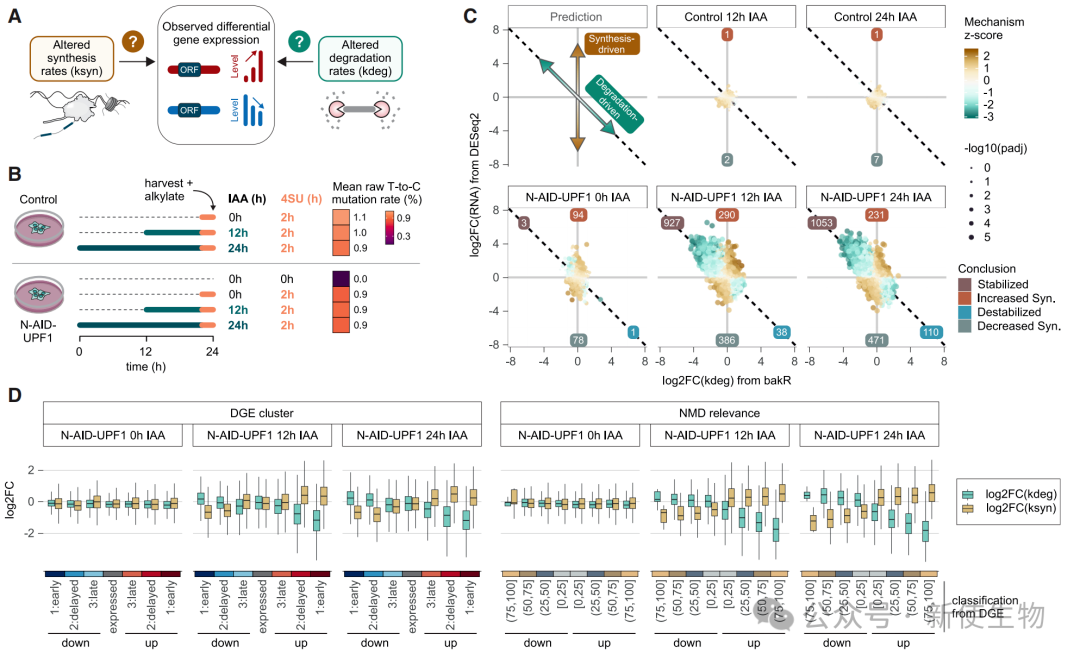
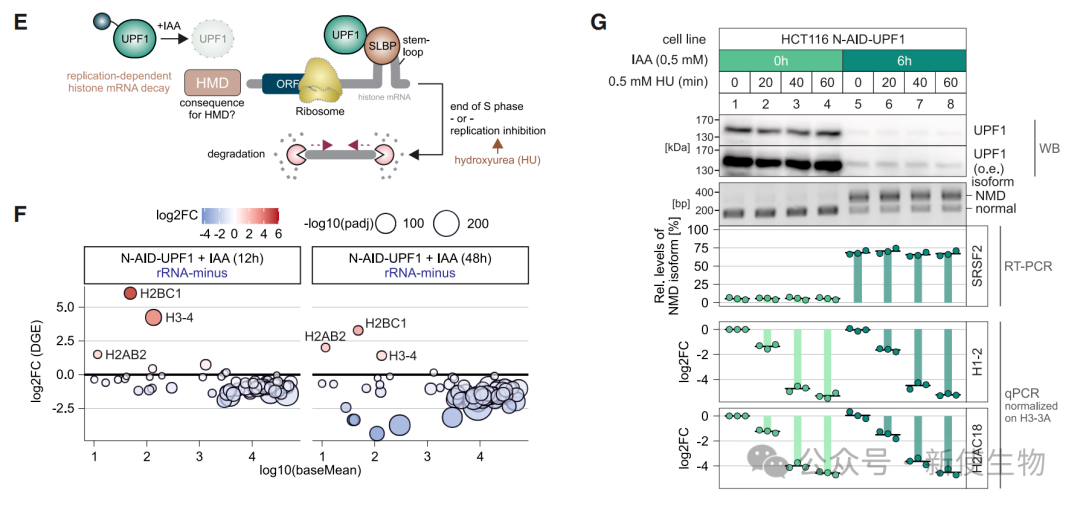
四、UPF1在复制依赖性组蛋白mRNA降解(HMD)中作用甚微
作者通过rRNA去除的RNA测序和羟基脲(HU)处理诱导HMD,发现无论是短期还是长期的UPF1降解,均不影响复制依赖性组蛋白mRNA的正常降解。
五、整合多组学数据构建NMD调控的人类转录本图谱(NMDRHT)
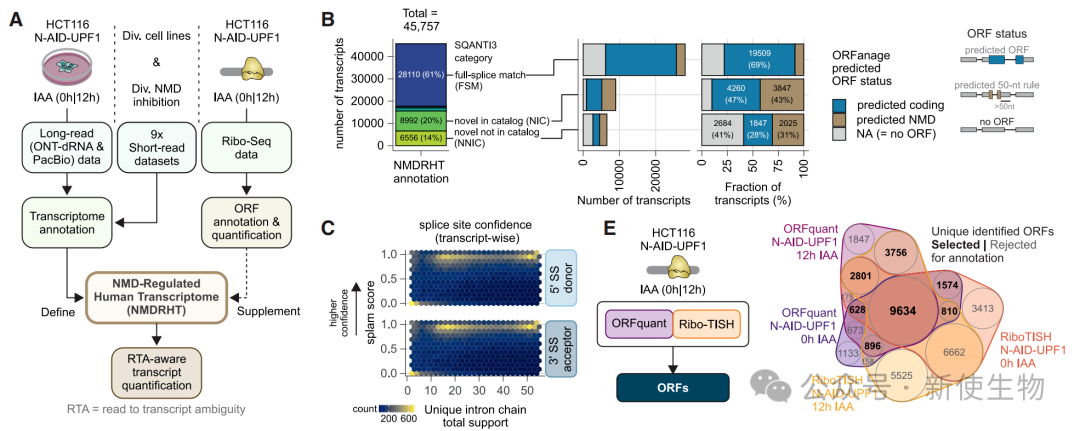
为解决短读长测序在转录本定量和注释上的局限性,研究整合了Oxford Nanopore(ONT)和PacBio长读长测序数据。
通过结合多细胞系、多抑制条件下的短读长数据,作者构建了一个包含45,747个转录本的高质量注释集——NMDRHT。
该注释集显著提升了转录本定量的准确性,尤其是对于选择性剪接产生的NMD敏感异构体。
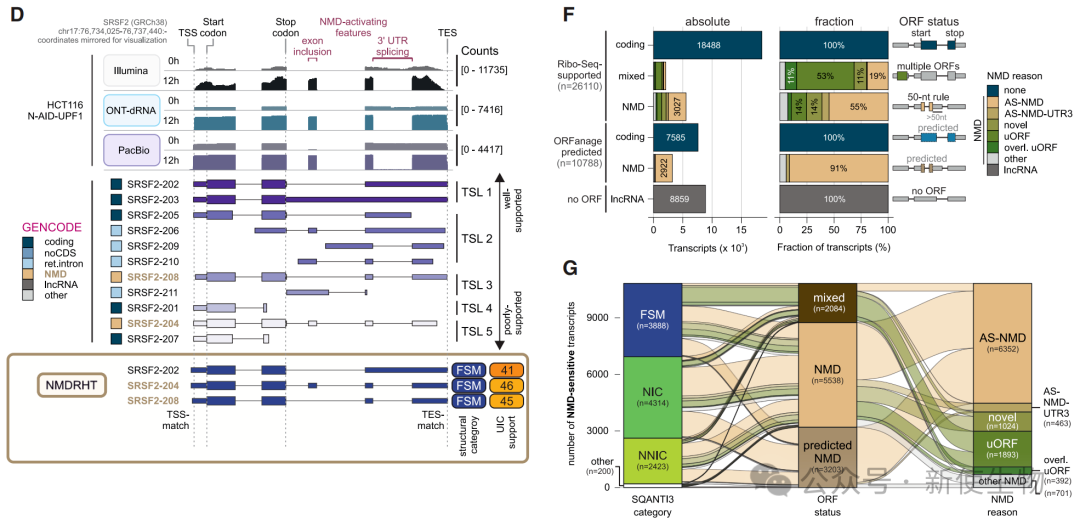
六、可变剪接是产生NMD靶标转录本的主要驱动因素
通过NMDRHT注释和定量分析,发现AS-NMD是最主要的NMD激活机制,其次是uORF和3′ UTR剪接事件。
novel转录本在UPF1缺失后显著积累,凸显了长读长数据在发现新异构体中的价值。
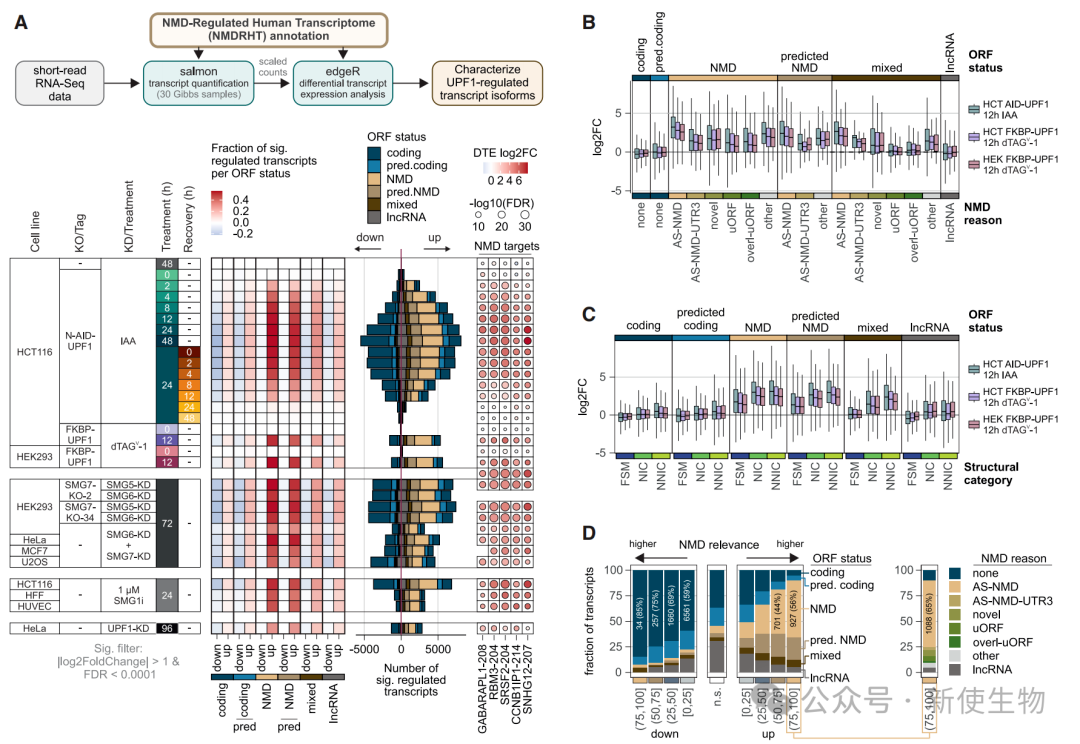
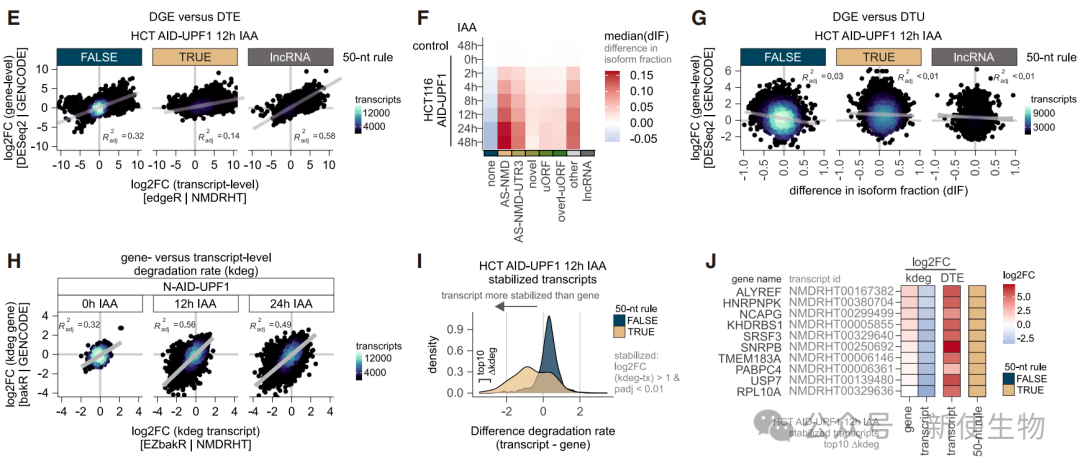
七、发现非经典或未注释的特征介导部分UPF1依赖的降解
研究发现,一小部分被UPF1快速调控的转录本并不符合经典的NMD识别规则。
作者排除了其他已知的UPF1相关降解通路(如SMD、SRD)的可能性,并通过精细分析推断。
这些转录本的降解可能是由一些未被常规注释的特征(如微小的上游开放阅读框uORF或3' UTR中的特殊元件)所介导的。
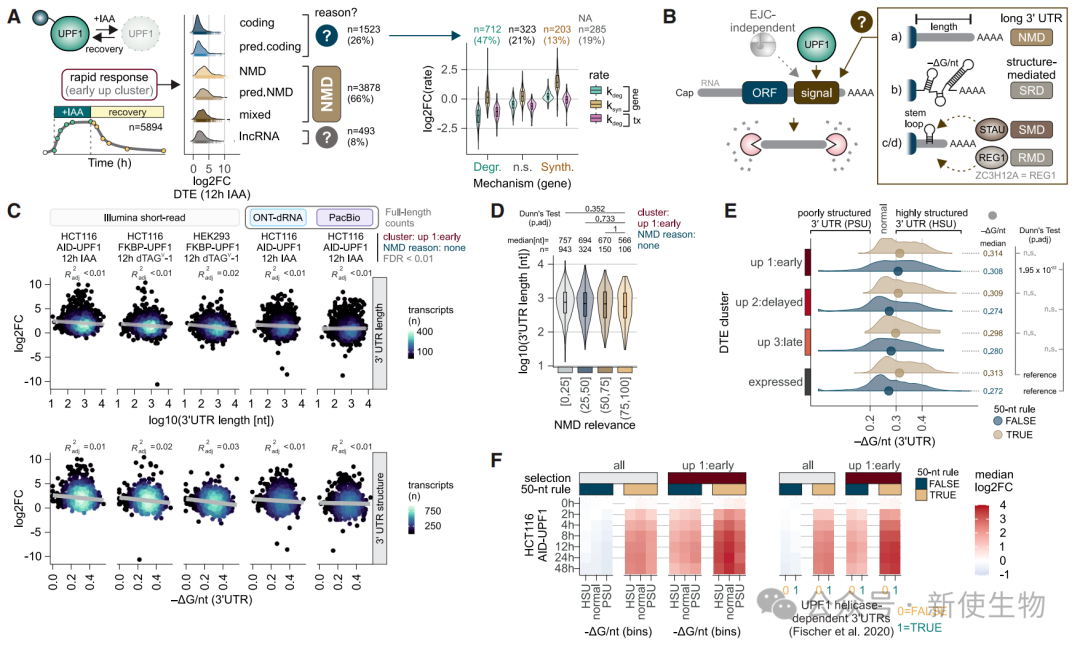
八、NMD抑制导致截短蛋白的积累并扰乱细胞稳态
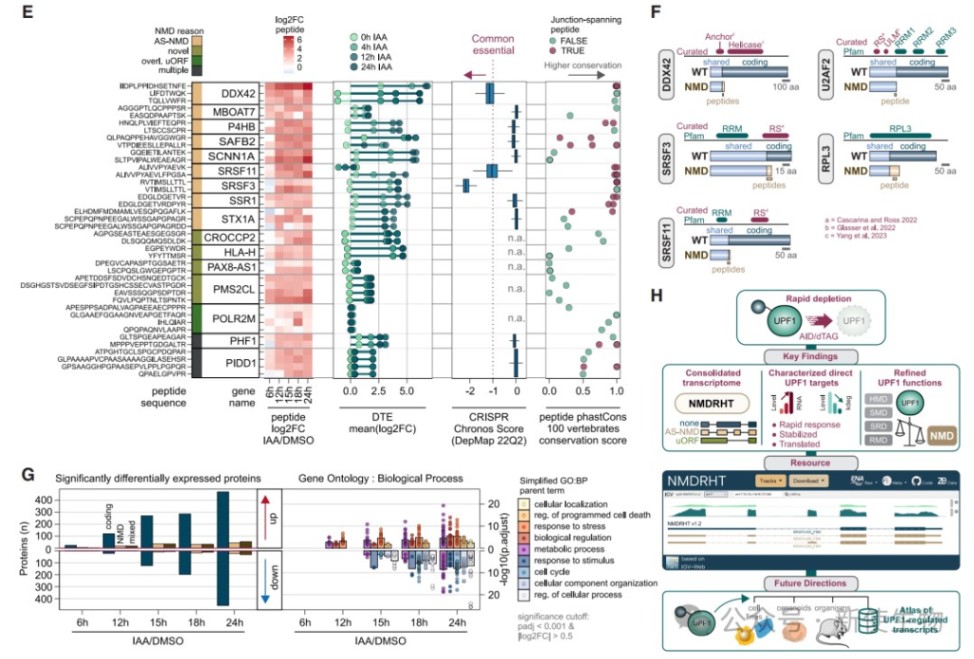
通过肽段水平的蛋白质组学分析,研究人员检测到部分由NMD异构体编码的 truncated 蛋白或肽段在UPF1缺失后积累。
这些肽段多来自RNA加工和剪接相关蛋白,其积累可能进一步扰乱细胞稳态。
此外,多个人类特异性基因(如CROCCP2和NBPF家族)在UPF1缺失后表达上调,提示NMD在调控近期进化基因中发挥重要作用。
总结
本研究通过快速、可逆的UPF1降解系统,结合多组学技术和长读长测序,首次在时间和分子分辨率上系统描绘了UPF1直接调控的转录组图谱,构建了高质量NMD转录本注释资源NMDRHT,并揭示选择性剪接是NMD最主要的激活机制。
| 新使生物专业翻译组一站式服务平台 |
| 产品名称 |
我们能够针对微量细胞或组织,如卵母细胞、卵巢、临床穿刺样品等产出高质量翻译组数据结果。
超高的准确性为研究非经典的开放阅读框(ORFs)提供极大便利,提高微肽(肿瘤新生抗原)的挖掘效率。
另外新使生物提供多物种多聚核糖体分析(Polysome profiling),了解更多翻译组技术信息可登录 www.neoribo.com。
点击图片查看
点击图片查看


 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们
