
导读
线粒体蛋白的精准定位对于维持细胞正常的代谢功能至关重要,绝大多数线粒体蛋白由核基因编码并在胞质中合成。核编码线粒体mRNA的翻译与定位过程受到多种调控机制的影响,但其分子机制尚不完全明确。
剪接因子U2AF1与U2AF2组成的异二聚体在细胞核内调控剪接,同时也能在胞质中穿梭并参与mRNA代谢。近年来,研究发现U2AF1的S34F突变在骨髓增生异常综合征等多种癌症中高频出现,且该突变与线粒体功能障碍密切相关。
然而,剪接因子在胞质中如何协调mRNA翻译与定位,以及这种非典型功能在肿瘤发生中的作用仍是一个未解之谜。解析这些RNA结合蛋白在核质间的协调机制,对于理解肿瘤代谢重编程具有重要的科学意义。
2026年4月2日,美国国家癌症研究所Daniel R. Larson团队在Molecular Cell上发表了题为“U2AF regulates the translation and localization of nuclear-encoded mitochondrial mRNAs”的论文。该研究揭示了剪接因子U2AF在胞质中具有调控核编码线粒体mRNA翻译与定位的非典型功能,该功能对于维持线粒体结构与功能至关重要。

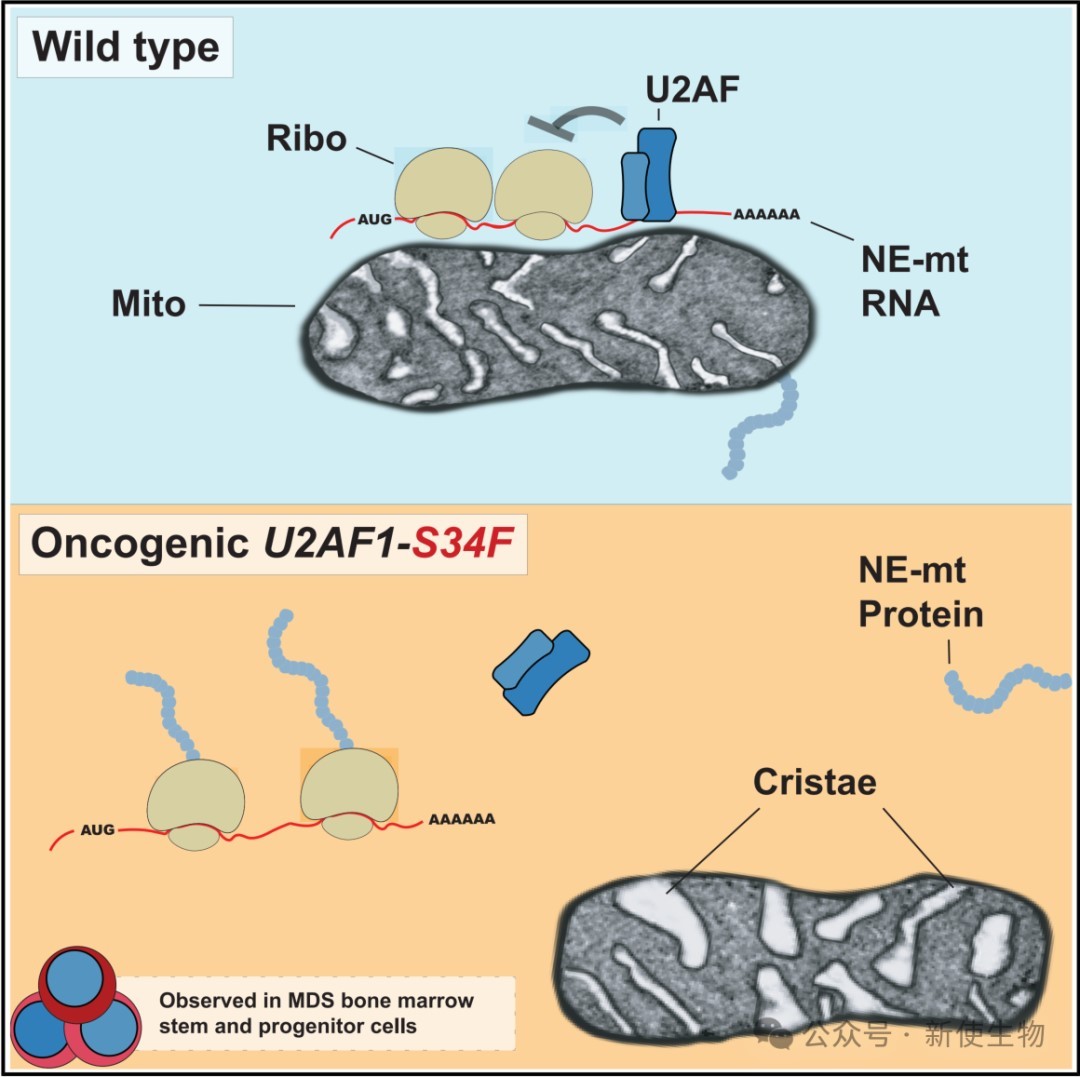
文章索引
【标题】U2AF regulates the translation and localization of nuclear-encoded mitochondrial mRNAs
【发表期刊】Molecular Cell
【发表日期】2026年4月2日
【作者及团队】美国国家癌症研究所Daniel R. Larson团队
【IF】16.6
研究结果
一、U2AF在细胞质中与线粒体蛋白及mRNA相互作用
通过亚细胞组分分离结合免疫沉淀-质谱联用技术,研究者发现U2AF在细胞质中与大量线粒体蛋白相互作用,超高分辨率显微镜和线粒体免疫沉淀实验证实U2AF定位于线粒体外膜。
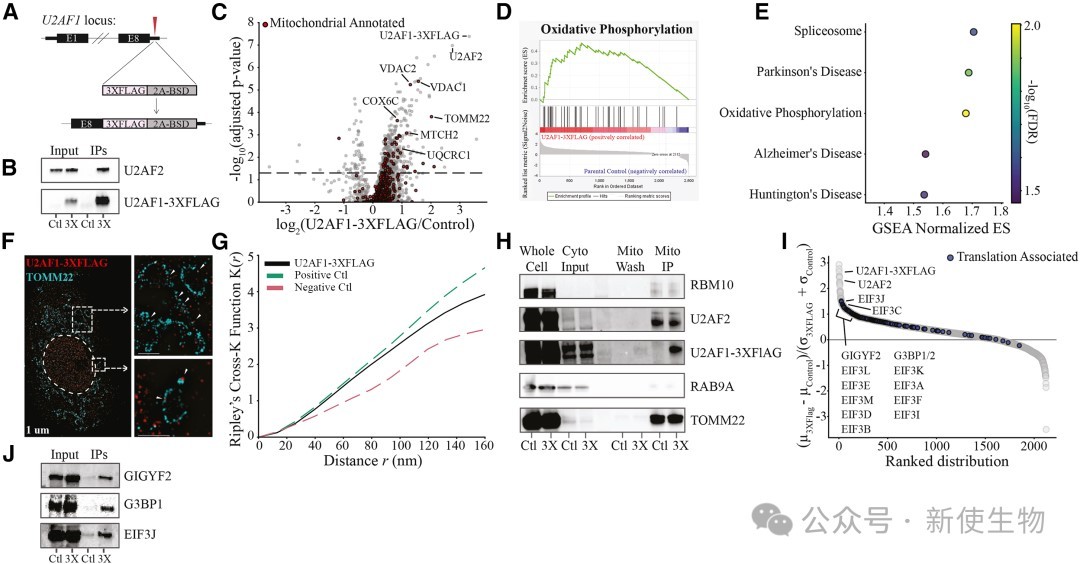
对PAR-CLIP数据的再分析显示,U2AF优先结合在核编码线粒体(NE-mt)mRNA靠近翻译起始密码子的编码区,且其结合能力会因致癌的S34F突变而减弱。
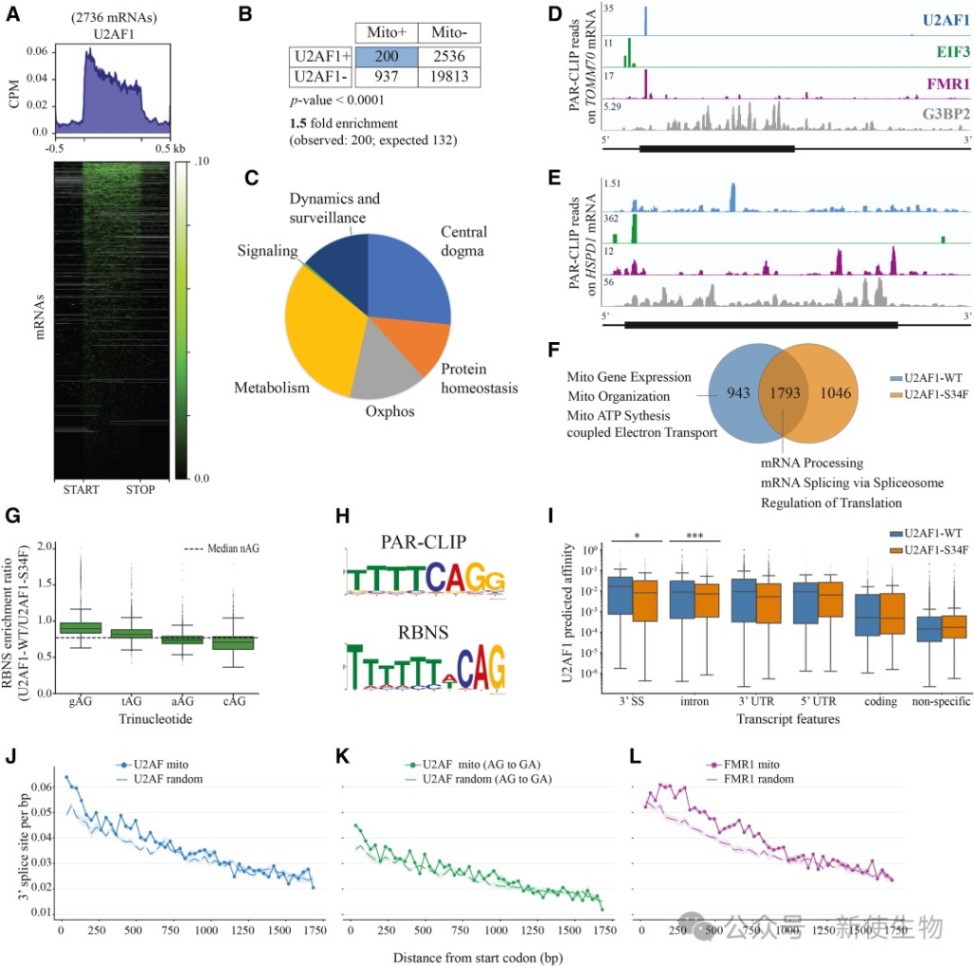
二、U2AF通过在结合位点诱导核糖体停滞来抑制翻译
通过将Ribo-seq核糖体印迹分析数据与PAR-CLIP数据进行互相关分析,发现U2AF的结合位点与其上游的双核糖体(disome)积累显著相关,表明U2AF可能作为一个动态路障,导致核糖体在其结合位点附近暂停。
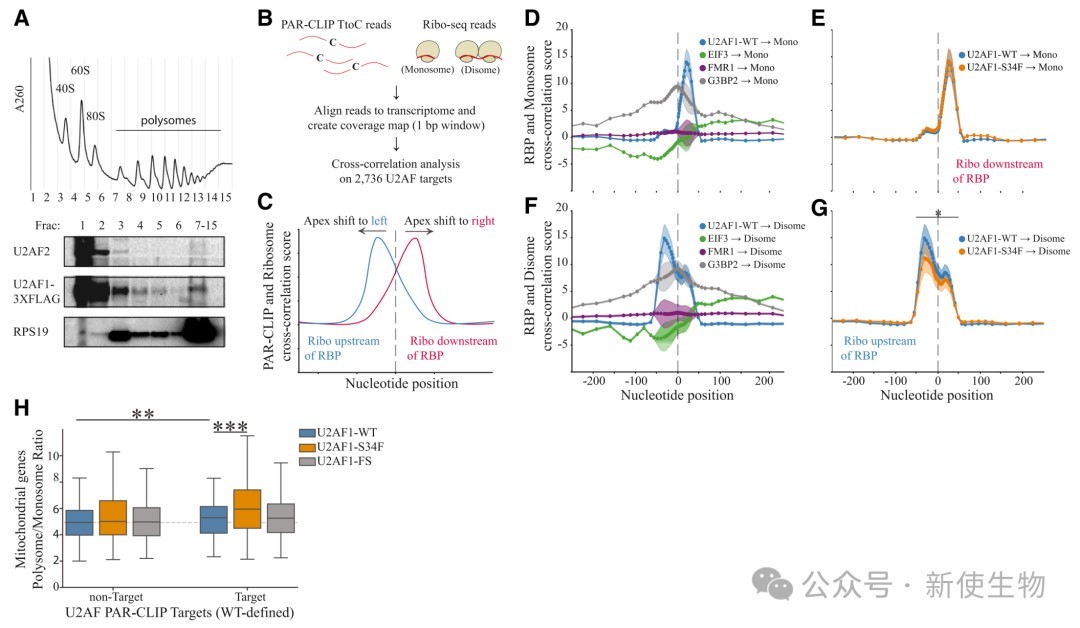
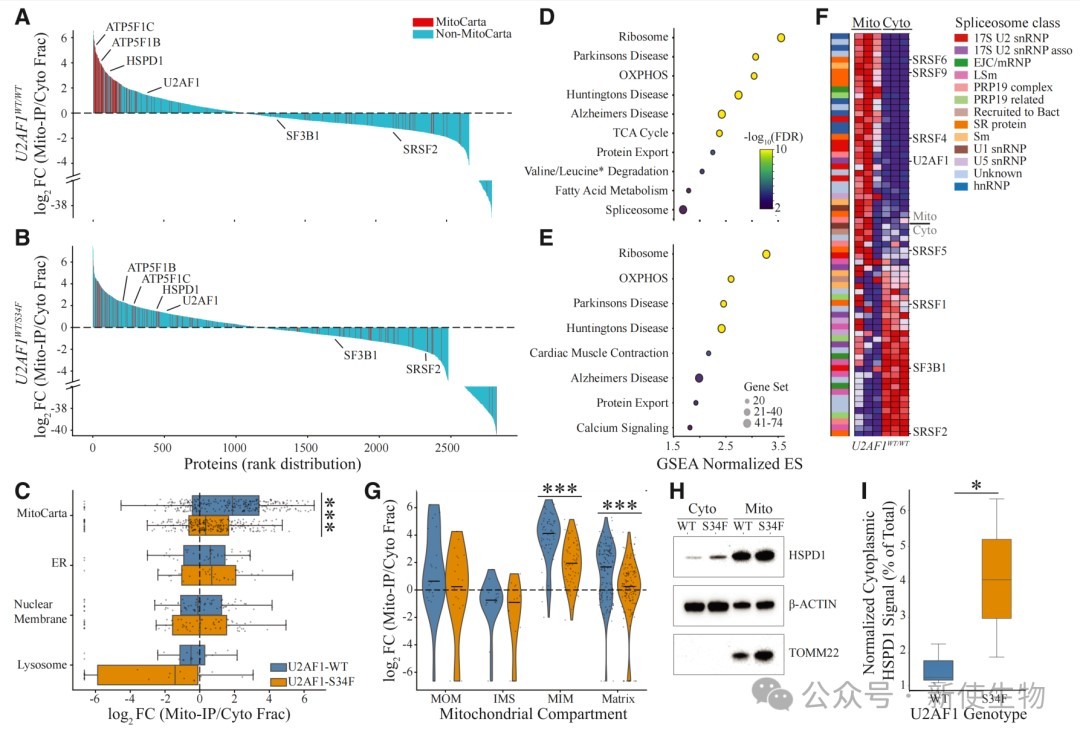
三、U2AF1-S34F突变导致线粒体蛋白质组紊乱和蛋白错误定位
利用线粒体免疫沉淀结合定量蛋白质组学技术,研究发现U2AF1-S34F突变细胞的线粒体蛋白质组发生广泛改变,特别是线粒体内膜和基质的蛋白丰度显著降低。
同时,Western Blot验证显示,部分线粒体蛋白在突变细胞的细胞质中异常积累,表明U2AF1功能失调损害了线粒体蛋白的有效靶向和定位。
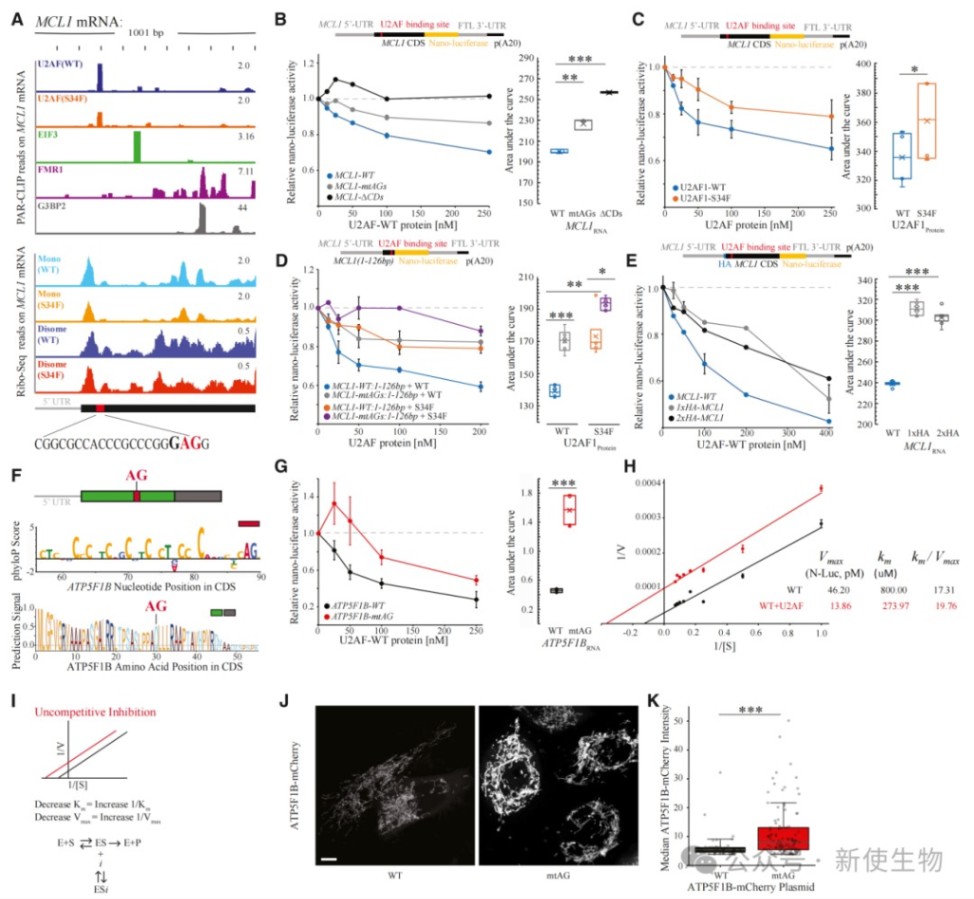
四、U2AF1直接抑制NE-mt mRNA的翻译且该功能受S34F突变影响
利用无细胞体系的体外翻译实验,研究者证实U2AF能以序列和位置依赖的方式直接抑制含有其结合位点的报告mRNA的翻译。
这种抑制作用被U2AF1-S34F突变蛋白显著减弱,或在结合位点被突变后消除,进一步证明了U2AF在翻译起始或早期延伸阶段的直接抑制功能。
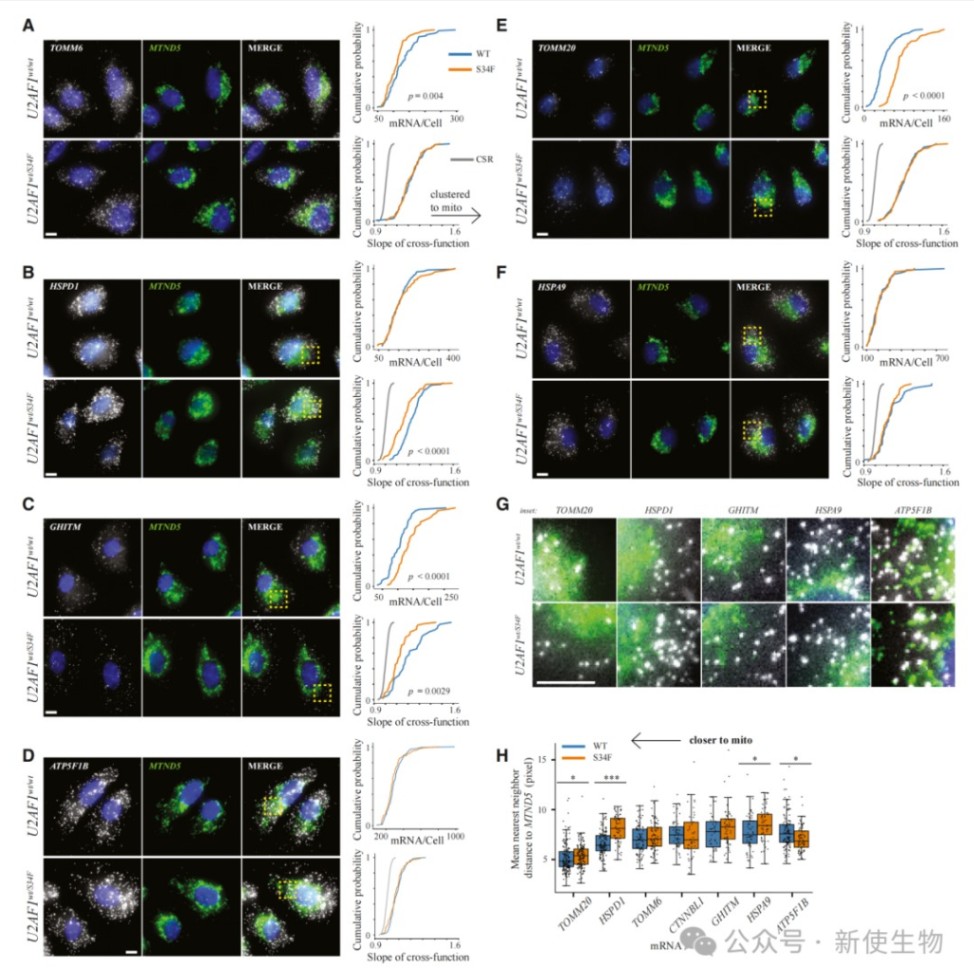
五、U2AF1调控NE-mt mRNAs向线粒体的定位
通过双色单分子荧光原位杂交(smFISH)技术,研究者在单细胞水平上观察了多个NE-mt mRNA与线粒体的空间关系。
结果显示,在U2AF1-S34F突变细胞中,多个U2AF1靶向的mRNA与线粒体的共定位程度显著低于野生型细胞,表明U2AF介导的翻译调控与其对mRNA的亚细胞定位作用是耦合的。
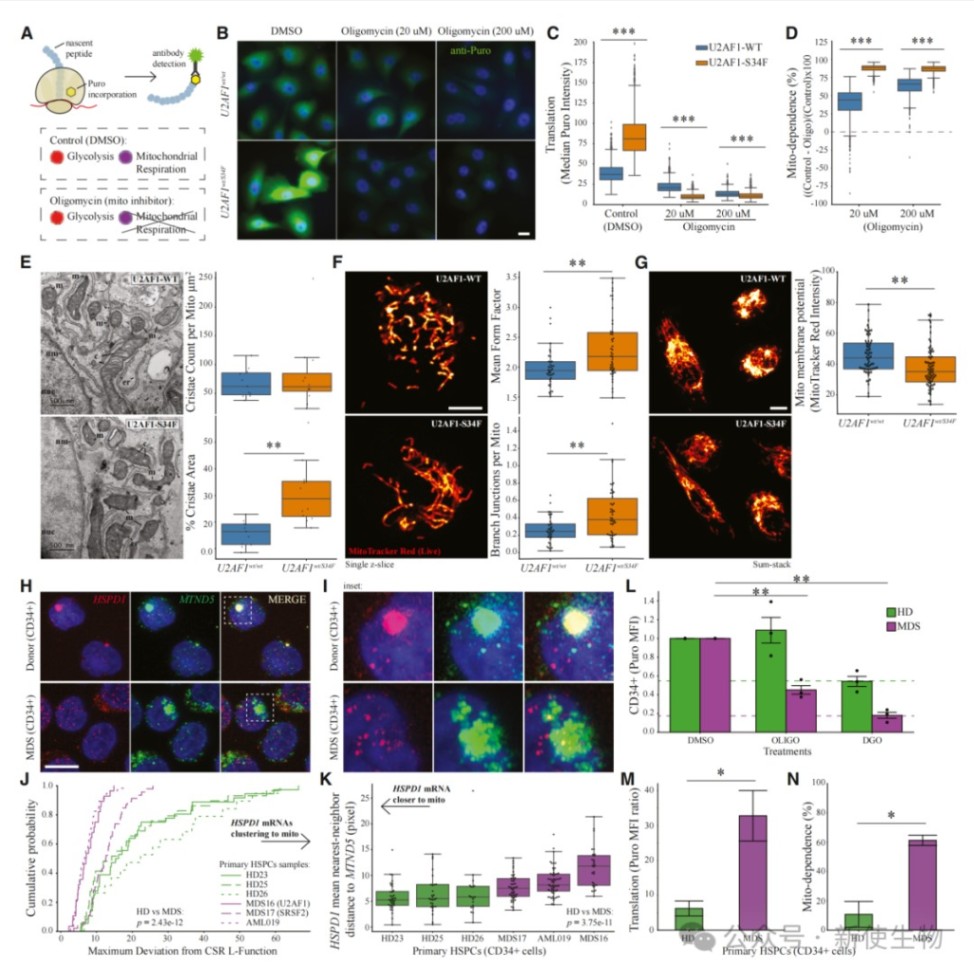
六、U2AF1-S34F突变导致细胞代谢重塑并重现MDS患者的线粒体功能障碍表型
功能实验表明,U2AF1-S34F突变细胞的基础翻译水平更高,线粒体形态异常,且对线粒体呼吸的能量依赖性显著增强。
此外,在从MDS患者体内分离的原代造血干/祖细胞中,研究者发现HSPD1 mRNA与线粒体的共定位被破坏,且细胞表现出异常增高的翻译水平和对线粒体呼吸的依赖性。
总结
该研究揭示了剪接因子U2AF在调控核编码线粒体基因表达中的一个非经典作用,即通过抑制翻译来协调mRNAs向线粒体的定位。一个常见的致癌突变U2AF1(S34F)破坏了这一精细调控,导致了多方面的线粒体功能缺陷,这为理解MDS等疾病的发病机制提供了新的视角,并强调了RNA结合蛋白在维持细胞器稳态中的重要性。
| 新使生物专业翻译组一站式服务平台 |
| 产品名称 |
点击图片查看
点击图片查看


 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们
