
导读
细菌进化出多种防御系统,包括CRISPR-Cas系统,以识别并切割噬菌体及其他移动遗传元件的DNA。作为反制措施,噬菌体编码抗CRISPR(Acr)蛋白,通过阻断DNA结合或切割来抑制CRISPR-Cas活性。
大多数已知的Acr蛋白通过直接结合核糖核蛋白复合物来抑制其功能,或者通过酶促修饰使复合物失活。这些分子间的冲突构成了细菌与噬菌体之间激烈的进化军备竞赛。
了解这些抑制机制对于揭示细菌基因调控的新范式以及开发新型基因编辑工具具有重要意义。然而,许多Acr蛋白的具体作用机制仍不明确,限制了我们对这些分子冲突的全面理解。
2026年4月29日,加州大学旧金山分校Joseph Bondy-Denomy与Nicole D. Marino团队合作,在Nature上发表了题为“Translation-dependent degradation of cas12 mRNA triggered by an anti-CRISPR”的研究论文。该研究发现了一种全新的抗CRISPR作用机制,即AcrVA2蛋白通过在翻译过程中识别并结合Cas12a新生肽链的N端保守基序,进而触发对cas12a mRNA的特异性降解。

文章索引
【标题】Translation-dependent degradation of cas12 mRNA triggered by an anti-CRISPR
【发表期刊】Nature
【发表日期】2026年4月29日
【作者及团队】加州大学旧金山分校Joseph Bondy-Denomy和Nicole D. Marino团队
【IF】48.5
研究结果
一、AcrVA2特异性下调不同来源的cas12a mRNA和蛋白水平
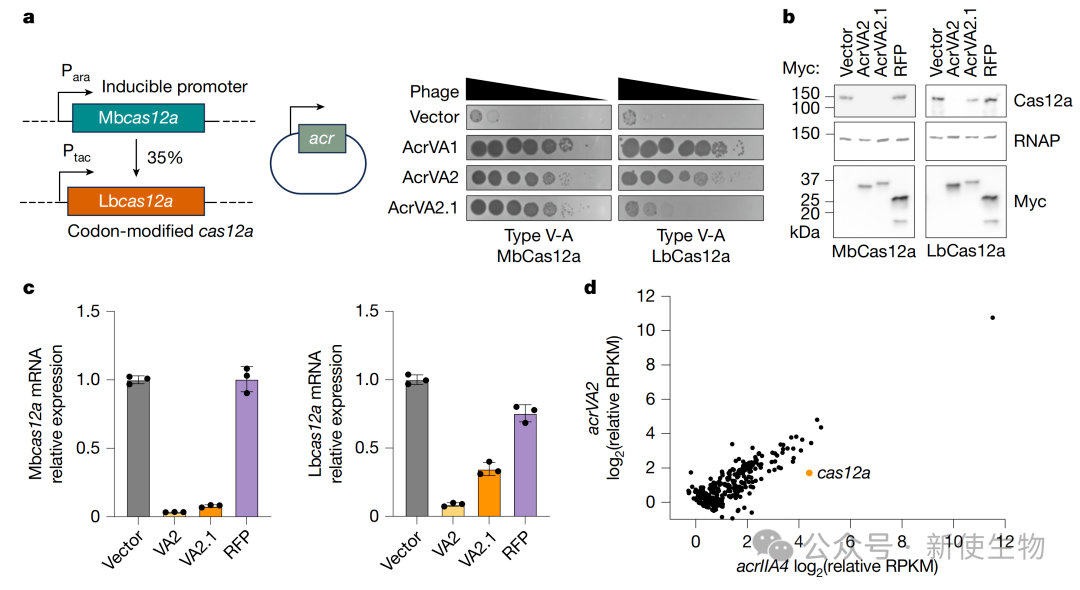
研究人员通过噬菌斑实验、蛋白质印迹和qRT-PCR等方法,证明AcrVA2能够有效抑制两种不同来源(MbCas12a和LbCas12a)的Cas12a活性,并显著降低其蛋白和mRNA水平。
转录组分析进一步证实,AcrVA2的下调作用对cas12a转录本具有高度特异性,且这种效应独立于启动子和核苷酸序列。
二、AcrVA2通过结合Cas12a N端的保守基序来触发mRNA降解
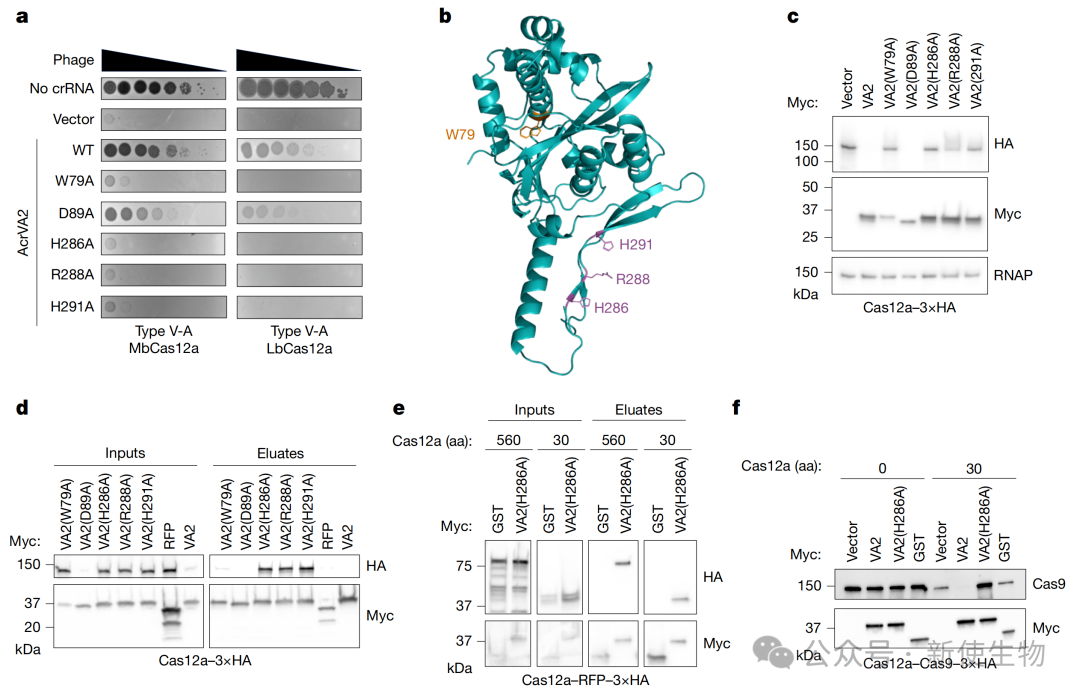
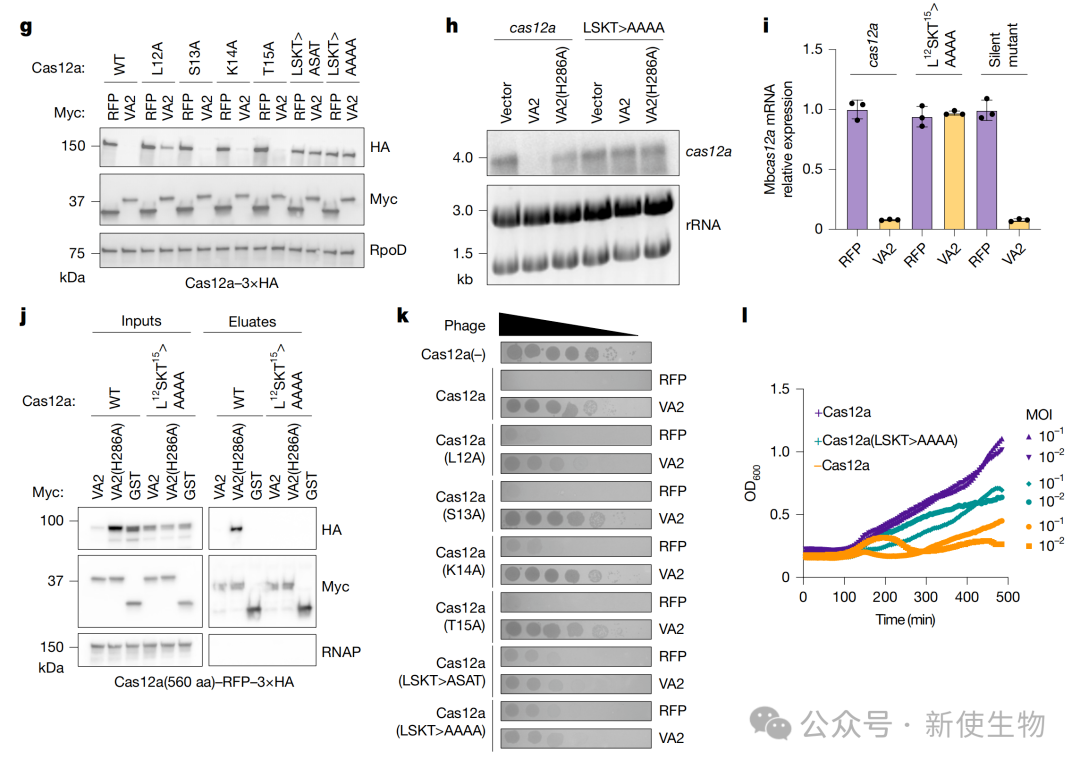
通过对AcrVA2进行定点突变,研究确定了其发挥功能的关键保守氨基酸残基。
利用免疫共沉淀、截短融合蛋白等实验,发现AcrVA2与Cas12a蛋白的N端前30个氨基酸相互作用,并且这段序列足以介导下游mRNA的降解。
进一步研究表明,Cas12a N端的LSKT保守基序对于AcrVA2的结合和抑制功能至关重要。
三、AcrVA2对cas12a mRNA的降解依赖于其翻译过程
研究人员使用翻译抑制剂四环素处理细胞或删除cas12a的起始密码子,发现这两种阻止翻译的手段都能消除AcrVA2对cas12a mRNA的降解作用。
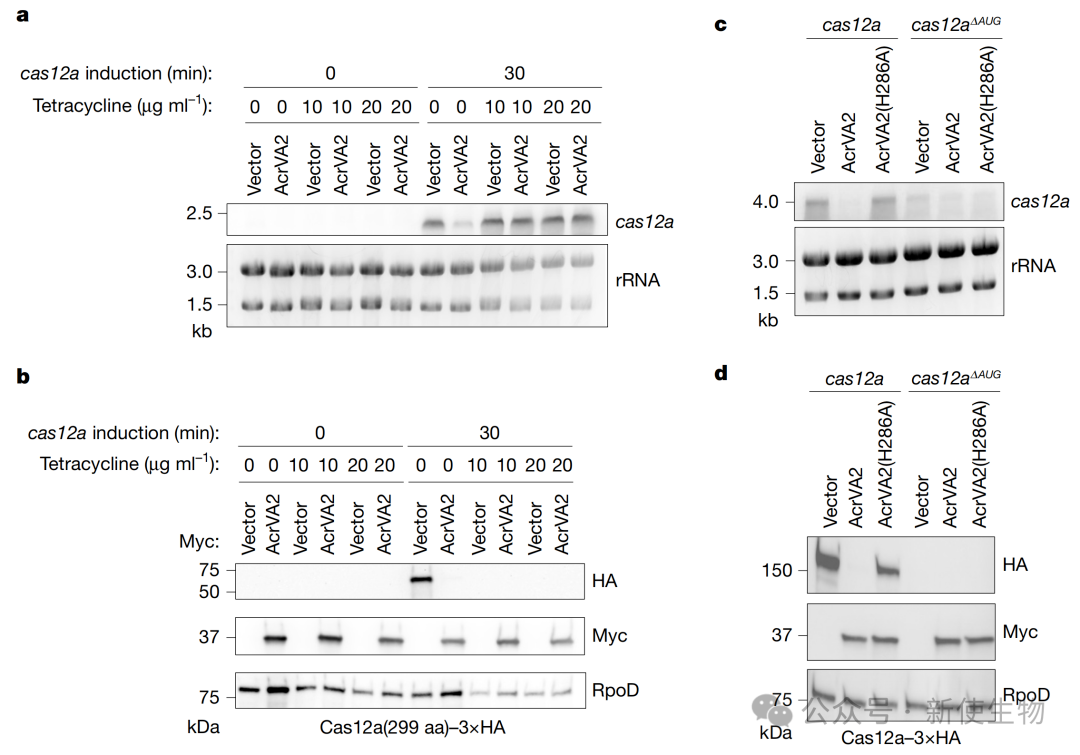
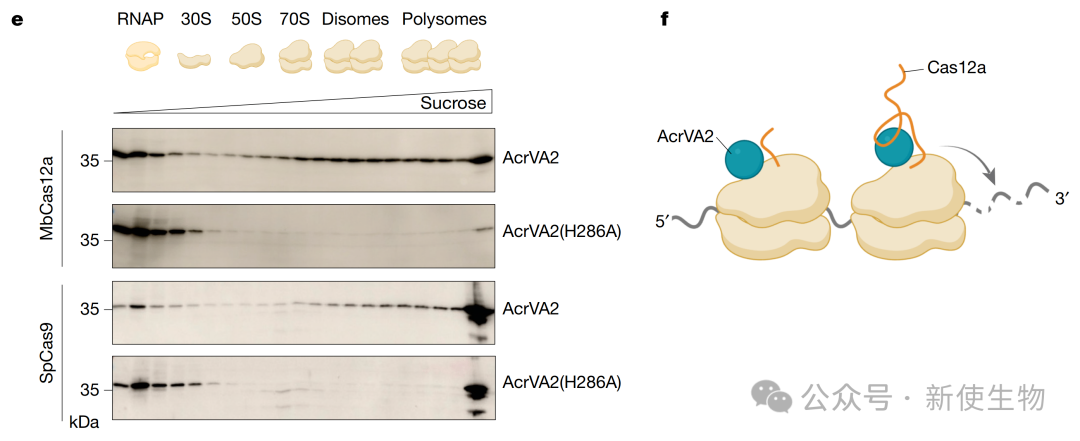
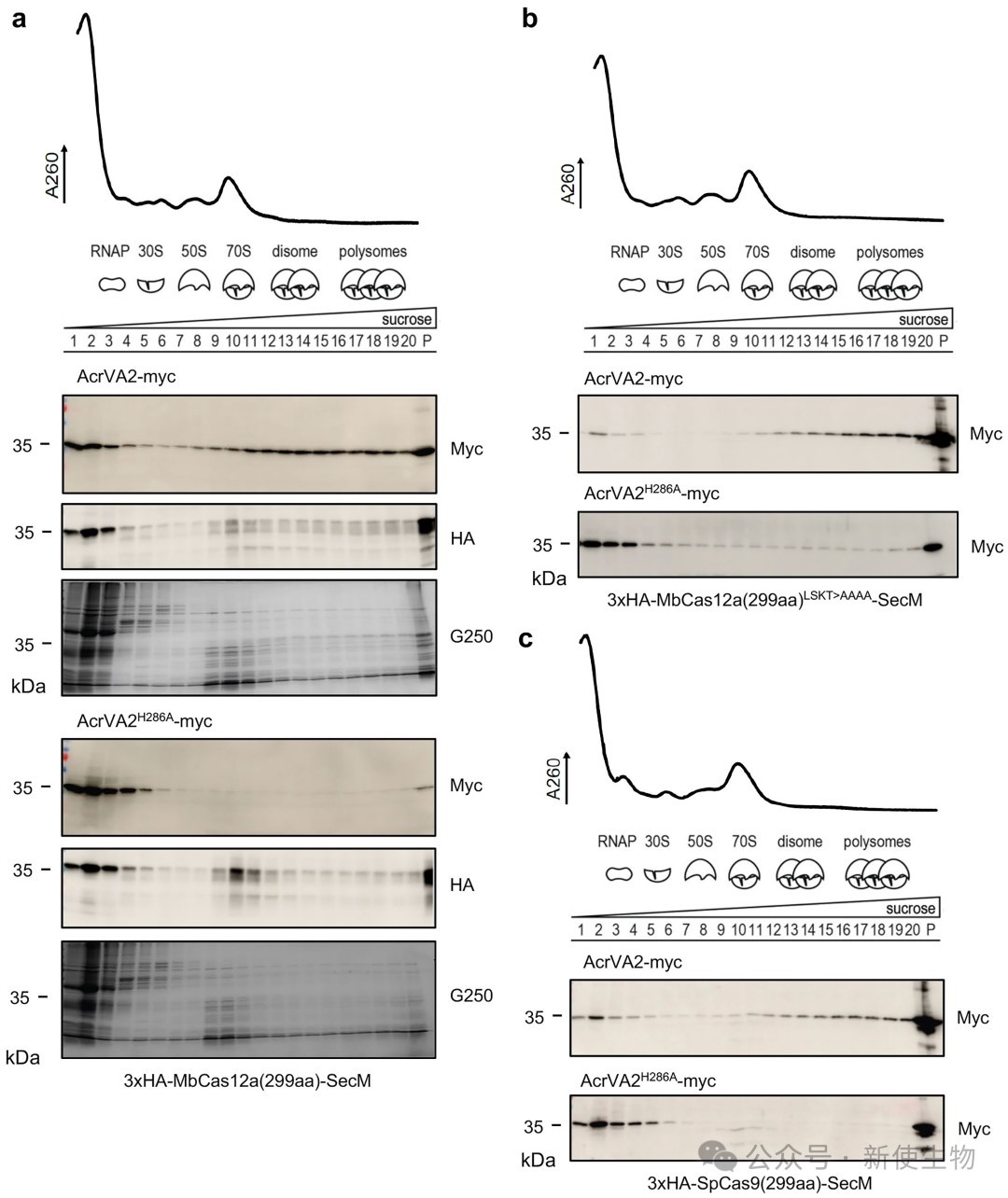
通过Polysome profiling多聚核糖体分析,作者证明了AcrVA2能够与核糖体及多聚核糖体共沉淀,这表明它在翻译活跃的核糖体上发挥作用,从而实现了共翻译降解。
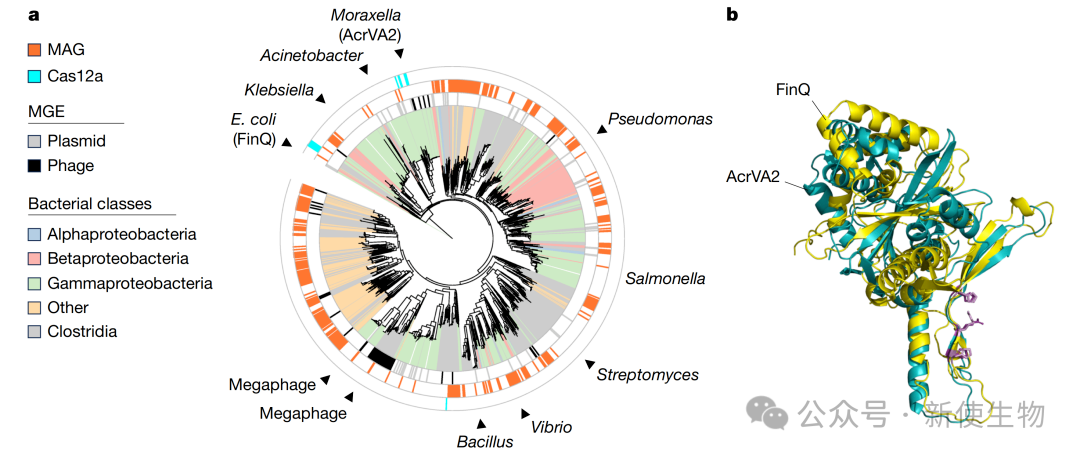
四、AcrVA2同源物广泛分布并可能具有多样的调控功能
系统发育分析显示AcrVA2同源物存在于多种细菌类的移动遗传元件上,包括FinQ等质粒蛋白。
结构模拟显示这些同源物具有保守的C端结构域,暗示这种基于肽链识别的mRNA降解机制在自然界中可能被广泛用于下调不同的目标底物。
总结
本文揭示了一种前所未有的反CRISPR蛋白AcrVA2的作用机制,它通过在翻译过程中识别并结合新生Cas12a多肽链的N端,进而触发cas12a mRNA的共翻译降解。该发现不仅深化了我们对细菌与噬菌体军备竞赛的理解,也为原核生物中的靶向基因调控提供了一种新策略和潜在工具。
点击图片查看 点击图片查看新使生物专业翻译组一站式服务平台 产品名称


 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们
