
导读
细胞通过调节蛋白质合成的各个步骤来响应环境变化和代谢需求,以确保生存。核糖体能够主动感知mRNA通道或多肽出口通道中的序列元件,从而控制基因表达。
多胺是调节细胞生长和增殖所必需的阳离子分子,其代谢酶的翻译受到严格调控。AMD1作为多胺生物合成的关键酶,其翻译效率受到多种机制的精确控制。
此前研究发现,AMD1的mRNA存在一个保守的翻译调控元件,能够根据细胞内多胺水平诱导核糖体停滞。此外,在AMD1编码序列下游发现的保守C端延伸序列也与核糖体停滞有关,但其具体的分子机制及终止失败的原因尚不明确。
2026年3月27日,美国弗吉尼亚大学Ahmad Jomaa与爱尔兰科克大学Pavel V. Baranov团队合作,在Science Advances上发表了题为“Mechanism of ribosome stalling by the AMD1 C-terminal tail arrest peptide”的研究论文。该研究解析了AMD1 C端尾部诱导核糖体停滞的结构基础,发现该多肽通过形成分子钳并插入精氨酸钩至肽基转移酶中心,从而锁定核糖体并阻断翻译终止。

文章索引
【标题】Mechanism of ribosome stalling by the AMD1 C-terminal tail arrest peptide
【发表期刊】Science Advances
【发表日期】2026年3月27日
【作者及团队】弗吉尼亚大学Ahmad Jomaa和科克大学Pavel V. Baranov团队
【IF】12.5
研究结果
一、翻译AMD1 C-末端尾部的核糖体捕获了释放因子eRF1和循环因子ABCE1
通过体外翻译实验证实,AMD1 C末端尾部序列能够在终止密码子处诱导核糖体停滞,且新生肽链与tRNA保持连接。
利用冷冻电镜技术解析了该停滞的核糖体-新生链复合物(RNC)结构,发现释放因子eRF1和再循环因子ABCE1被共同捕获在停滞的核糖体上。
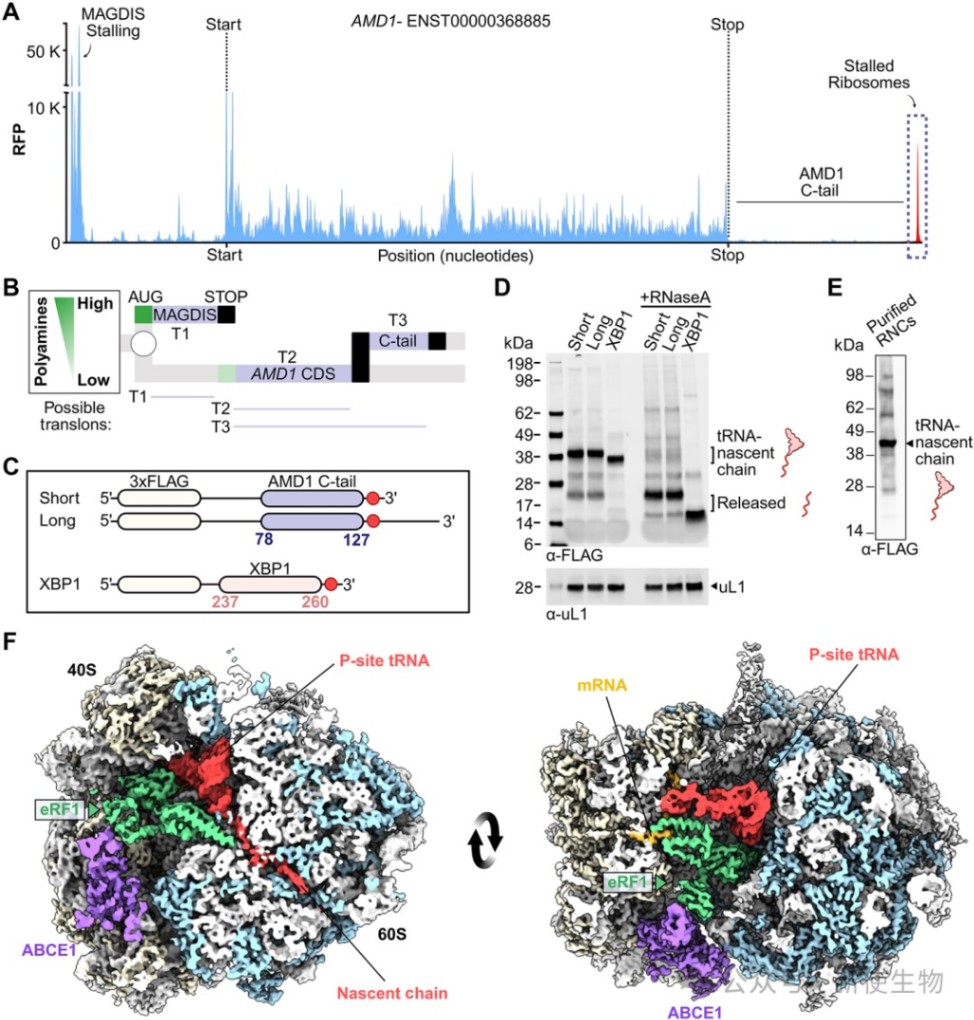
二、释放因子eRF1被锁定在一种无催化活性的构象
结构分析显示,尽管eRF1能够正确识别A位点的终止密码子,但其催化肽链释放所必需的GGQ基序却被隔离在一个非活性构象中。
该构象使其远离肽基转移酶中心约8Å,无法接触新生肽链-tRNA的酯键,因而不能催化翻译终止反应。
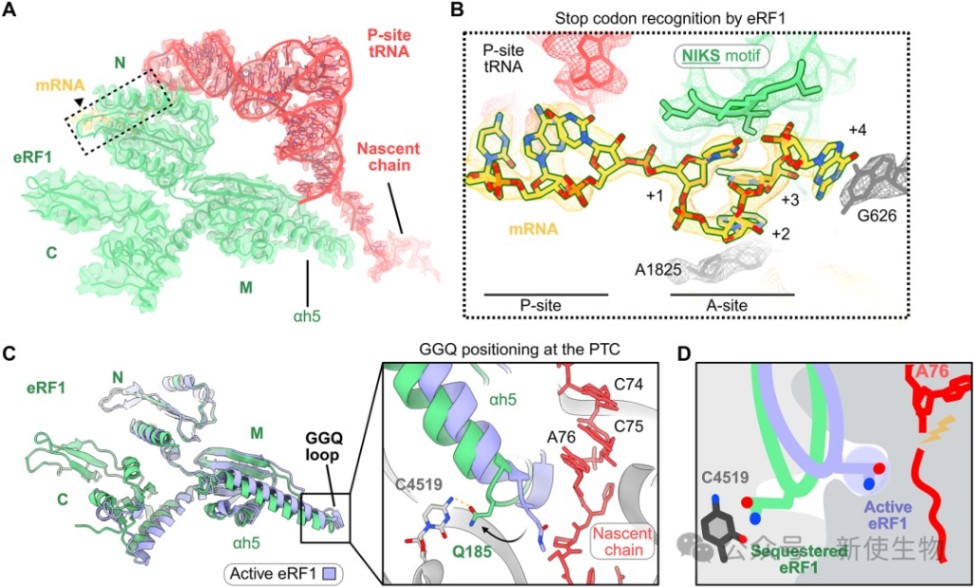
三、新生肽链中的一个保守“分子钳”是核糖体停滞的关键
研究发现,新生肽链中的三个高度保守的氨基酸(Phe124、Arg121、Lys117)形成了一个“FRK分子钳”。
该分子钳与核糖体多肽出口通道(PET)中的rRNA相互作用,使新生肽链发生独特的压缩和折叠。
定点突变实验证明,破坏这个分子钳的任何一个氨基酸都会显著减弱核糖体的停滞效率。
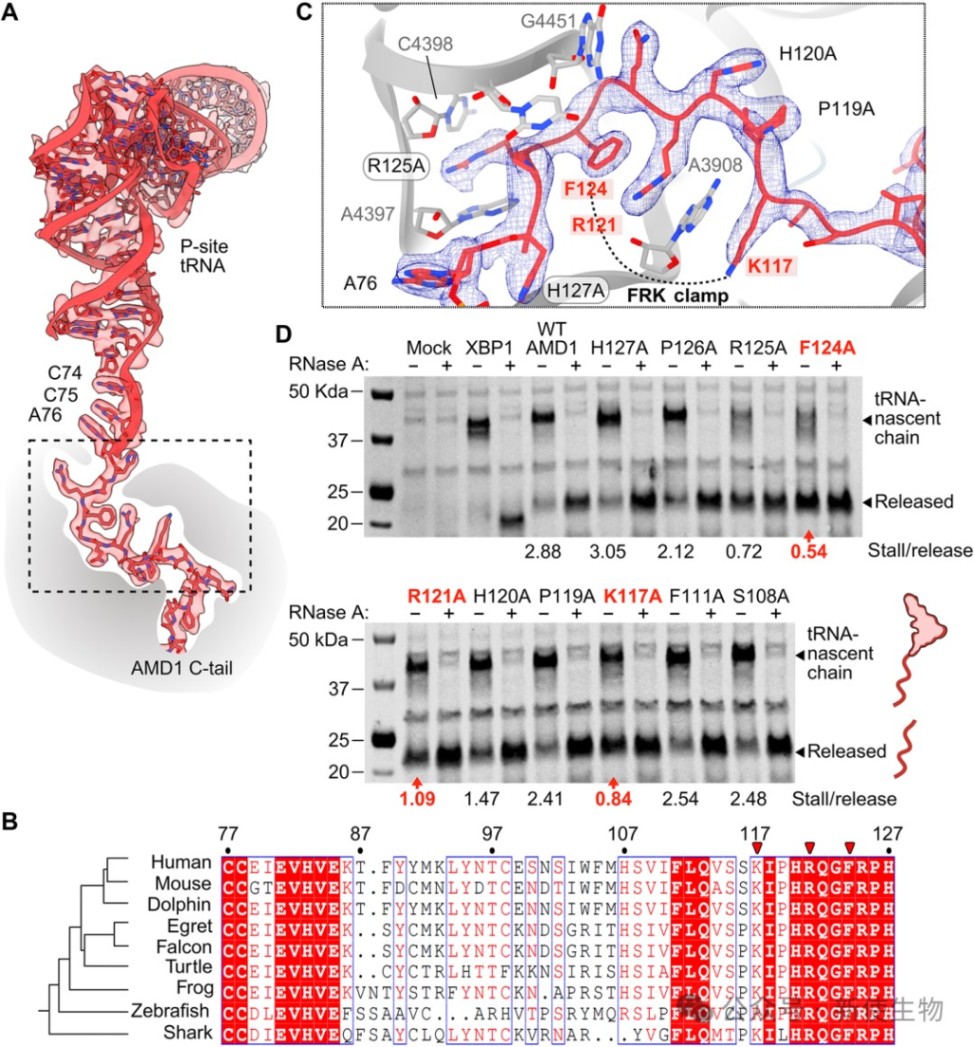
四、精氨酸钩插入PTC是阻断翻译终止的直接原因
该分子钳的形成能够精确地将一个高度保守的精氨酸残基(Arg125)以“钩子”的形式插入到核糖体的肽基转移酶中心(PTC)。
这个精氨酸钩直接占据了eRF1的GGQ基序进入PTC催化位点所必需的空间,通过空间位阻效应阻止了翻译终止的发生。
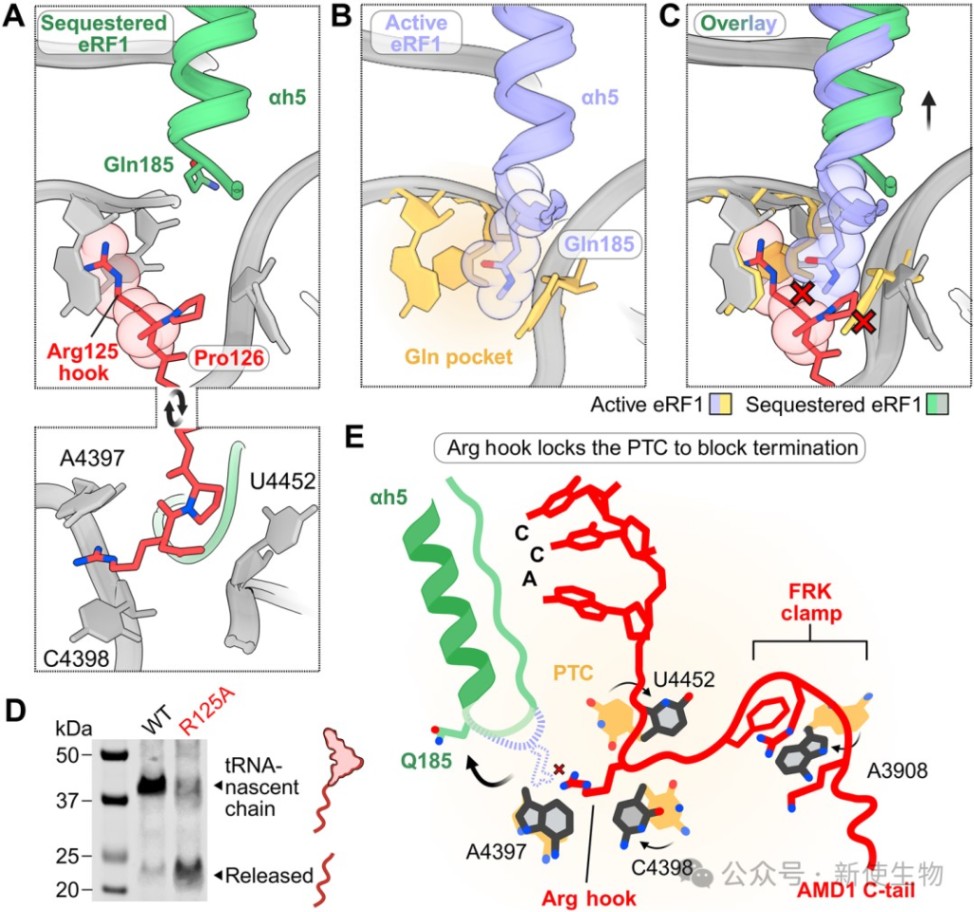
五、在其他基因中也发现了类似的终止密码子通读后停滞的现象
通过对已发表的Ribo-seq核糖体印迹分析数据进行整合分析,研究人员在EEF1A2、MAPK10和SACM1L等多个其他人类基因中,也发现了在终止密码子通读后,核糖体在3' UTR特定位置停滞的模式。
这表明由新生肽链介导的翻译调控机制可能比之前预想的更为普遍。
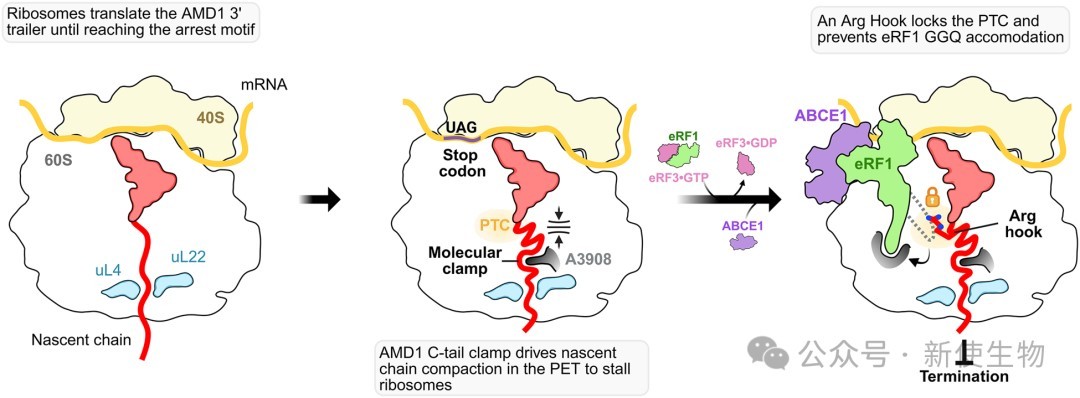
总结
本研究通过高分辨率结构揭示了AMD1 C末端尾部新生肽介导核糖体停滞并抑制翻译终止的分子机制,阐明了一个由“分子钳”和“精氨酸钩”协同作用的精密调控模型。这一发现不仅为理解翻译过程中的顺式调控元件提供了新的范例,还暗示了这种终止密码子通读后再停滞的调控策略可能在生物体中具有更广泛的功能意义。
点击图片查看 点击图片查看新使生物专业翻译组一站式服务平台 产品名称


 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们
