
导读
代谢功能障碍相关脂肪性肝病(MASLD)已成为全球范围内极其普遍的慢性肝病,影响着近20亿人的健康。该疾病包含从单纯性肝脂肪变性(SLD)到严重的代谢功能障碍相关脂肪性肝炎(MASH)的连续演变过程。
长期高脂肪饮食摄入诱导的代谢压力是推动MASLD发生及其向肝硬化和肝细胞癌进展的关键驱动力。这种持续的代谢压力会诱发肝细胞产生慢性内质网应激,并进一步激活未折叠蛋白反应以试图维持稳态。
尽管学术界对急性内质网应激下的转录响应已有深入研究,但肝细胞如何通过转录后机制适配慢性内质网应激仍不明确。深入探索慢性压力下的基因表达重编程机制,对于寻找预防肝脏疾病恶化及肿瘤发生的治疗新策略具有重要意义。
2026年4月3日,西班牙巴塞罗那生物医学研究所Raul Mendez、Mercedes Fernandez与Patrick Aloy团队合作,在Science Advances上发表了题为“Posttranscriptional reprogramming controls MASLD progression through chronic ER stress adaptation”的研究论文。研究发现CPEB4介导的转录后重编程是肝细胞适配慢性内质网应激的核心机制,它通过延长特定mRNA的多聚腺苷酸尾来激活翻译。
文章索引
【标题】Posttranscriptional reprogramming controls MASLD progression through chronic ER stress adaptation
【发表期刊】Science Advances
【发表日期】2026年4月3日
【作者及团队】 西班牙巴塞罗那生物医学研究所Raul Mendez、Mercedes Fernandez与Patrick Aloy团队
【IF】12.5
研究结果
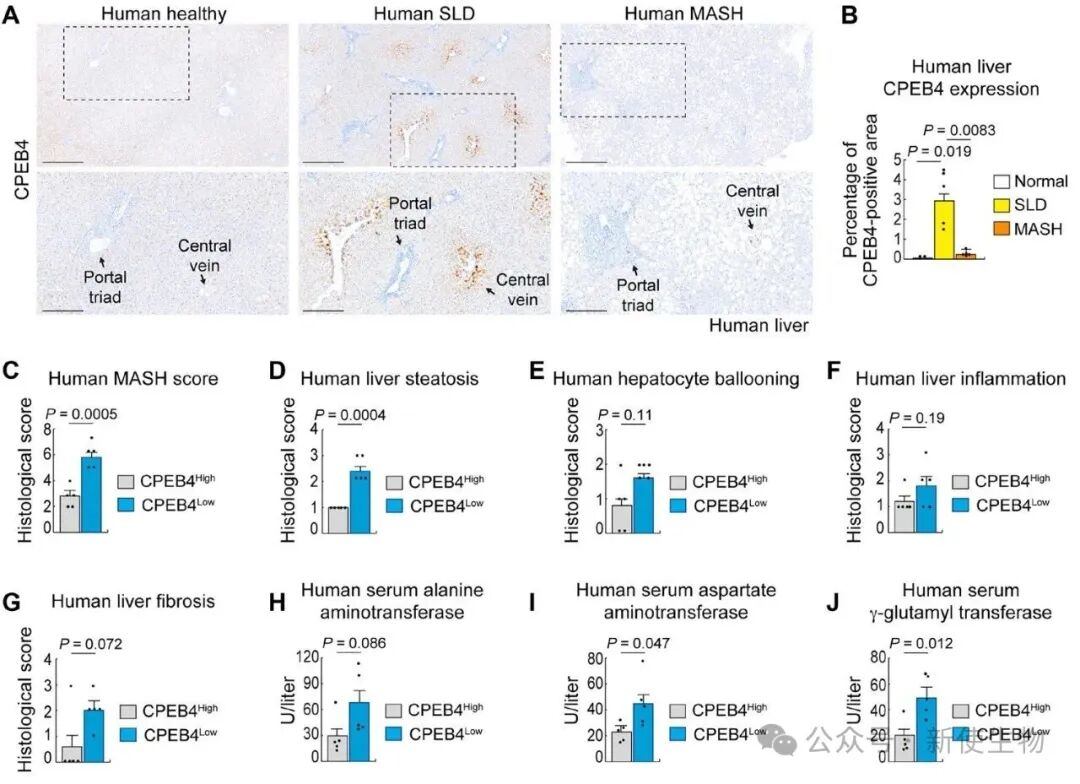
一、CPEB4水平与人类MASH严重程度呈负相关
通过对肥胖患者肝脏样本的免疫组化分析,研究发现虽然早期脂肪变性(SLD)阶段CPEB4表达升高,但随疾病进展至MASH阶段,CPEB4显著下降达92%。
低水平的CPEB4与肝功能受损指标及严重的肝组织病理损伤密切相关。
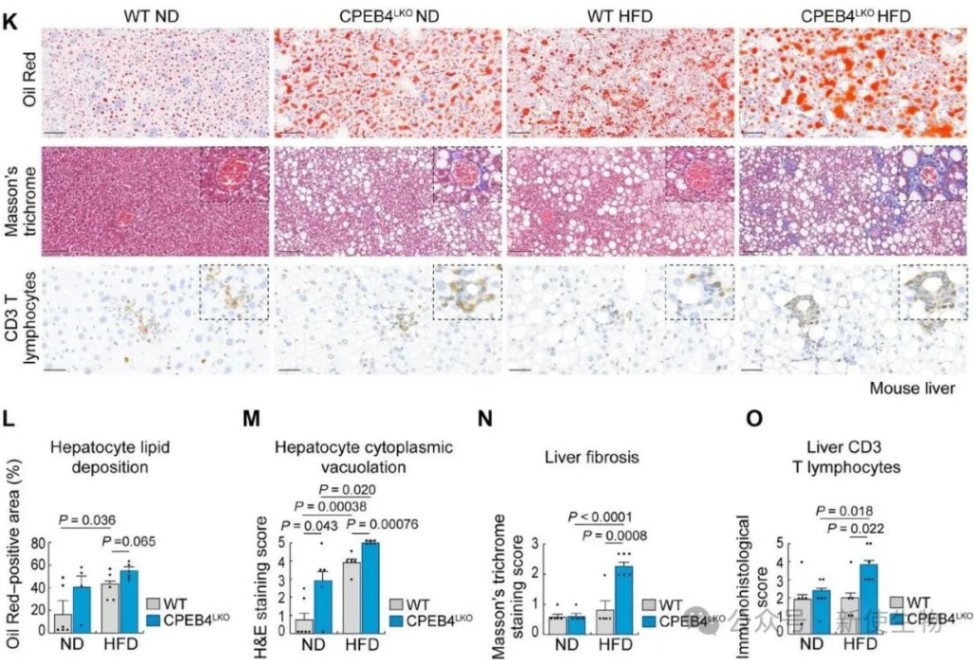
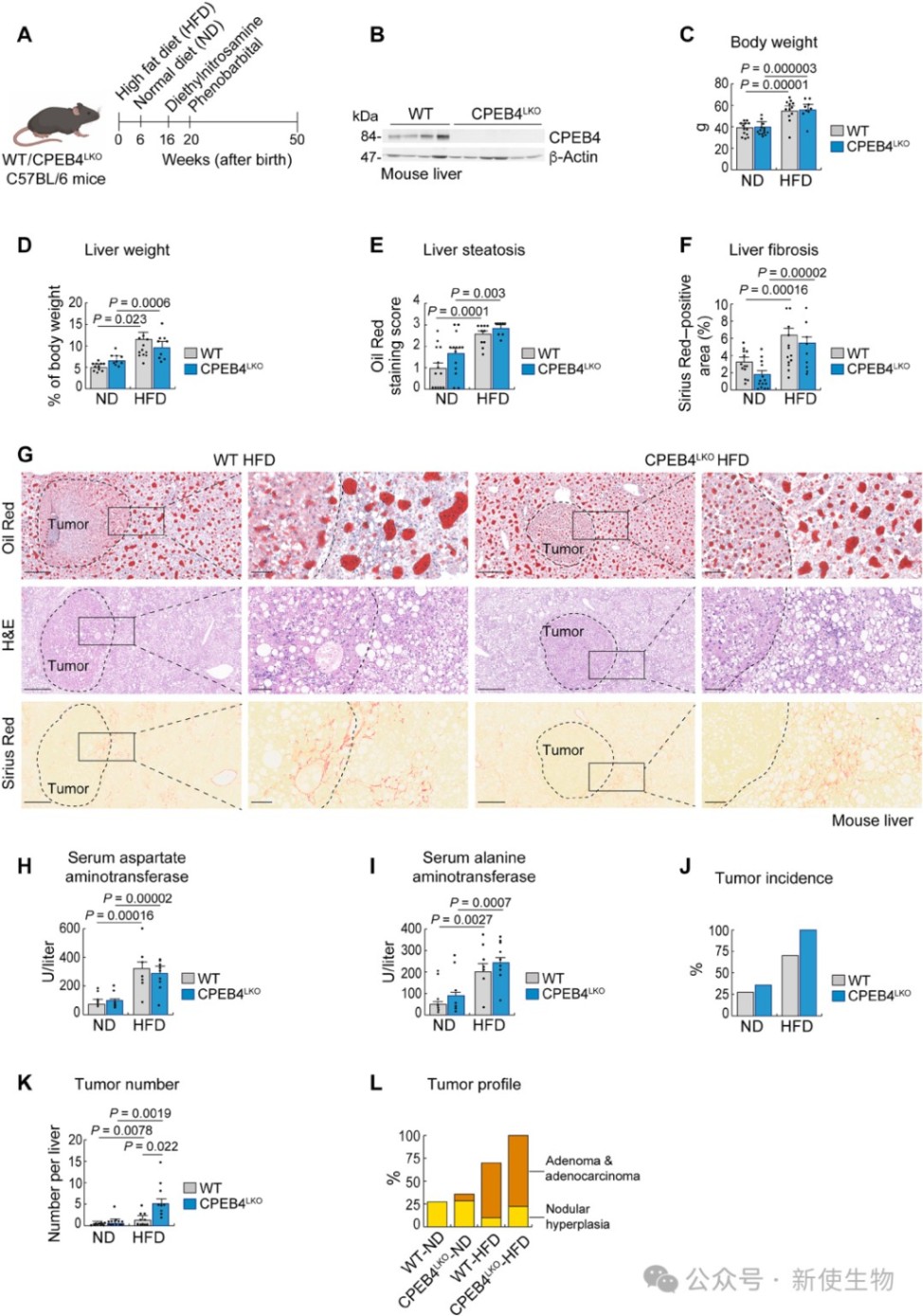
二、敲除CPEB4会显著加剧小鼠MASLD的病理演变
研究者构建了肝细胞特异性敲除CPEB4的小鼠模型,发现高脂饮食(HFD)喂养下,缺失CPEB4的小鼠比野生型小鼠表现出更严重的肝脂肪变性、纤维化和炎症浸润。
实验证明CPEB4通过介导慢性内质网应激适配保护肝细胞,其缺失会导致肝损伤加重。
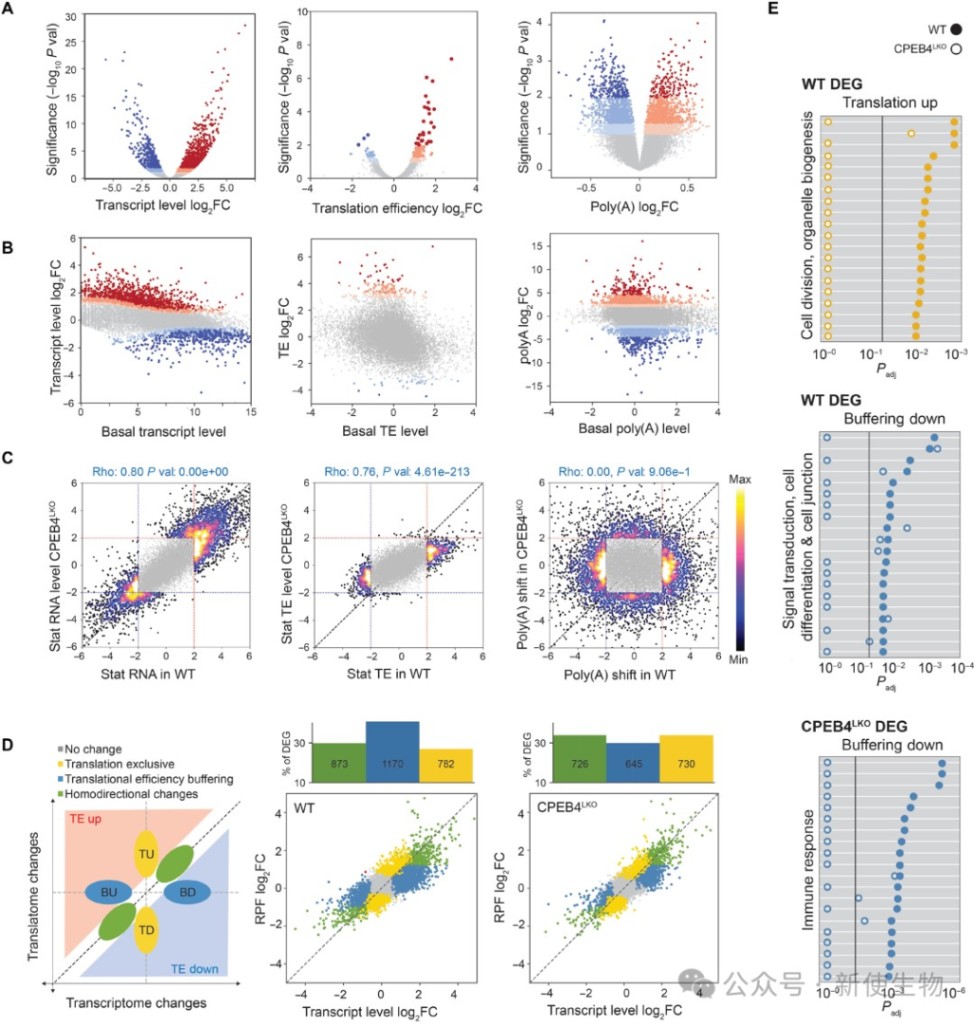
三、高脂饮食诱导的肝脏基因表达变化主要受翻译水平驱动
Ribo-seq核糖体印迹分析发现,HFD诱导的基因表达改变中约70%涉及翻译效率的调整。
这种调控在CPEB4缺失后发生显著扰乱,表明CPEB4是控制慢性代谢压力下翻译稳态的关键枢纽。
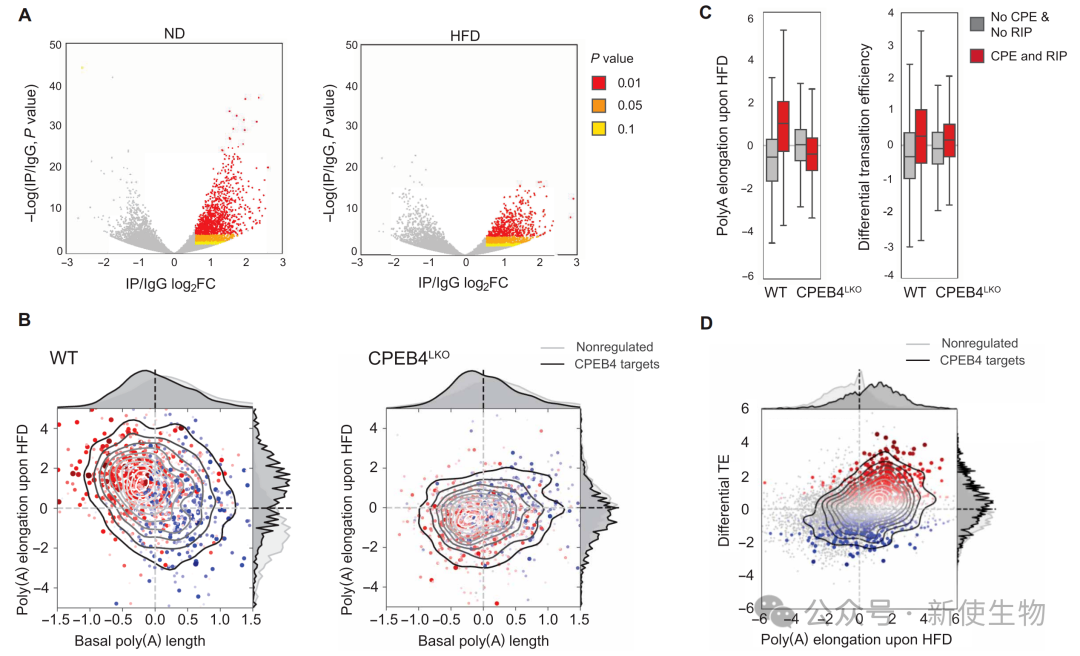
四、CPEB4通过延长poly(A)尾选择性激活细胞周期和免疫相关基因的翻译
通过poly(A)尾分析和RNA免疫沉淀(RIP)技术,研究人员发现CPEB4是HFD诱导的mRNA poly(A)尾长度变化的关键调控者。
在野生型小鼠中,HFD会诱导CPEB4靶向的mRNA发生poly(A)尾延长,并伴随翻译效率的提高,而这一现象在CPEB4敲除小鼠中完全消失。
五、CPEB4的调控特异性取决于mRNA上的顺式元件组合及密码子偏好性
研究揭示了一种由多种顺式作用元件构成的协同调控模式,即含有平衡数量CPE和ARE基序且密码子优化度较低的mRNA最易受CPEB4调控。
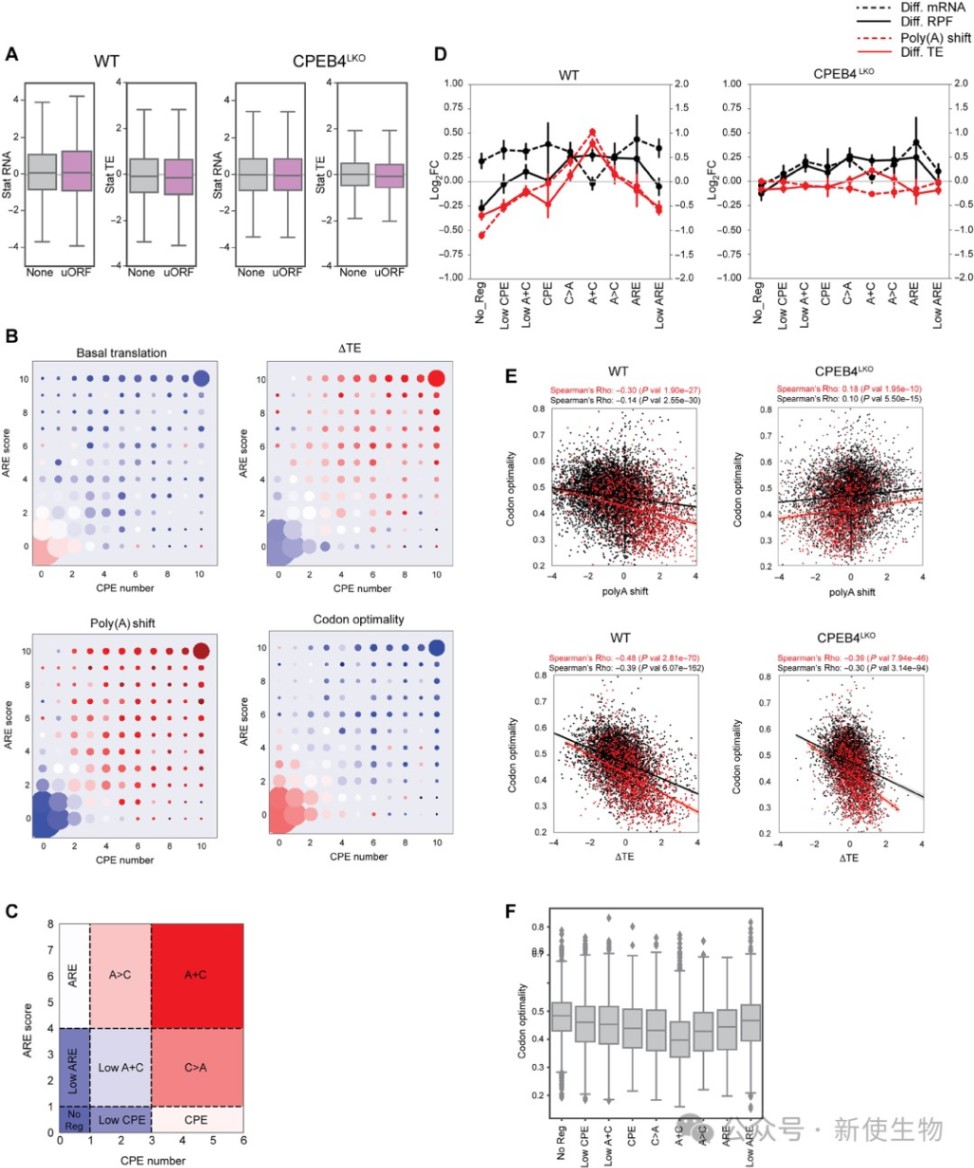
这种机制允许细胞根据应激程度,在mRNA的去腺苷酸化与多聚腺苷酸化之间寻找平衡点,实现蛋白质合成的精准波动。
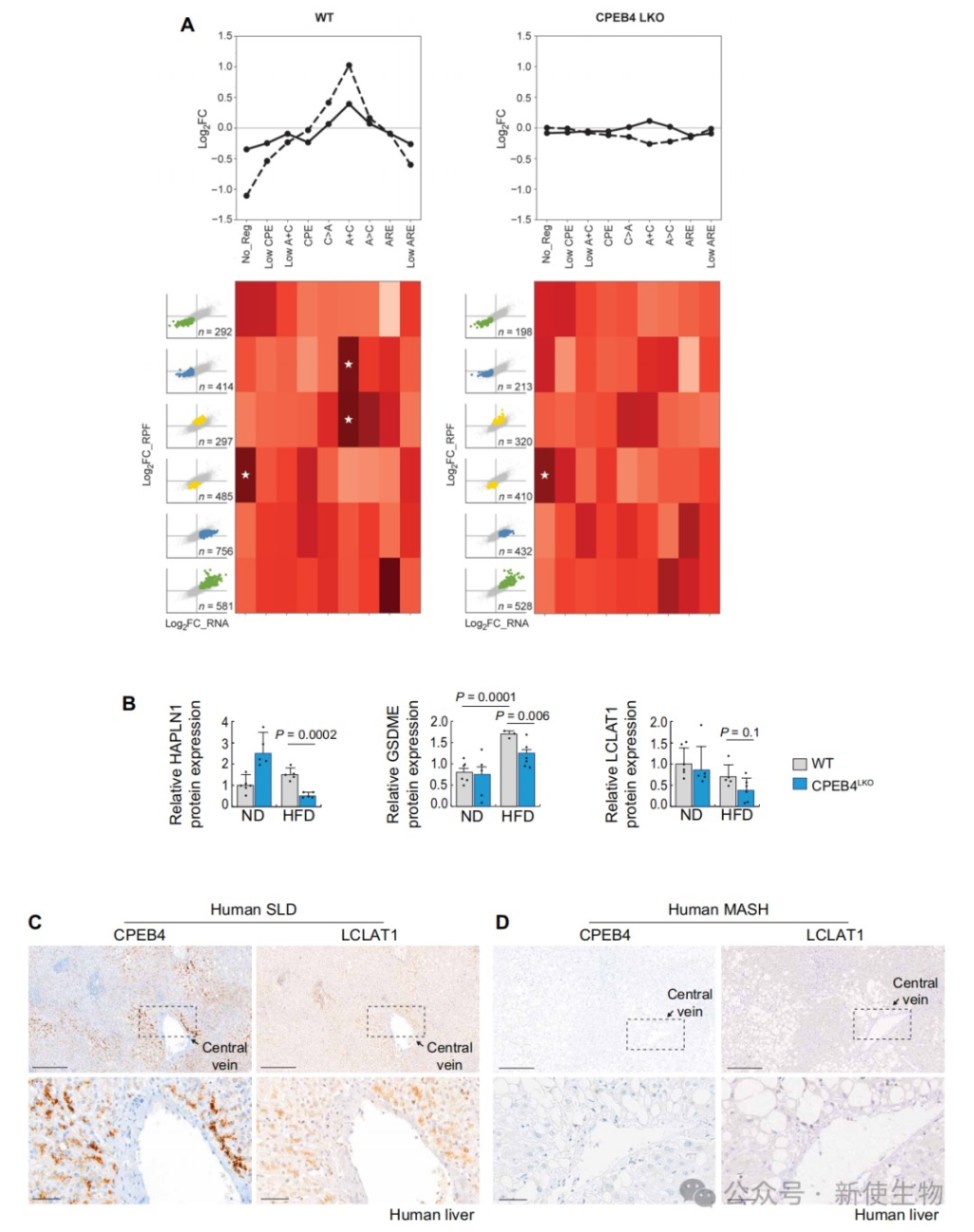
六、缺失CPEB4会显著提高MASLD向肝癌转化的风险
在长期高脂饮食配合致癌剂的模型中,CPEB4敲除小鼠的肿瘤发生率和肿瘤数量显著高于野生型,且肿瘤更具侵袭性。
体外实验显示CPEB4缺失的肝癌细胞具有更强的迁移和克隆形成能力,确证了CPEB4在肝脏中的抑癌作用。
总结
本研究通过多组学整合分析,构建了CPEB4在调控肝细胞应对慢性内质网应激中的核心地位,揭示了其作为转录后重编程调控枢纽在MASLD进展中的关键作用。通过维持翻译稳态,CPEB4不仅保护肝脏免受代谢应激损害,还作为肿瘤抑制因子阻断了从脂肪性肝炎到肝癌的恶化路径。
点击图片查看 点击图片查看新使生物专业翻译组一站式服务平台 产品名称


 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们
