
导读
血红素调节抑制剂(HRI)曾被长期认为仅限于调节红细胞中血红素与珠蛋白的合成平衡。然而,随着研究的深入,这一经典的eIF2α激酶已被重新定义为一个多维度的细胞稳态传感器。
它不仅在应对线粒体应激、细胞质蛋白折叠压力中发挥核心作用,还深度参与了先天免疫、神经生物学稳态及肿瘤抑制过程。
2026年4月15日,哈佛医学院Bertal H. Aktas团队在Trends in Cell Biology上发表了一篇题为“The heme-regulated inhibitor eIF2α kinase: a multifaceted sensor and drug target”的综述文章。该文系统梳理了HRI在生理与病理条件下的多重角色,详细解析了新发现的OMA1-DELE1-HRI轴如何在分子水平上介导线粒体综合应激反应(ISR),并重点讨论了HRI作为新型药理学靶标在治疗血液病、代谢性疾病及癌症中的巨大潜力。

综述整理
一、HRI在细胞器未折叠蛋白反应中的核心机制
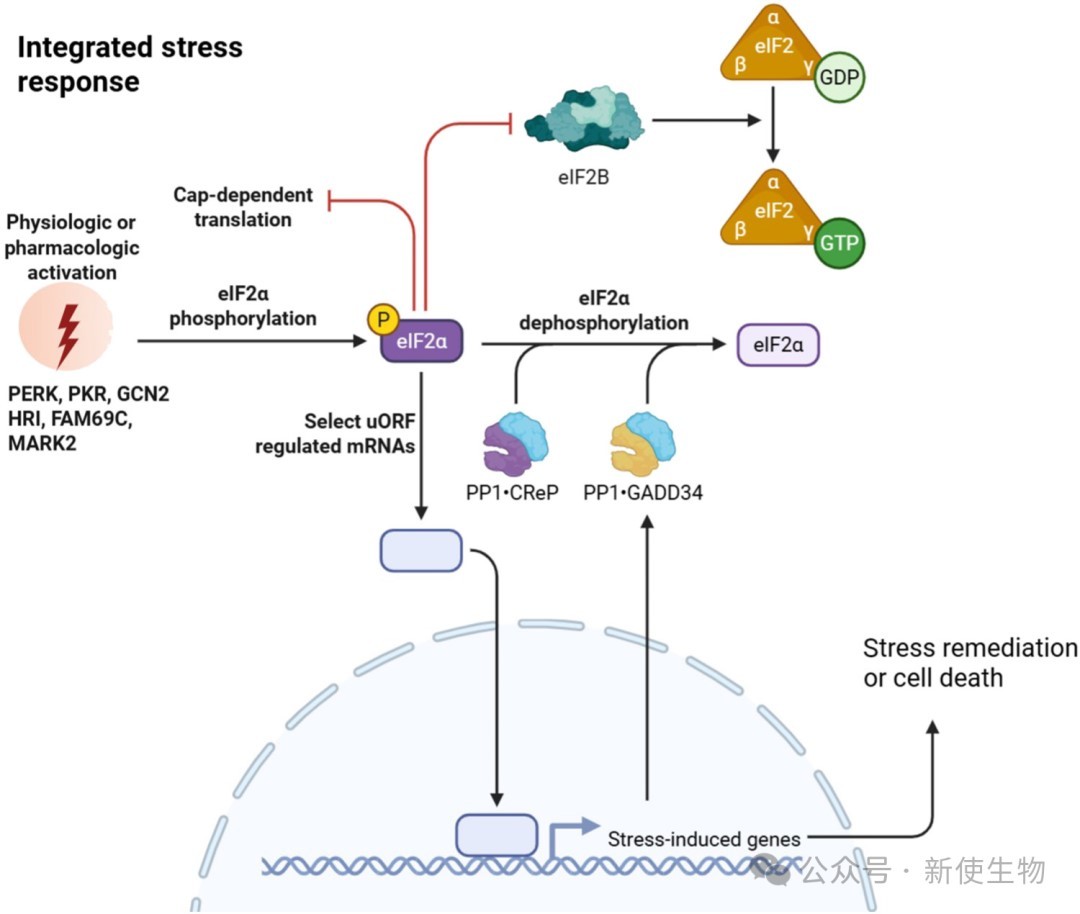
1.1)介导线粒体应激反应(ISRmito)
HRI不仅响应游离胞浆蛋白应激,更是线粒体应激的关键传感器。
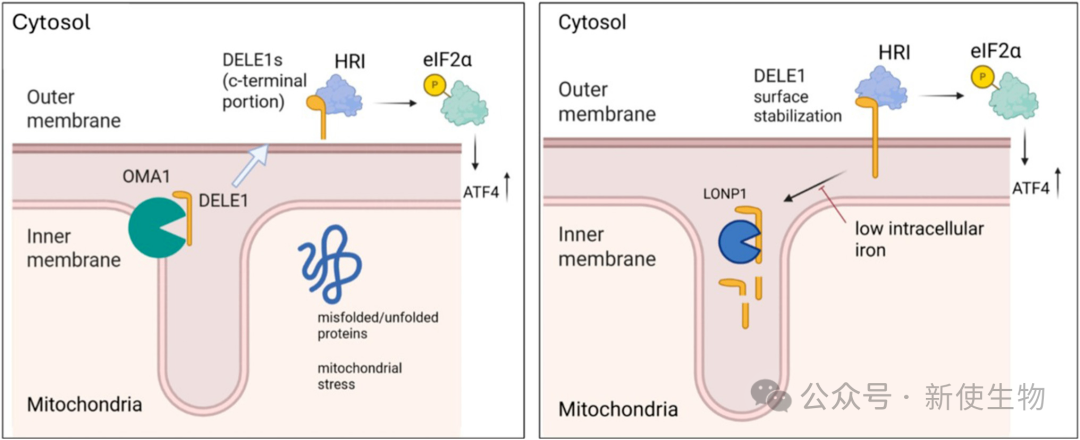
当线粒体受损时,其内膜蛋白酶OMA1被激活,裂解DELE1蛋白产生截短体DELE1s。
DELE1s随后进入胞浆结合并激活HRI,引发eIF2α磷酸化并上调ATF4和CHOP等下游因子,启动线粒体保护机制。
1.2)负调控mTORC1信号通路
在线粒体应激网络中,HRI发挥着代谢重塑的关键作用。
HRI依赖性的ATF4激活会进一步上调Sestrin2和Redd1基因的表达。
这两个靶标蛋白能强烈抑制mTORC1信号通路的活化,从而抑制全局蛋白质合成,辅助细胞度过应激难关。
二、HRI在红细胞生成与血液病理中的作用
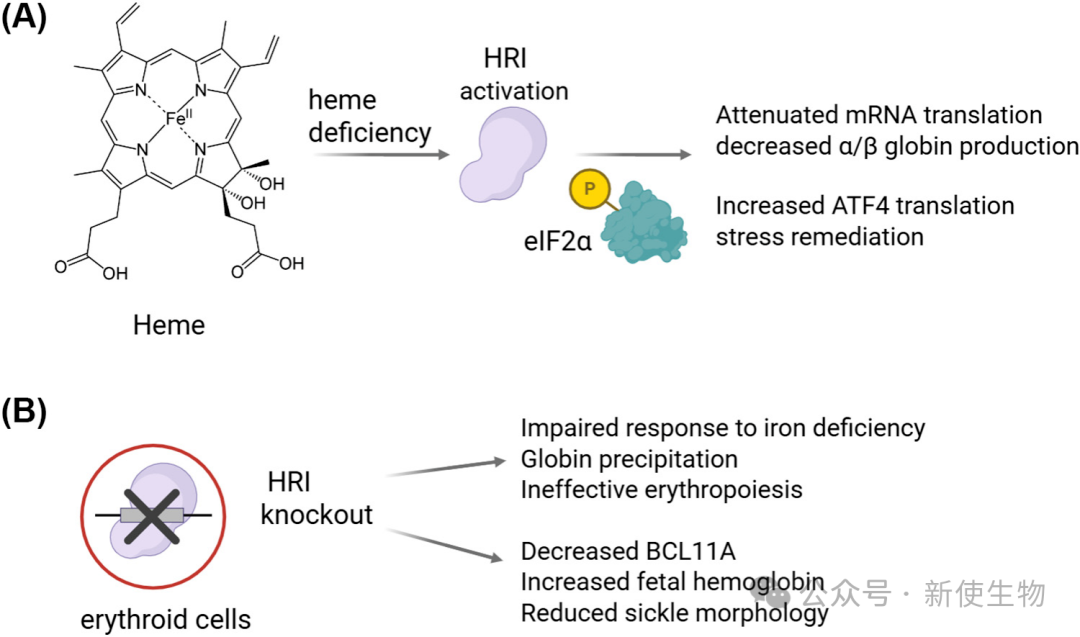
2.1)感知血红素平衡并调控珠蛋白翻译
HRI在红系细胞中呈高表达,作为核心血红素传感器运作。
当体内缺铁或血红素匮乏时,HRI迅速自磷酸化激活,抑制珠蛋白mRNA的翻译,避免有毒的游离珠蛋白沉淀积累,同时上调ATF4以减轻氧化应激,维持红系祖细胞存活。
2.2)临床干预红系疾病的双刃剑特征
基因敲除HRI会导致小鼠在缺铁状态下发生严重的无效红细胞生成。
然而在临床前研究中,敲除镰状细胞贫血患者细胞中的HRI,却能通过下调阻遏蛋白BCL11A来促进胎儿血红蛋白产生,显著逆转红细胞的镰刀化形态,提示其作为血液病干预靶点具有极高潜力。
三、HRI在先天免疫与神经生物学中的多维调控
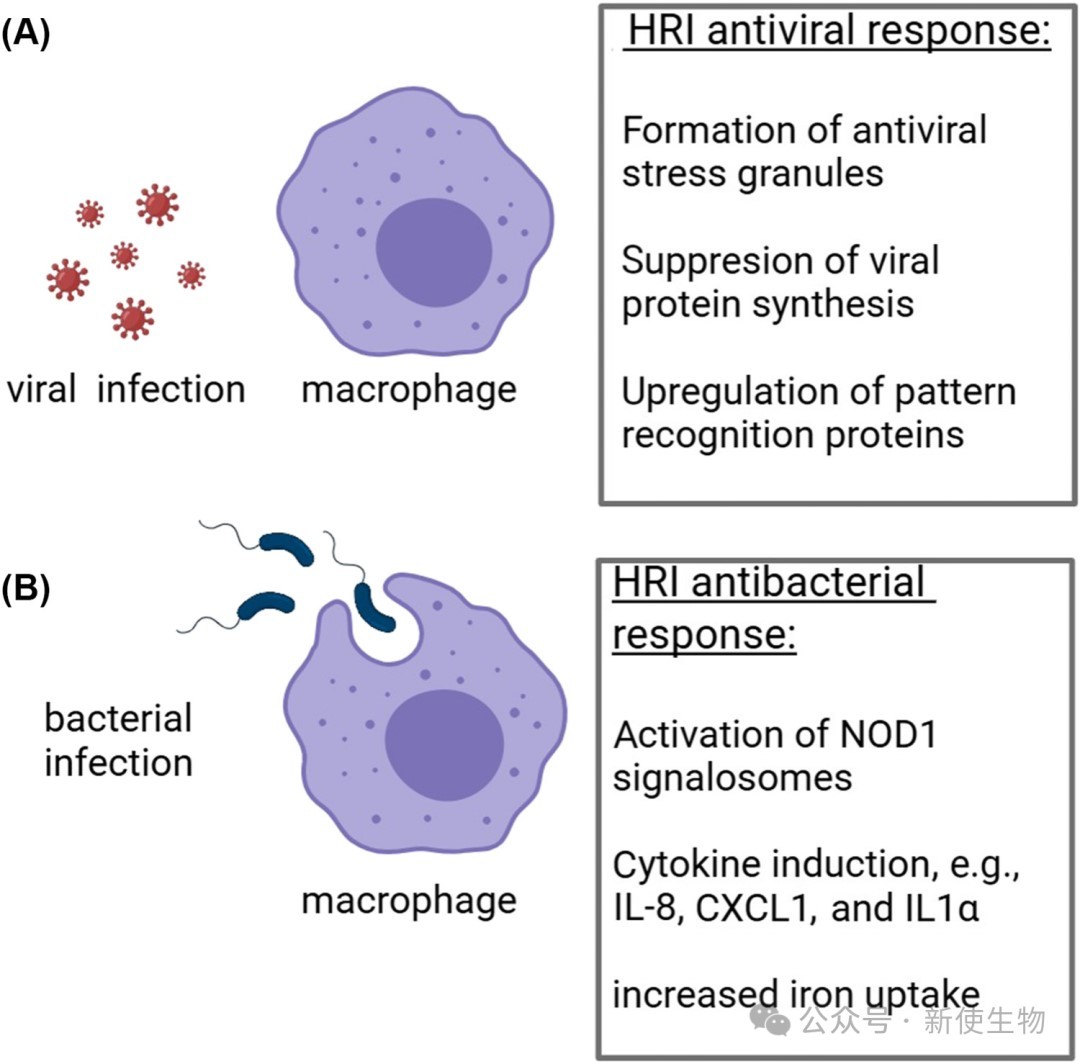
3.1)对抗病原体感染的免疫防线
HRI独立于经典抗病毒激酶PKR,通过促成抗病毒应激颗粒(SGs)阻断病毒蛋白合成。
在面对耶尔森菌或李斯特菌等细菌感染时,HRI能激活NOD1信号小体,驱动炎性细胞因子(如IL-8、IL-1α)分泌,并促使巨噬细胞扣留血清铁以限制病原体增殖。
3.2)调控突触可塑性与神经退行性病变
在海马体中,HRI受一氧化氮(NO)激活并促进BACE1翻译,这对突触生长和记忆巩固至关重要,但过度表达的BACE1也会加速阿尔茨海默病(AD)中淀粉样斑块形成。
同时,相关激酶FAM69C与HRI协同,在小胶质细胞中限制NLRP3炎症小体活化,发挥关键的神经保护作用。
四、靶向HRI在肿瘤及心血管疾病中的临床前景
4.1)作为潜在的肿瘤抑制因子与增敏靶点
HRI介导的翻译抑制常被癌细胞视为生存威胁,部分上皮性肿瘤通过UBKU泛素连接酶复合体降解HRI以逃避凋亡。
研究表明,恢复HRI表达或使用小分子激活HRI,可显著抑制G1周期蛋白等促癌因子翻译,并在多发性骨髓瘤和白血病中与现有靶向药产生协同致死效应。
4.2)线粒体心肌病的代偿保护机制
在伴有线粒体功能障碍的胎儿及成人心肌病中,HRI介导的应激反应是维持心肌细胞存活的最后防线。
动物模型显示,敲除HRI会显著恶化心室表型并大幅缩短寿命,这表明激活HRI激酶是延缓线粒体缺陷型心衰的有效干预策略。
4.3)HRI特异性化学调节剂的开发
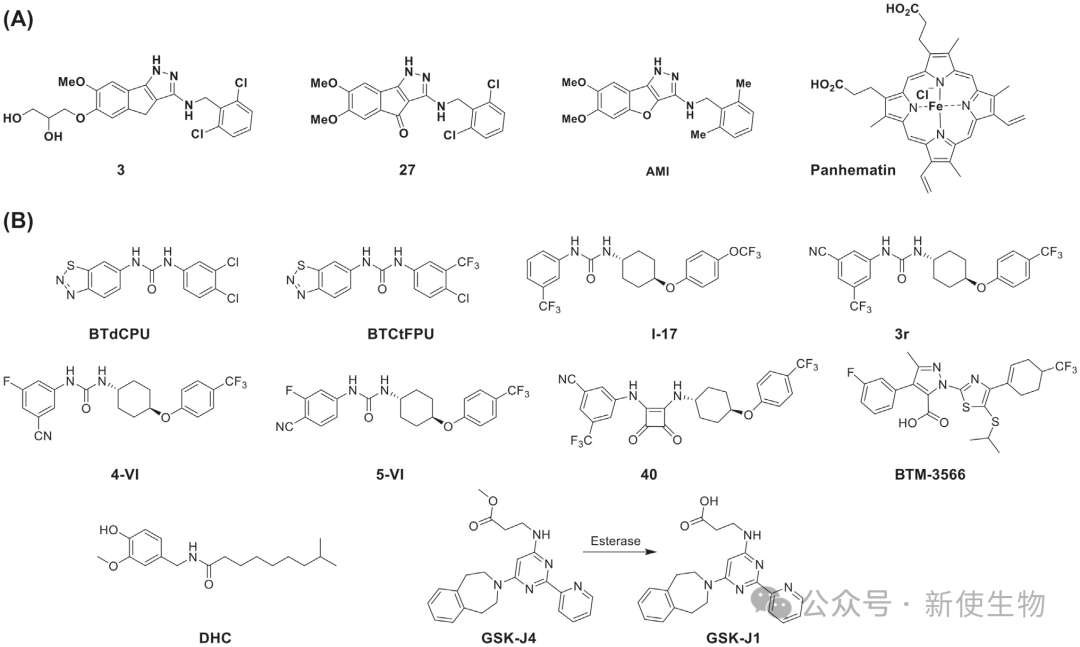
目前学界已开发出以indeno[1,2-c]pyrazoles为代表的HRI抑制剂,以及以N,N'-二芳基脲类(如BTdCPU、cHAU)为代表的HRI激活剂。
这些非血红素类小分子药物在抑制乳腺癌增殖、改善肝脏脂肪变性以及抗寄生虫感染的体内外模型中,均展现出了卓越的药效与良好的治疗窗口。
总结与展望
HRI的研究已从一个局限于红系细胞的血红素传感器,扩展为一个在先天性免疫、神经生物学、代谢和线粒体健康中发挥关键作用的多功能eIF2α激酶。未来的研究需要集中解析HRI的精细调控网络和三维结构,这将为开发靶向HRI的精准疗法,用于治疗从血液病到癌症和神经退行性疾病等多种人类顽疾提供关键依据。
点击图片查看 点击图片查看新使生物专业翻译组一站式服务平台 产品名称


 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们
