
导读
造血干细胞(HSC)是研究干细胞维持的经典体系,它在整个生命周期中持续补充循环血细胞。HSC的自我更新与分化平衡对维持造血稳态至关重要,这一过程由一个精确调控的基因表达程序所控制。
已有研究揭示了HSC必需基因的表达程序受到表观遗传修饰、转录因子和蛋白质降解等多种机制的调控。在这些调控之上,RNA水平的调控也参与并协调着HSC必需基因的表达。
例如,RNA调控因子METTL3和SRSF1分别通过m⁶A修饰和可变剪接影响HSC的功能。尽管RNA调控因子在HSC中的作用已有报道,但对转录本命运决定的系统性特征分析仍有待深入。
2026年5月4日,中国医学科学院基础医学研究所王芳、余佳团队与浙江大学钱鹏旭团队合作,在Nature Cell Biology上发表了题为“NAT10 maintains stem cell homeostasis by mitigating mRNA decay through an ac⁴C-independent mechanism”的论文。本研究揭示了HSC核心基因具有富含ARE基序的超长3' UTR特征,并发现NAT10通过结合这些基序发挥关键作用。

文章索引
【标题】NAT10 maintains stem cell homeostasis by mitigating mRNA decay through an ac⁴C-independent mechanism
【发表期刊】Nature Cell Biology
【发表日期】2026年5月4日
【作者及团队】中国医学科学院基础医学研究所王芳、余佳团队和浙江大学钱鹏旭团队
【IF】19.1
研究结果
一、HSC核心基因的3' UTR富含ARE元素且受NAT10调控
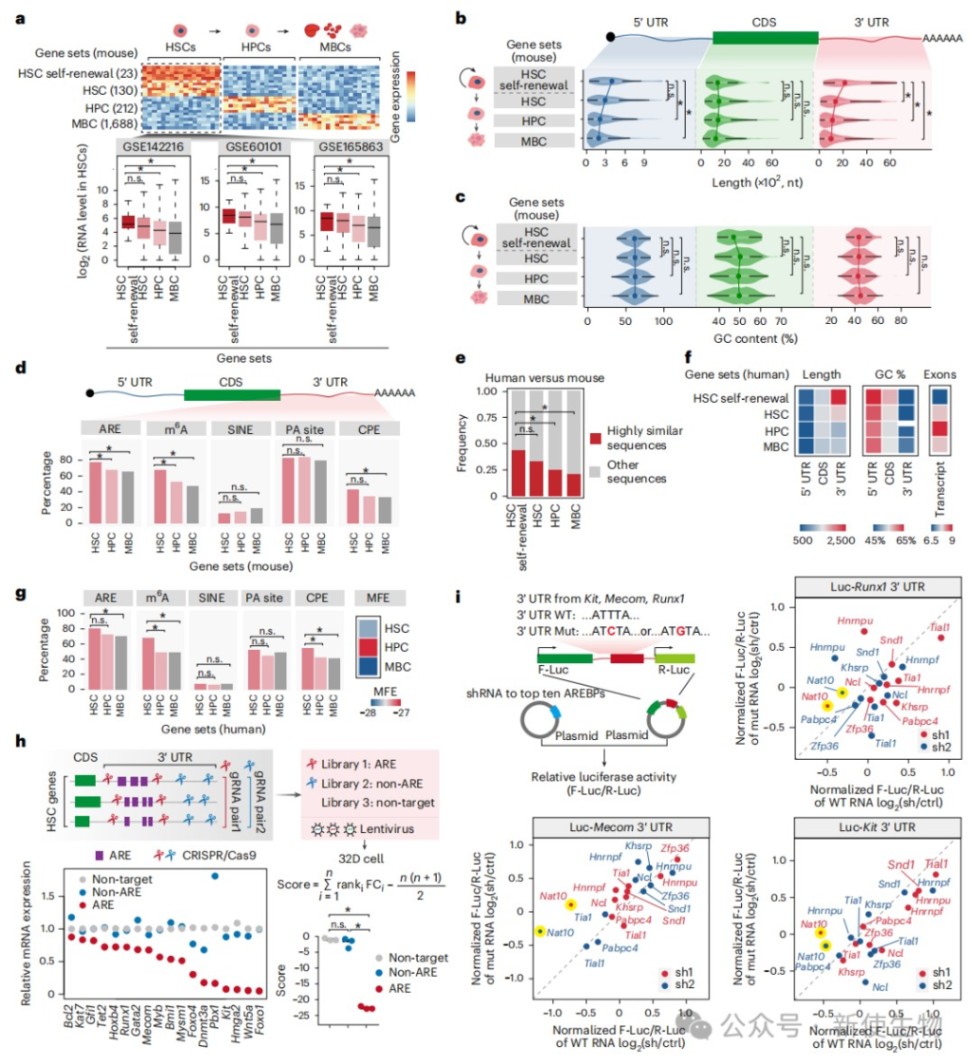
研究人员通过系统分析人类和小鼠HSC核心基因的转录本特征,发现其3' UTR显著延长且特异性富含AU富集元件(AREs)。
利用CRISPR-Cas9介导的库筛选和荧光素酶报告实验,证实这些AREs对HSC基因表达至关重要,并从中鉴定出NAT10是结合这些元件的关键调节蛋白。
二、Nat10缺失会严重损害HSC的自我更新和长期重建能力
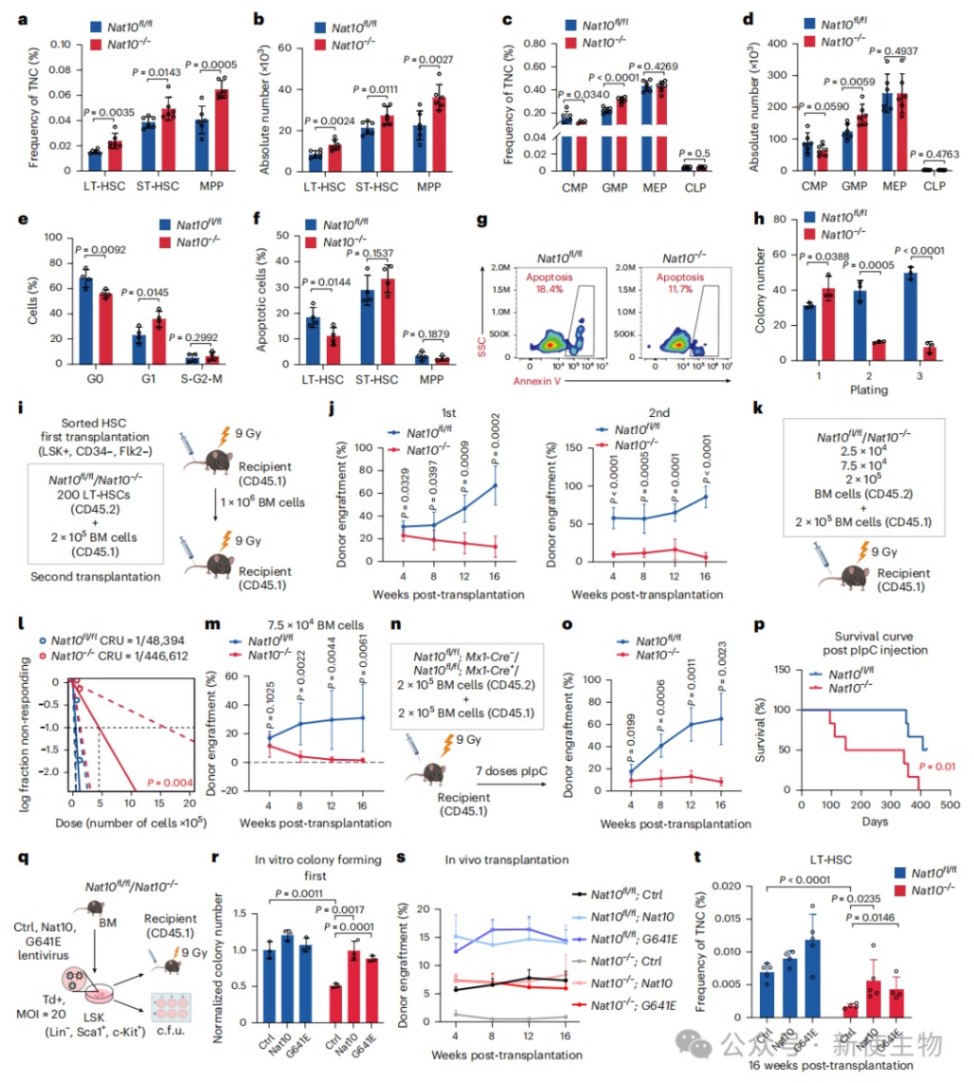
通过Mx1-Cre介导的Nat10条件敲除小鼠模型,研究发现Nat10缺失导致HSC失去静止期并发生分化偏向,显著削弱了干细胞的自我更新。
骨髓移植及移植实验进一步证明,Nat10缺失使HSC的长期造血重建能力严重受损,而过表达催化活性失活的G641E突变体仍能恢复其功能,提示该作用不依赖于乙酰转移酶活性。
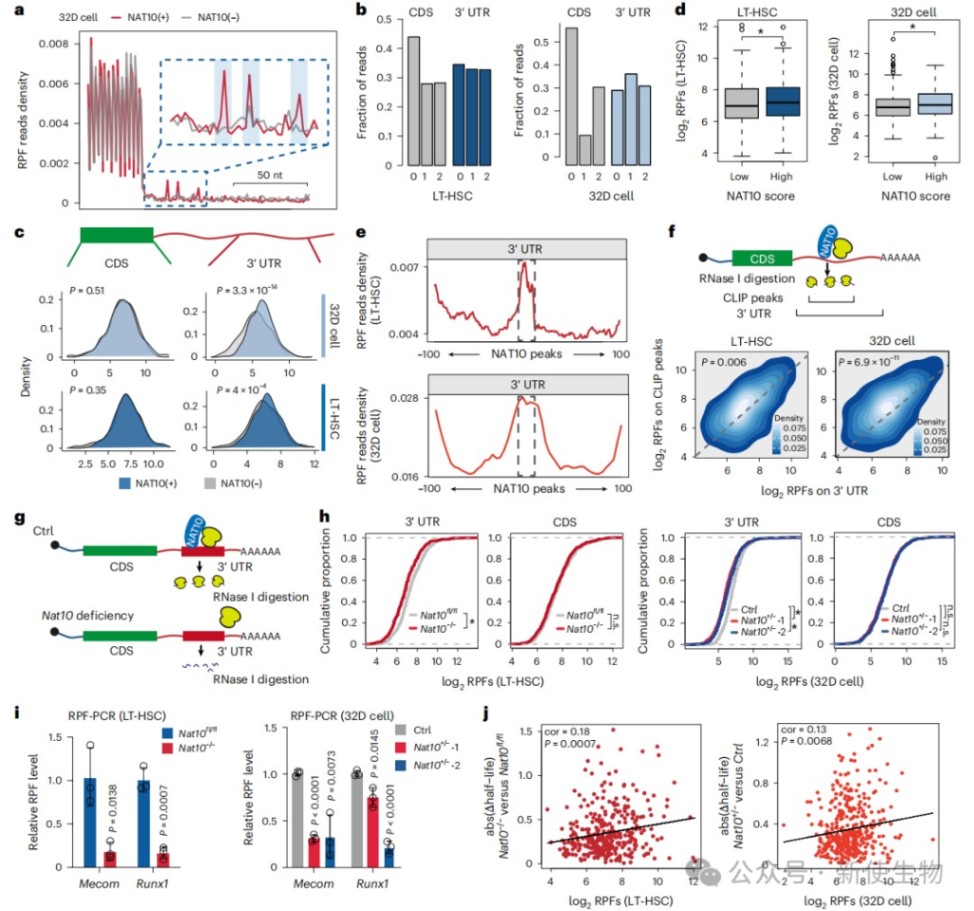
三、NAT10通过结合3' UTR ARE增强关键HSC mRNA的稳定性
结合acRIP-seq和eCLIP-seq技术,研究发现NAT10主要结合在HSC核心基因的3' UTR ARE区域,且这种结合与ac⁴C修饰位点并不重叠。
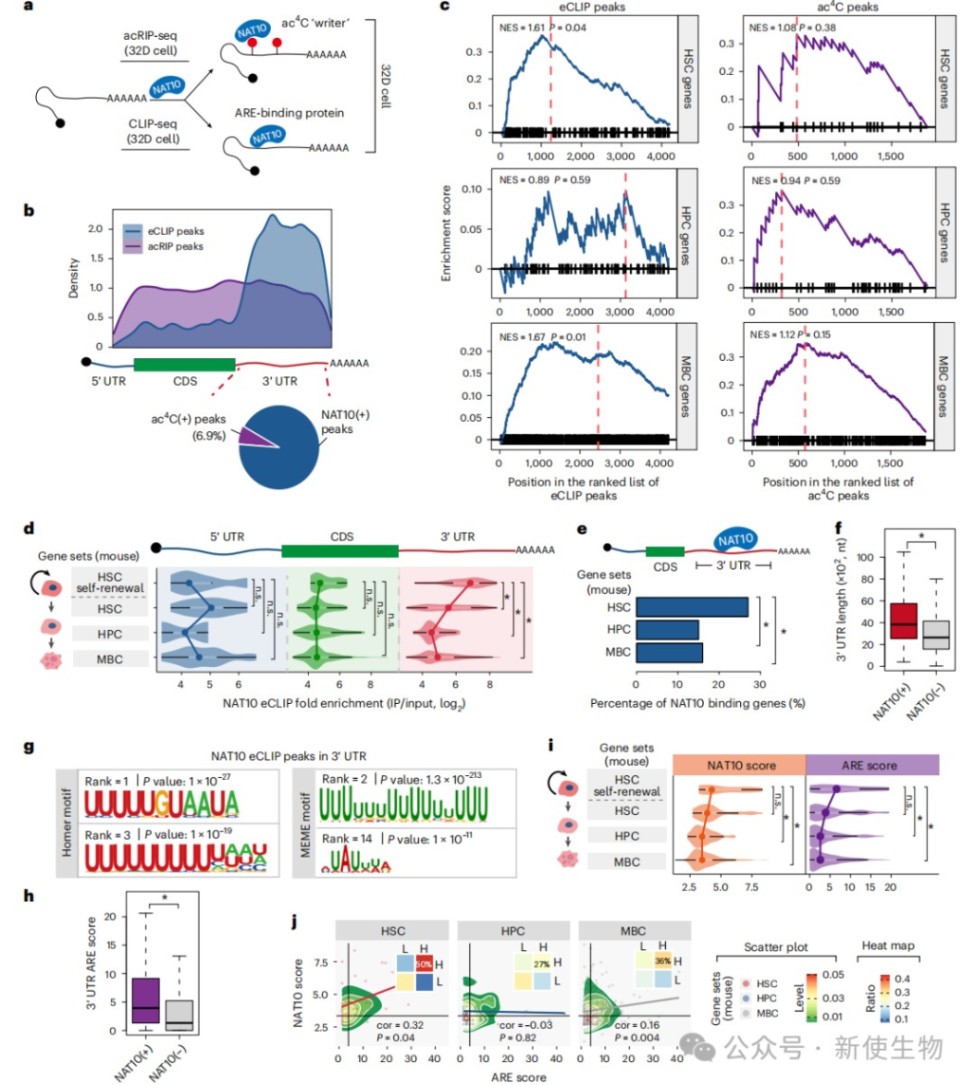
RNA半衰期谱分析显示,Nat10缺失显著缩短了Mecom和Runx1等关键造血调节因子的mRNA寿命,证明NAT10通过直接结合3' UTR来维持转录本稳定性而非调节翻译效率。
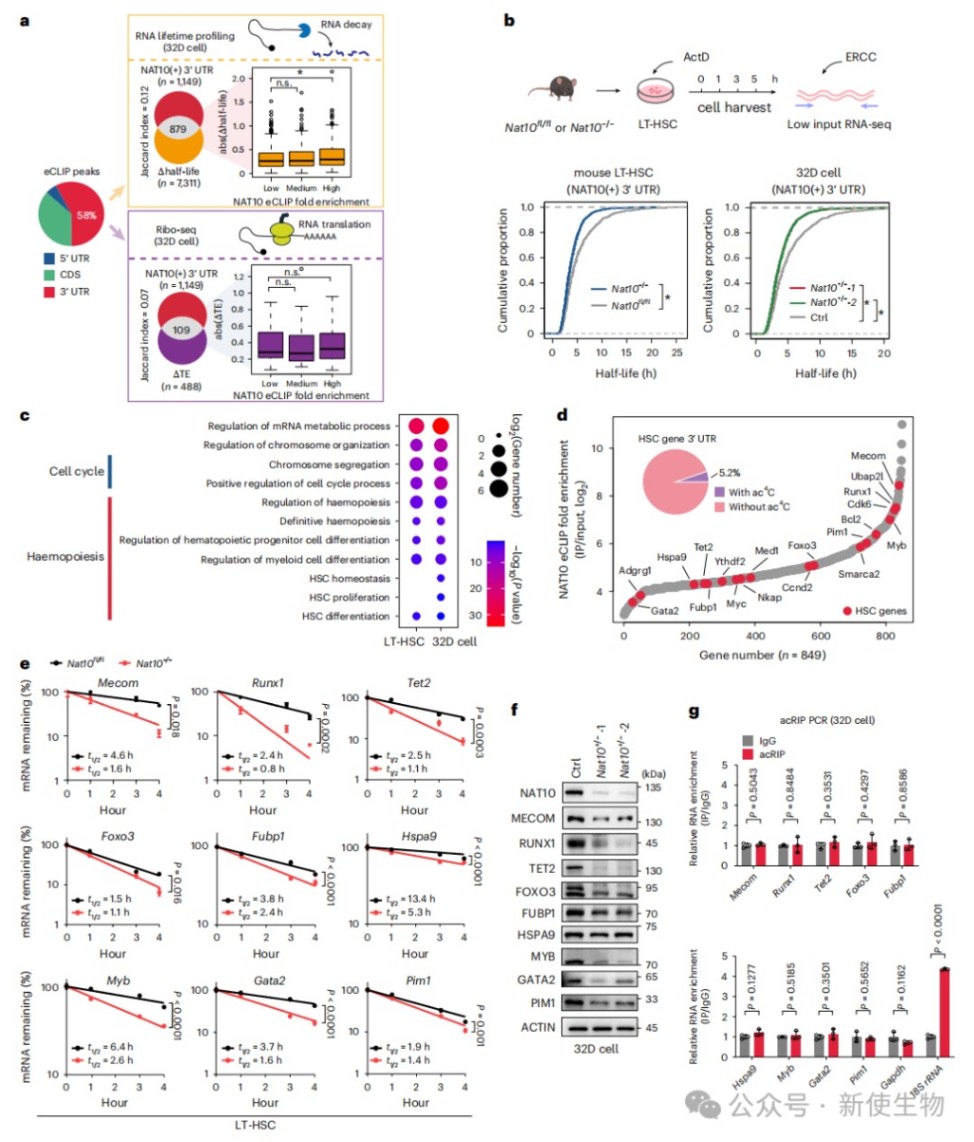
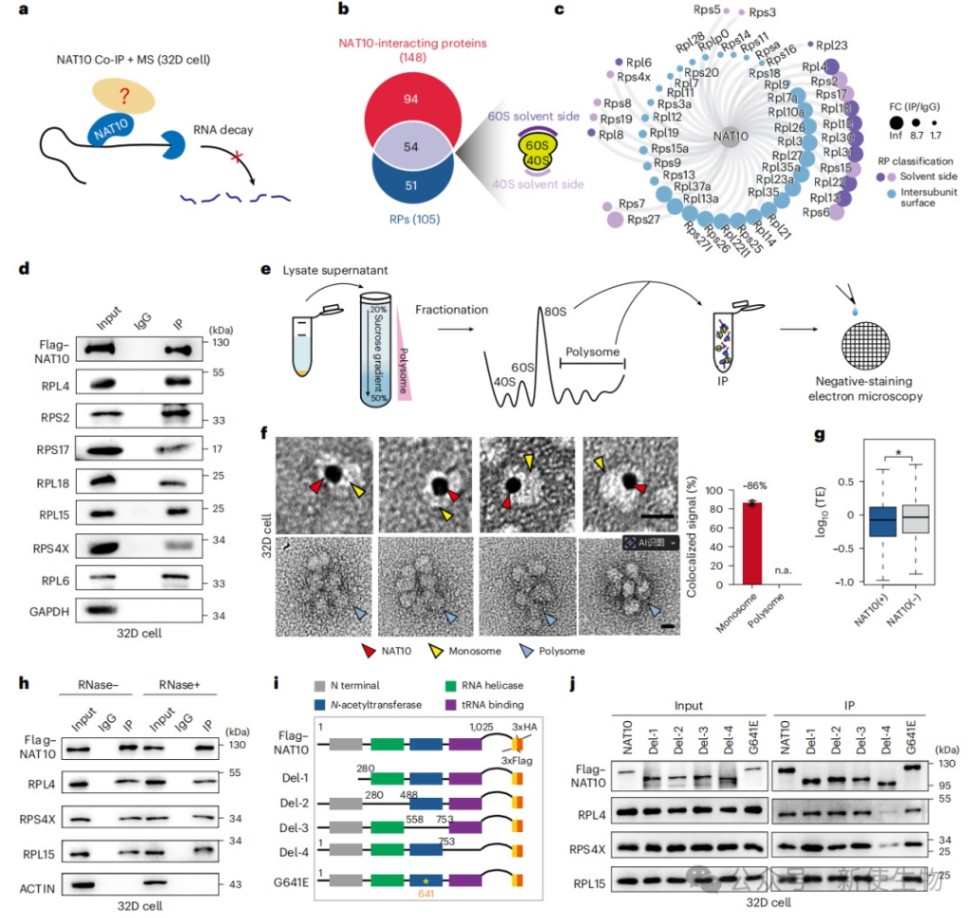
四、NAT10招募核糖体至mRNA的3' UTR以保护其免于降解
免疫共沉淀质谱(Co-IP MS)分析和Polysome profiling多聚核糖体分析显示,NAT10与超过一半的核糖体蛋白(RPs)相互作用,且主要存在于单核糖体而非多聚核糖体中。
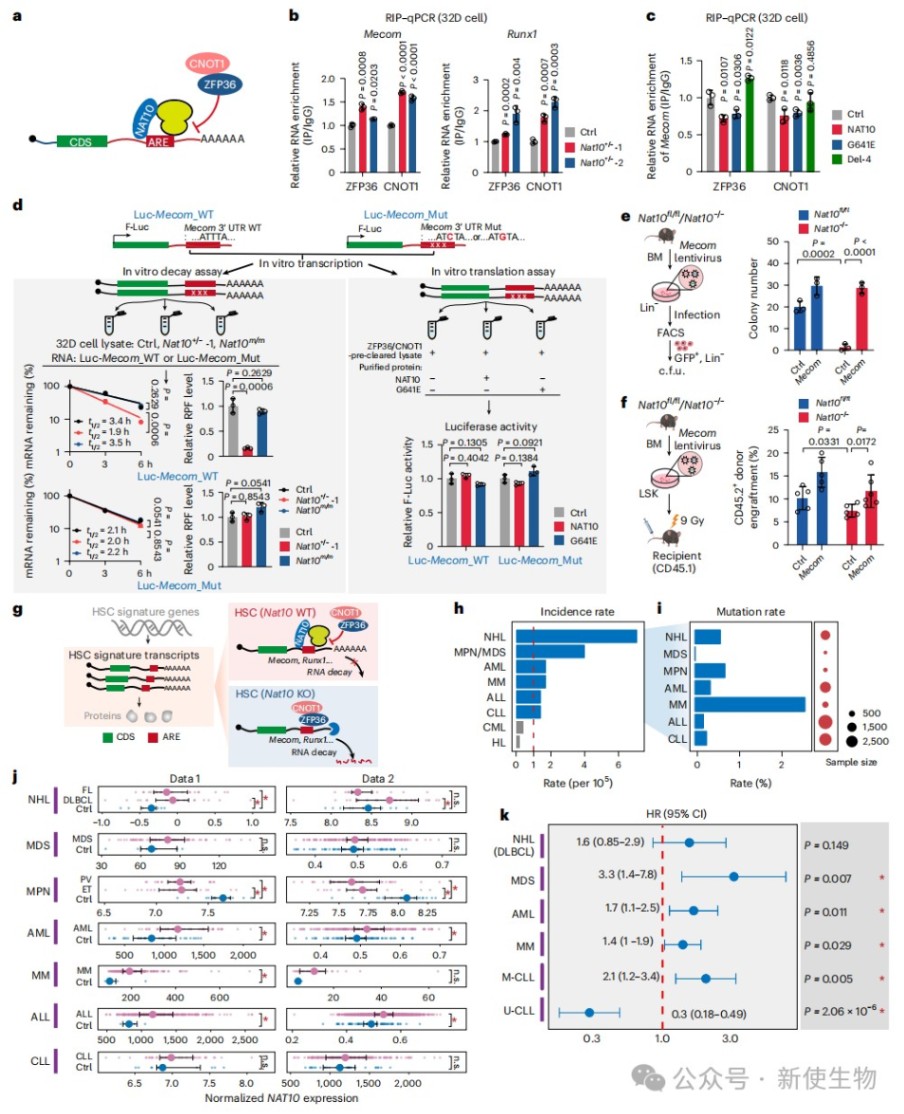
五、NAT10通过拮抗衰变复合物发挥功能且与临床预后相关
研究进一步证实NAT10通过招募核糖体与ZFP36-CNOT1衰变复合物竞争结合3' UTR,从而阻止关键mRNA降解并维持HSC功能。
最后,临床数据分析显示NAT10在多种人类血液恶性肿瘤中表达异常,且其高表达与MDS、AML和MM患者的不良预后密切相关。
总结
本研究发现了一种由NAT10介导的、不依赖于其乙酰转移酶活性的RNA稳定性调控新模式,即通过在3’ UTR招募核糖体来拮抗mRNA衰变。该研究不仅深化了对造血干细胞稳态维持机制的理解,也为血液系统恶性肿瘤的治疗提供了潜在的新靶点和理论依据。
点击图片查看 点击图片查看新使生物专业翻译组一站式服务平台 产品名称


 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们
