
导读
肺腺癌(LUAD)是全球癌症相关死亡的主要原因之一,其预后与诊断时的临床分期密切相关,晚期患者的生存率极低。尽管靶向治疗和免疫治疗取得了一定进展,但晚期或转移性肺腺癌的治疗效果仍不理想,因此亟需寻找新的预后生物标志物并阐明其发病机制。
N4-乙酰胞苷(ac⁴C)是一种重要的RNA修饰,其写入酶NAT10在多种癌症中异常上调并促进肿瘤发生。THUMPD1作为NAT10在tRNA修饰中的关键辅因子已被熟知,但其是否参与mRNA的ac⁴C修饰仍存在争议。
目前,THUMPD1在癌症中的功能,尤其是在肺腺癌中的具体作用和调控机制尚不明确,有待深入研究。
2026年5月4日,郑州大学张澎团队在Advanced Science 上发表了题为“Cuproptosis and Mitophagy Mediated by the THUMPD1/IGF2R-Dependent Suppression of AKT and Activation of AMPK Signaling Suppress Lung Adenocarcinoma Progression” 的研究论文。该研究揭示了THUMPD1通过调控IGF2R的翻译及亚细胞定位,进而抑制AKT信号通路并激活AMPK,最终诱导铜死亡与过度线粒体自噬的全新肿瘤抑制机制。

文章索引
【标题】Cuproptosis and Mitophagy Mediated by the THUMPD1/IGF2R-Dependent Suppression of AKT and Activation of AMPK Signaling Suppress Lung Adenocarcinoma Progression
【发表期刊】Advanced Science
【发表日期】2026年5月4日
【作者及团队】郑州大学张澎团队
【IF】14.1
研究结果
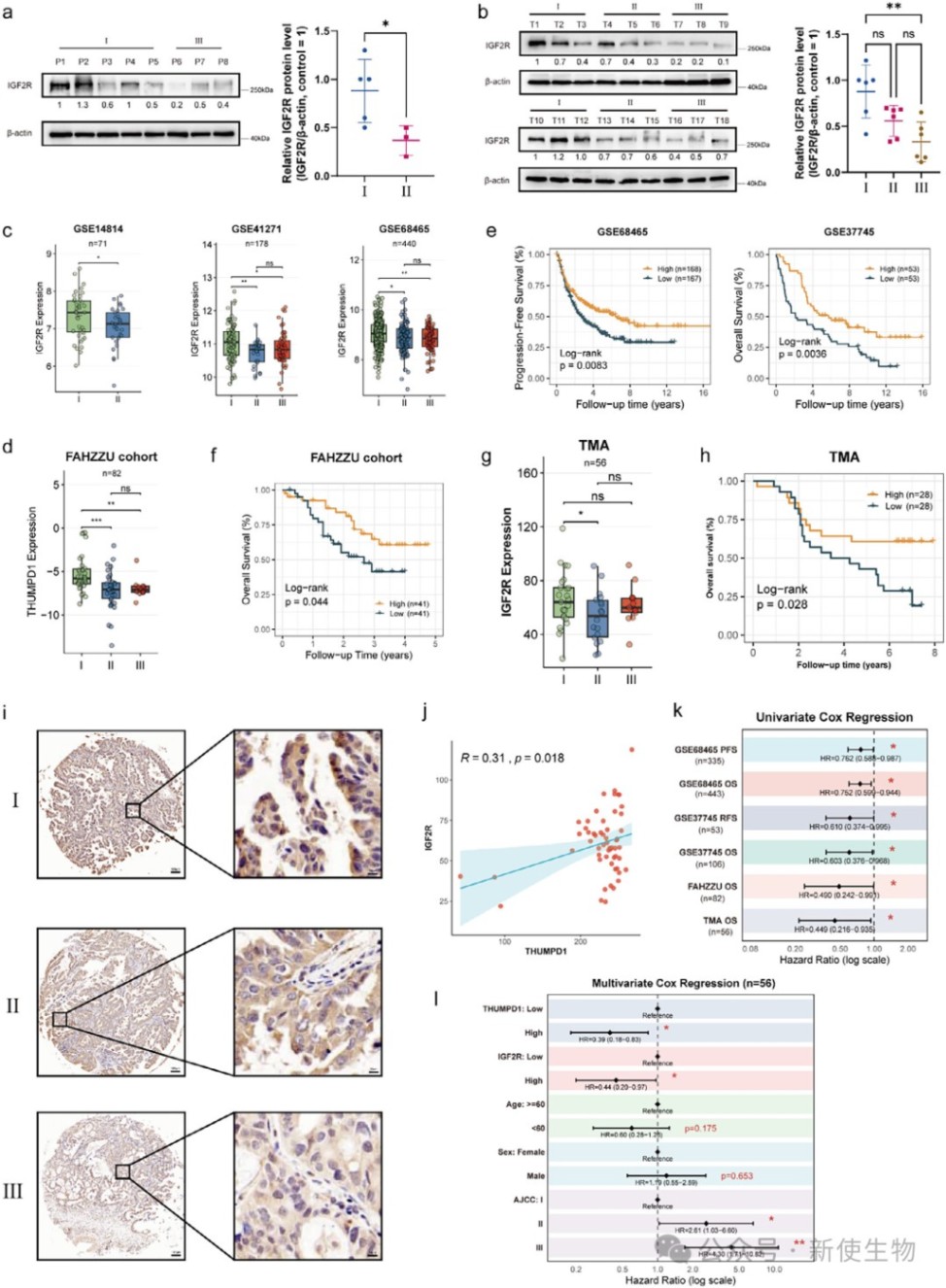
一、THUMPD1在肺腺癌中的低表达与晚期疾病和不良预后相关
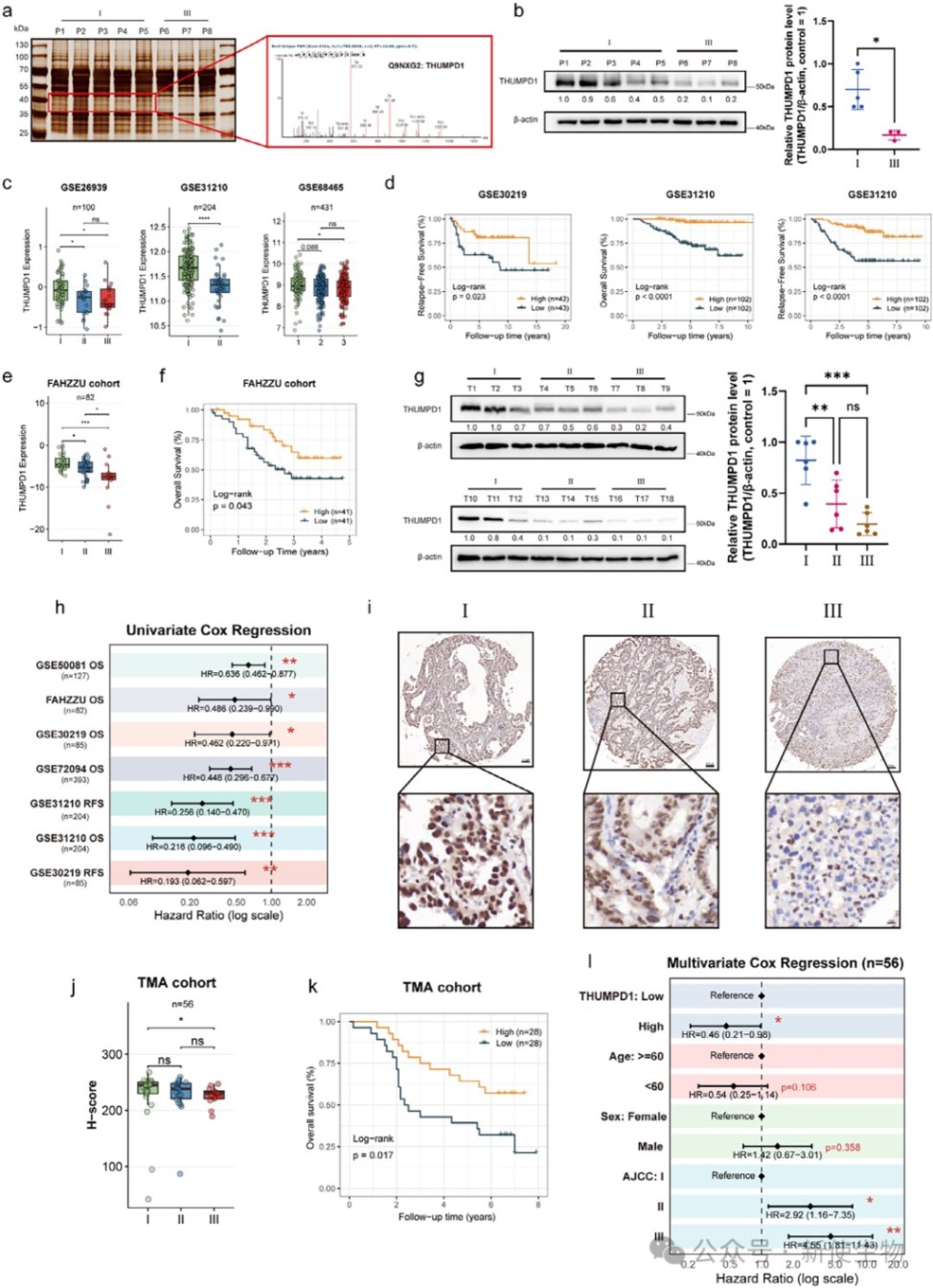
通过对临床样本的蛋白质谱分析,研究发现THUMPD1蛋白在晚期肺腺癌组织中显著下调。
结合公共数据库和本院队列数据的分析证实,THUMPD1的低表达与肺腺癌的不良预后密切相关,是一个独立的有利预后因素。
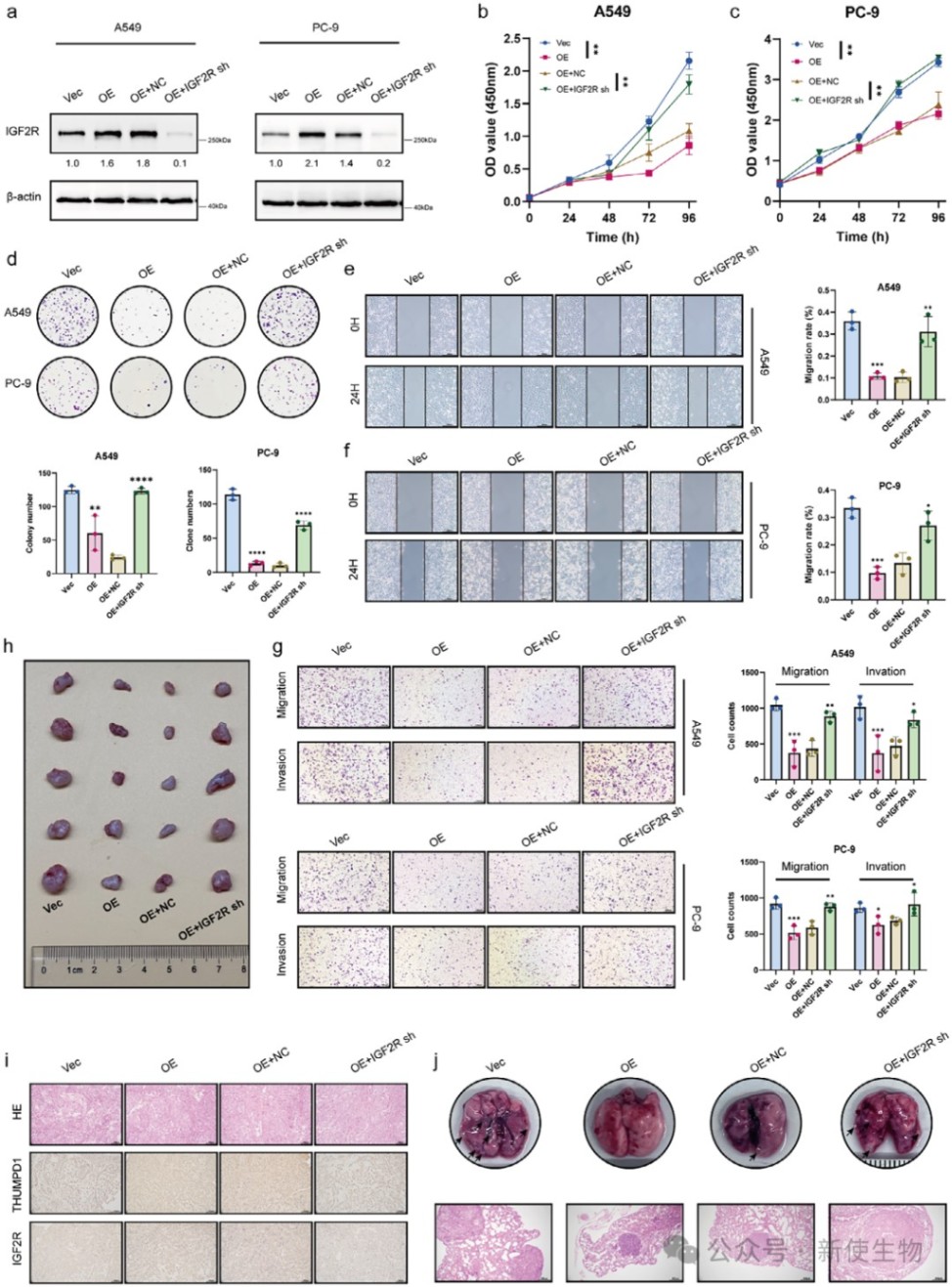
二、THUMPD1抑制肺腺癌的增殖、迁移和侵袭
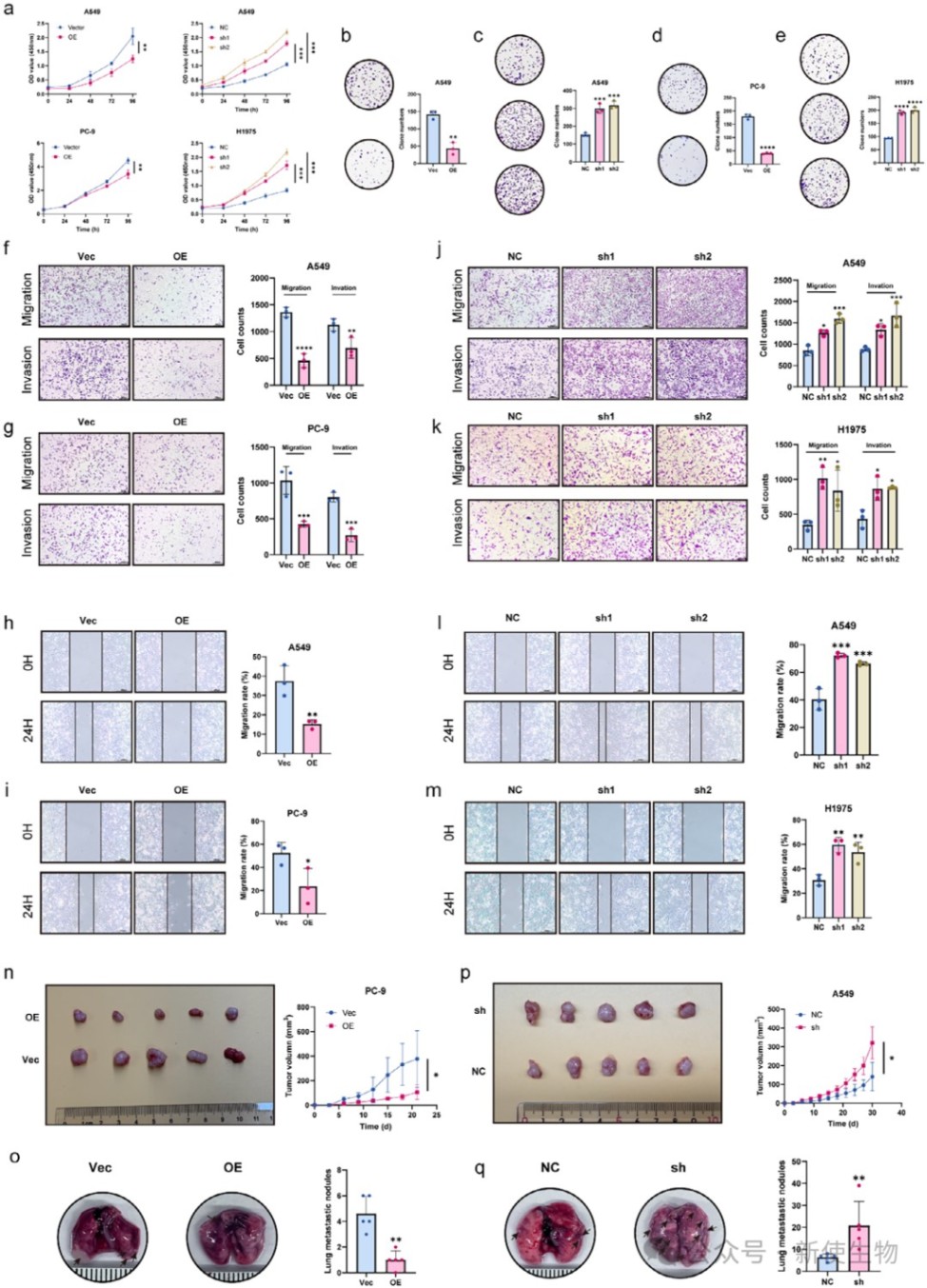
通过在多种肺腺癌细胞系中进行过表达和敲低实验,发现THUMPD1能够显著抑制细胞的增殖、克隆形成、迁移和侵袭能力。
在小鼠模型中,过表达THUMPD1同样抑制了肿瘤的生长和肺转移。
三、THUMPD1可能调控mRNA的ac⁴C修饰和翻译过程
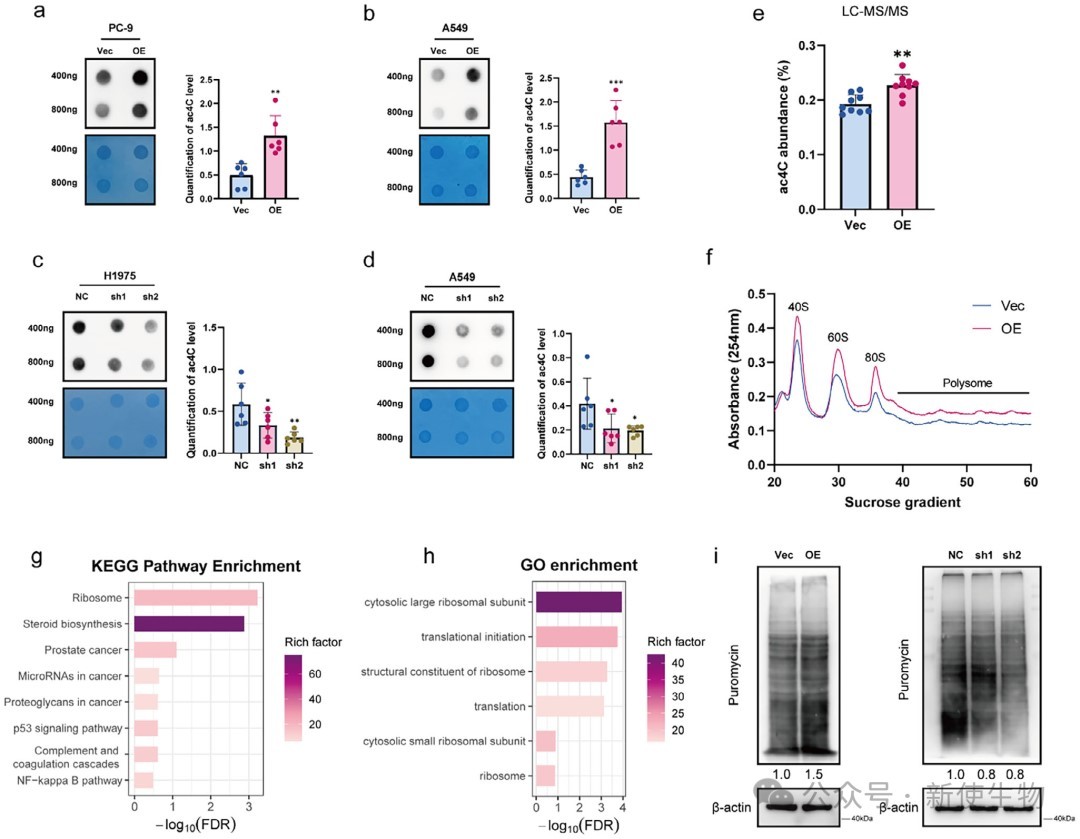
研究通过质谱分析、Polysome profiling多聚核糖体分析和嘌呤霉素掺入实验,证明THUMPD1的表达水平与mRNA的整体ac⁴C修饰水平及全局翻译效率呈正相关,表明THUMPD1可能参与了mRNA的翻译调控。
四、THUMPD1通过不依赖ac⁴C修饰的方式增强IGF2R的翻译来上调其表达
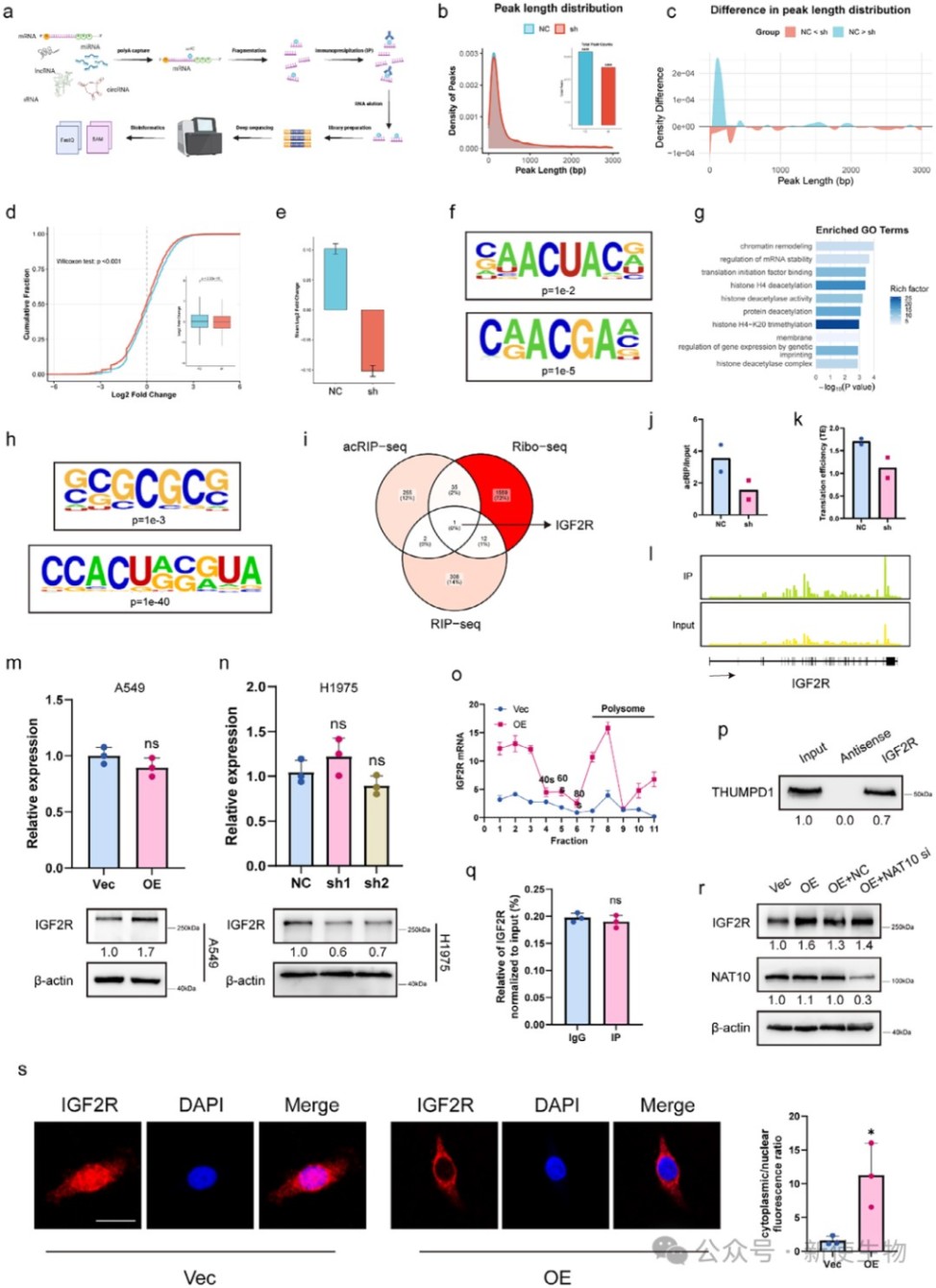
利用acRIP-seq、RIP-seq和Ribo-seq核糖体印迹分析等多组学联合分析,筛选出IGF2R是THUMPD1的直接调控靶点。
进一步实验表明,THUMPD1直接结合IGF2R mRNA并促进其从细胞核向细胞质的转运,从而增强其翻译,且这一过程不依赖于ac⁴C修饰或NAT10。
五、IGF2R在LUAD中是抑癌因子并与THUMPD1表达正相关
通过分析临床样本和公共数据库,验证了IGF2R在肺腺癌中同样扮演抑癌角色,其表达量在晚期肿瘤中降低,且高表达预示着更好的生存。
此外,IGF2R与THUMPD1的蛋白水平呈正相关。
六、IGF2R介导THUMPD1的肿瘤抑制功能
在过表达THUMPD1的细胞中敲低IGF2R,发现THUMPD1对肿瘤细胞增殖、迁移和侵袭的抑制作用被显著逆转。
体内实验也证实,IGF2R的缺失削弱了THUMPD1的抑癌效果,表明THUMPD1的功能依赖于IGF2R。
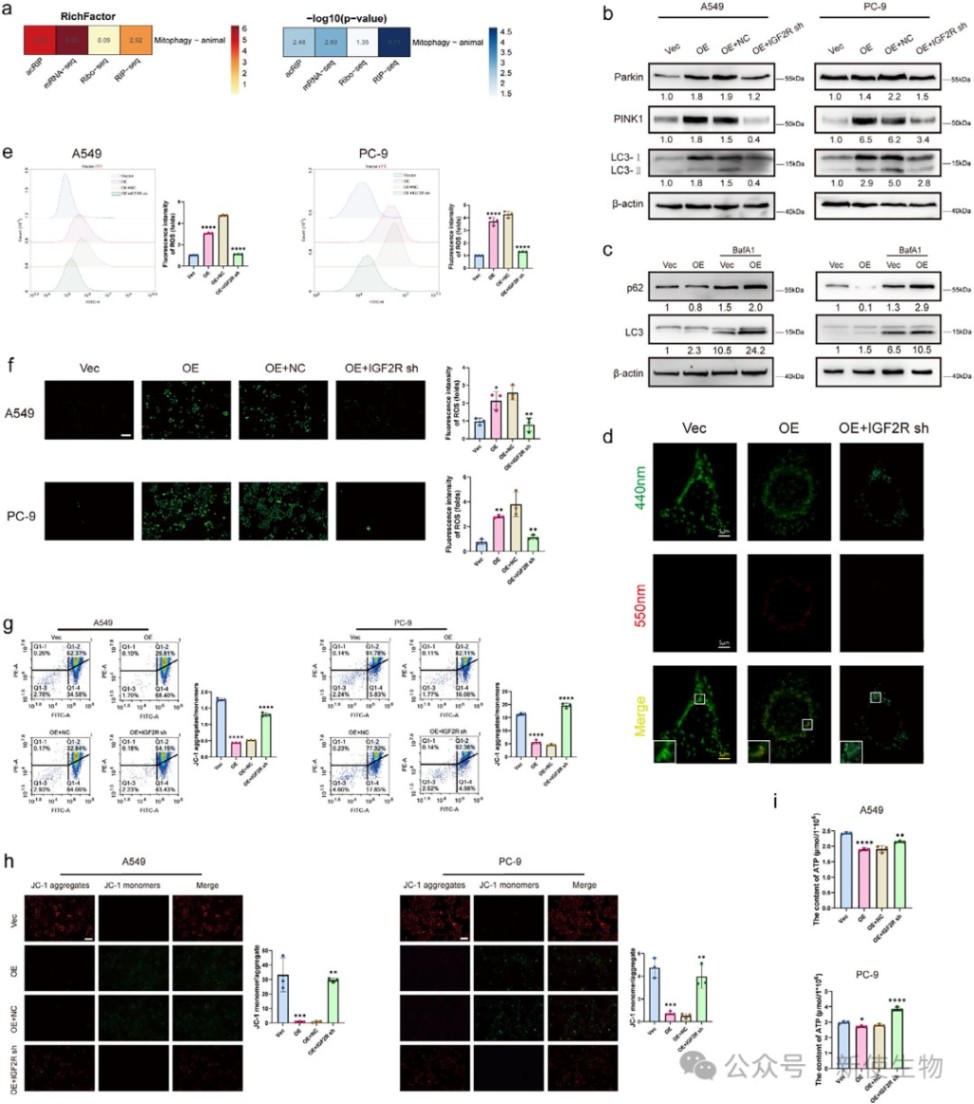
七、线粒体自噬是THUMPD1-IGF2R介导的肿瘤抑制的关键机制
多组学数据显示线粒体自噬通路富集,实验证实THUMPD1-IGF2R轴能够上调线粒体自噬相关蛋白,并增加线粒体自噬流。
这种效应伴随着活性氧(ROS)水平升高和线粒体膜电位下降等线粒体应激现象。
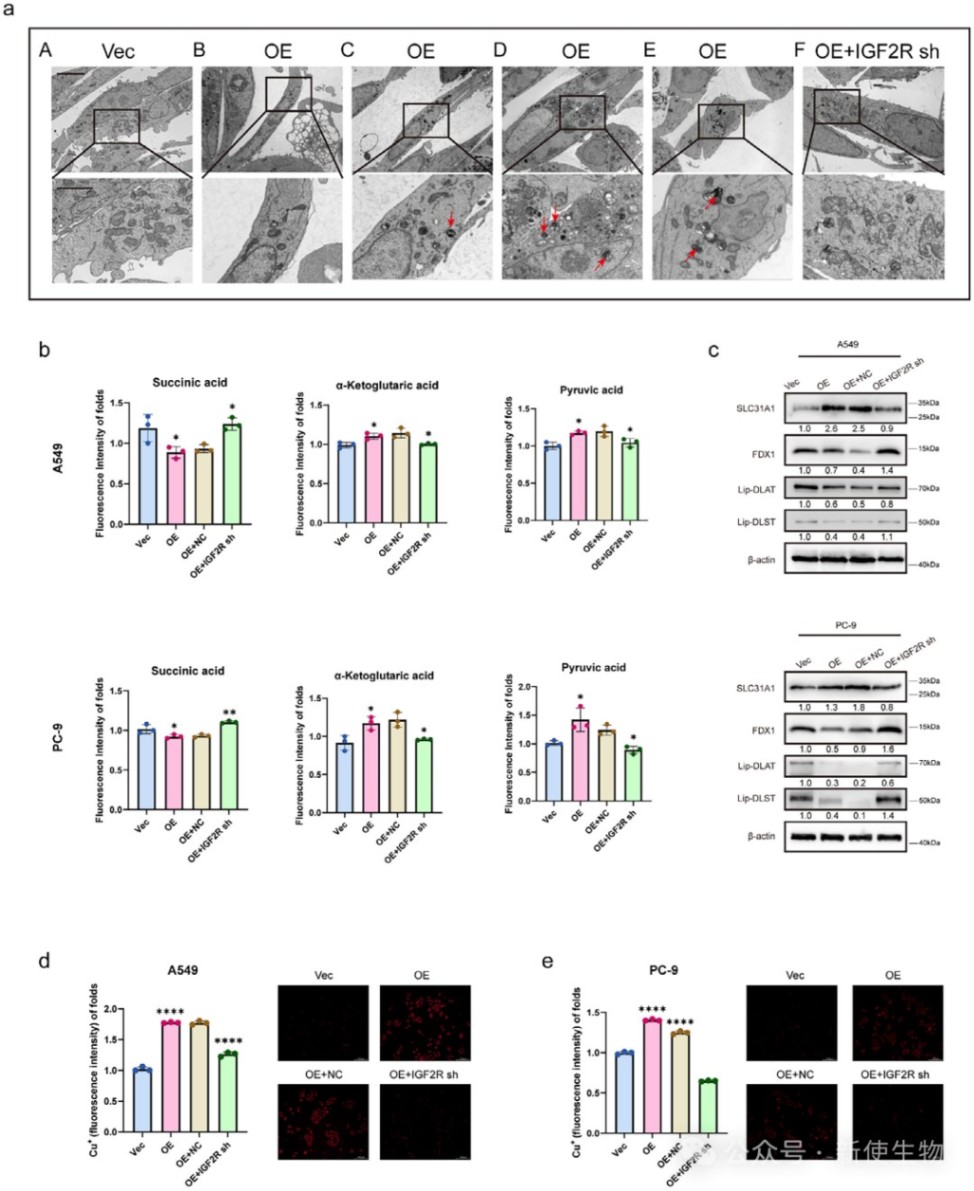
八、Cu+超载和铜死亡相关的代谢压力激活肺腺癌中的过度线粒体自噬
通过电镜观察和代谢物检测,发现THUMPD1过表达导致线粒体严重损伤和三羧酸循环代谢物异常,这与铜死亡的特征相符。
研究进一步证实,THUMPD1通过上调铜转运蛋白SLC31A1导致细胞内Cu+积累,诱发了铜死亡相关蛋白的改变和过度的线粒体自噬。
九、艾司氯莫(ES)通过诱导铜死亡抑制肺腺癌
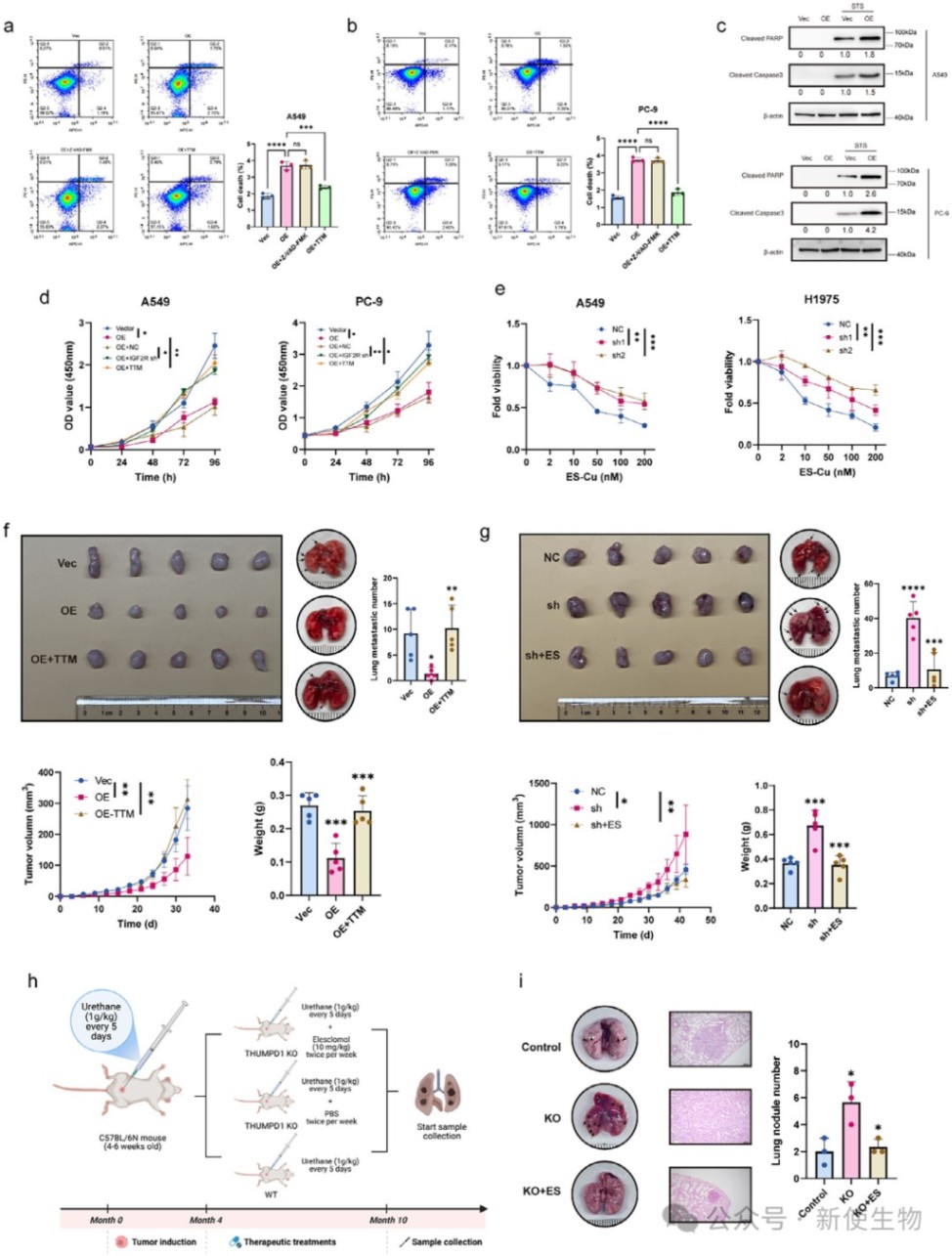
体外实验显示,THUMPD1诱导的细胞死亡可被铜螯合剂TTM抑制,而非凋亡抑制剂。
在小鼠模型中,TTM逆转了THUMPD1的抑癌效果,而铜离子载体艾司氯莫(ES)则能有效抑制THUMPD1敲除小鼠的肿瘤生长,证明靶向铜死亡通路具有治疗潜力。
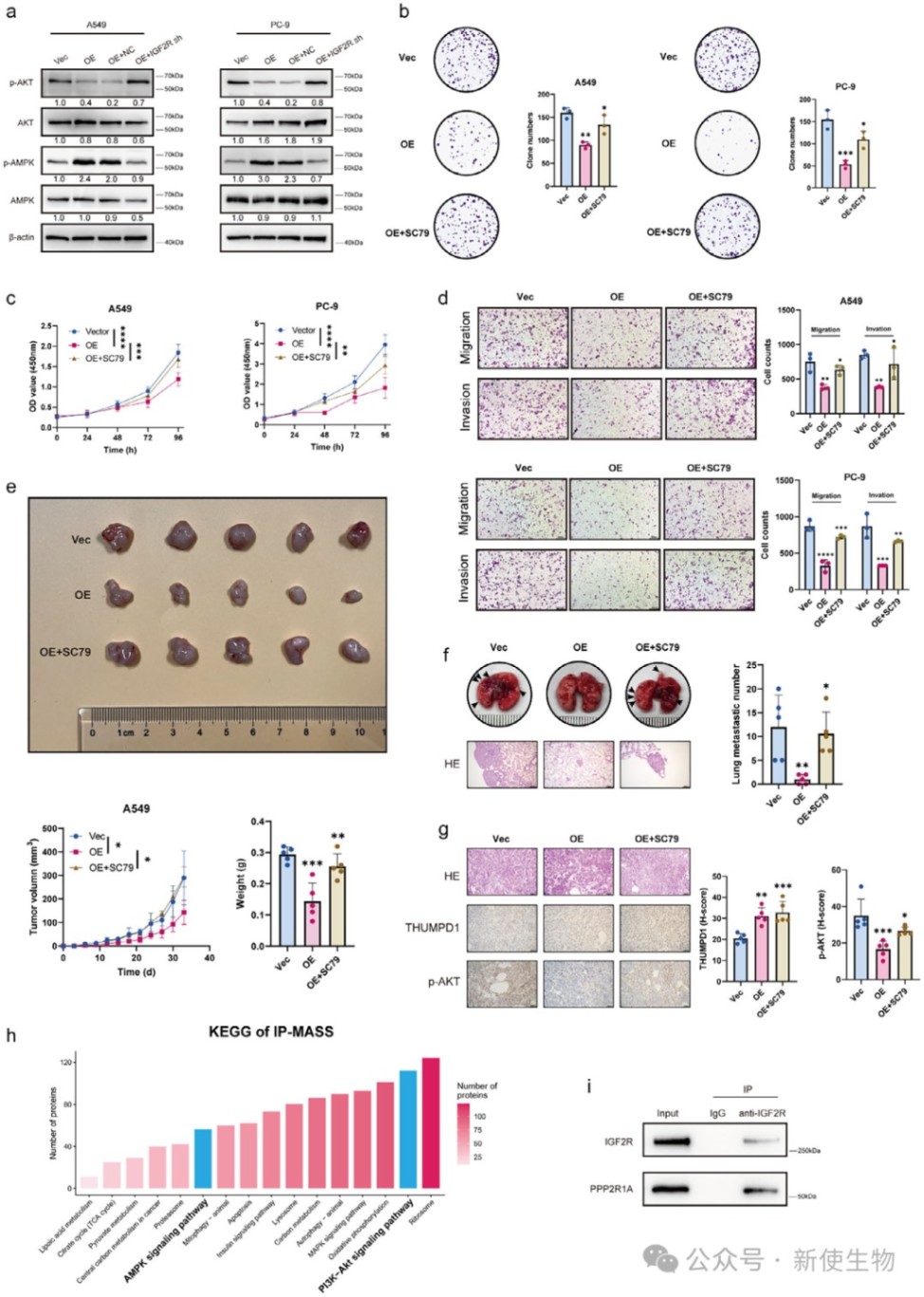
十、THUMPD1-IGF2R轴通过抑制AKT并激活AMPK信号通路发挥作用
机制研究发现,THUMPD1-IGF2R轴通过抑制p-AKT水平和激活p-AMPK水平发挥作用,而使用AKT激动剂SC79可逆转THUMPD1的抑癌效应。
Co-IP实验表明IGF2R与PP2A的支架亚基PPP2R1A相互作用,这可能是其抑制AKT信号的机制。
该通路最终汇合于SLC31A1的上调,连接了信号传导与铜死亡。
总结
本文揭示了THUMPD1/IGF2R轴通过非经典的转录后调控机制增强抑癌蛋白表达,并通过AKT/AMPK通路精细调控细胞代谢稳态。这种由铜离子触发的、结合了铜死亡与过度线粒体自噬的细胞死亡新模式,不仅深化了对肺腺癌进展机制的理解,也为重新定位Elesclomol等药物在肺癌临床治疗中的应用提供了科学依据。
| 新使生物专业翻译组一站式服务平台 |
| 产品名称 |
点击图片查看
点击图片查看


 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们
