
导读
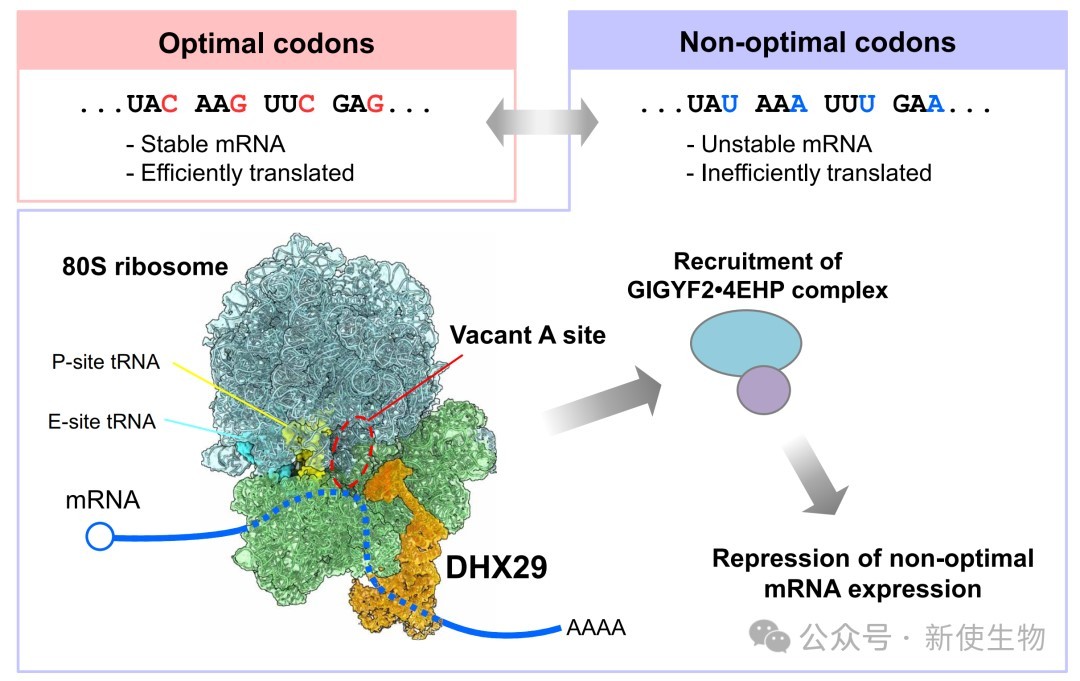
遗传密码具有简并性,多个同义密码子编码同一种氨基酸,但它们在功能上并不等同。同义密码子的使用会显著影响mRNA的稳定性和翻译效率,这种现象在不同物种中普遍存在。
富含最优密码子的mRNA通常表现出较高的稳定性和翻译效率,而富含非最优密码子的mRNA则会被快速降解。翻译与mRNA降解紧密耦合,核糖体在异常翻译过程中充当分子枢纽,激活质量控制机制。
在酿酒酵母等模式生物中,非最优密码子导致核糖体减速的机制已被部分揭示,涉及CCR4-NOT复合物的招募。然而在人类细胞中,感知非最优密码子并调控基因表达的具体分子机制和通用因子仍有待深入探索。
2026年5月7日,日本京都大学Osamu Takeuchi和日本理化学研究所(RIKEN)Takuhiro Ito团队合作,在Science上发表了题为“Human DHX29 detects nonoptimal codon usage to regulate mRNA stability”的研究论文。该研究通过全基因组CRISPR筛选,鉴定出RNA结合蛋白DHX29是人类细胞中密码子依赖性基因表达的关键调控因子。

文章索引
【标题】Human DHX29 detects nonoptimal codon usage to regulate mRNA stability
【发表期刊】Science
【发表日期】2026年5月7日
【作者及团队】京都大学Osamu Takeuchi团队,理化学研究所Takuhiro Ito团队
【IF】 45.8
研究结果
一、DHX29被鉴定为密码子依赖性基因表达的关键调控因子
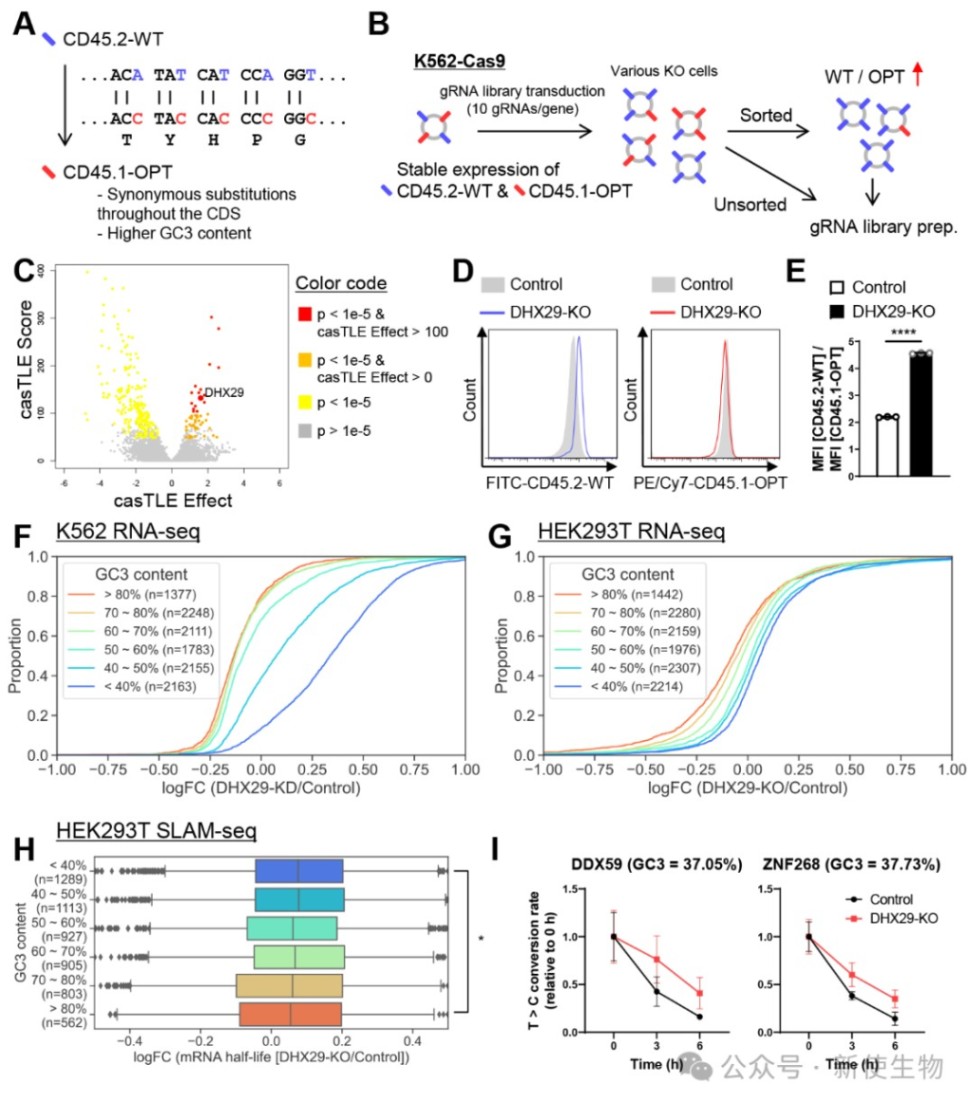
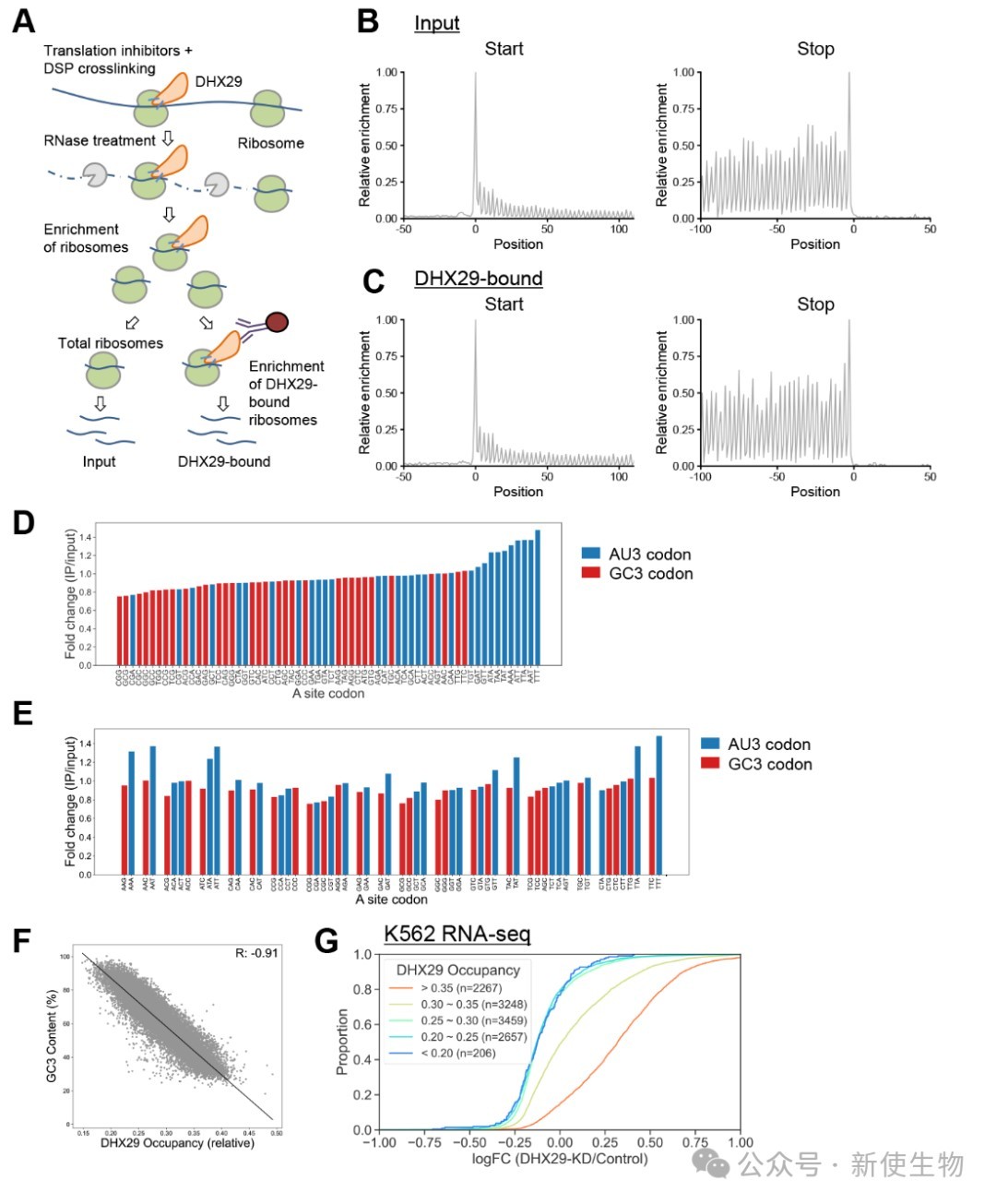
研究人员通过全基因组CRISPR筛选,发现RNA结合蛋白DHX29是选择性靶向非优选mRNA序列的关键调控因子。
RNA测序分析证实,在多种人类细胞系中敲低DHX29后,富含非优选密码子(AU3)的mRNA表达量在全转录组范围内显著上调,且其降解速率减慢。
二、DHX29在结构上与翻译中的80S核糖体直接相互作用
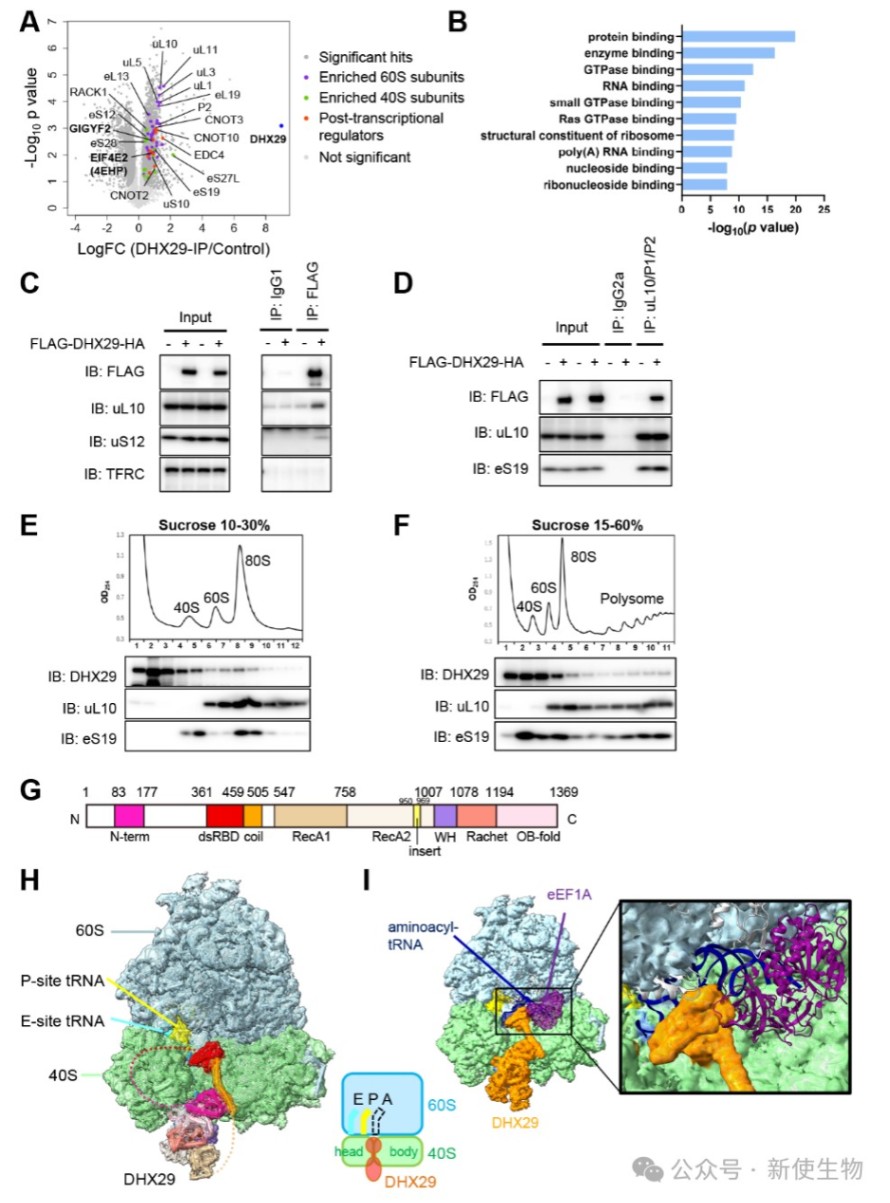
蛋白质组学和Polysome profiling多聚核糖体分析显示,DHX29不仅在翻译起始阶段,也在延伸阶段与翻译中的核糖体互作。
冷冻电镜结构进一步揭示,DHX29通过其dsRBD结构域直接结合于80S核糖体的A位点入口,该结合位置与携带氨基酸的tRNA复合物(eEF1A•GTP•aminoacyl-tRNA)的结合位点相互排斥。
三、DHX29与核糖体A位点入口的相互作用是其发挥功能的关键
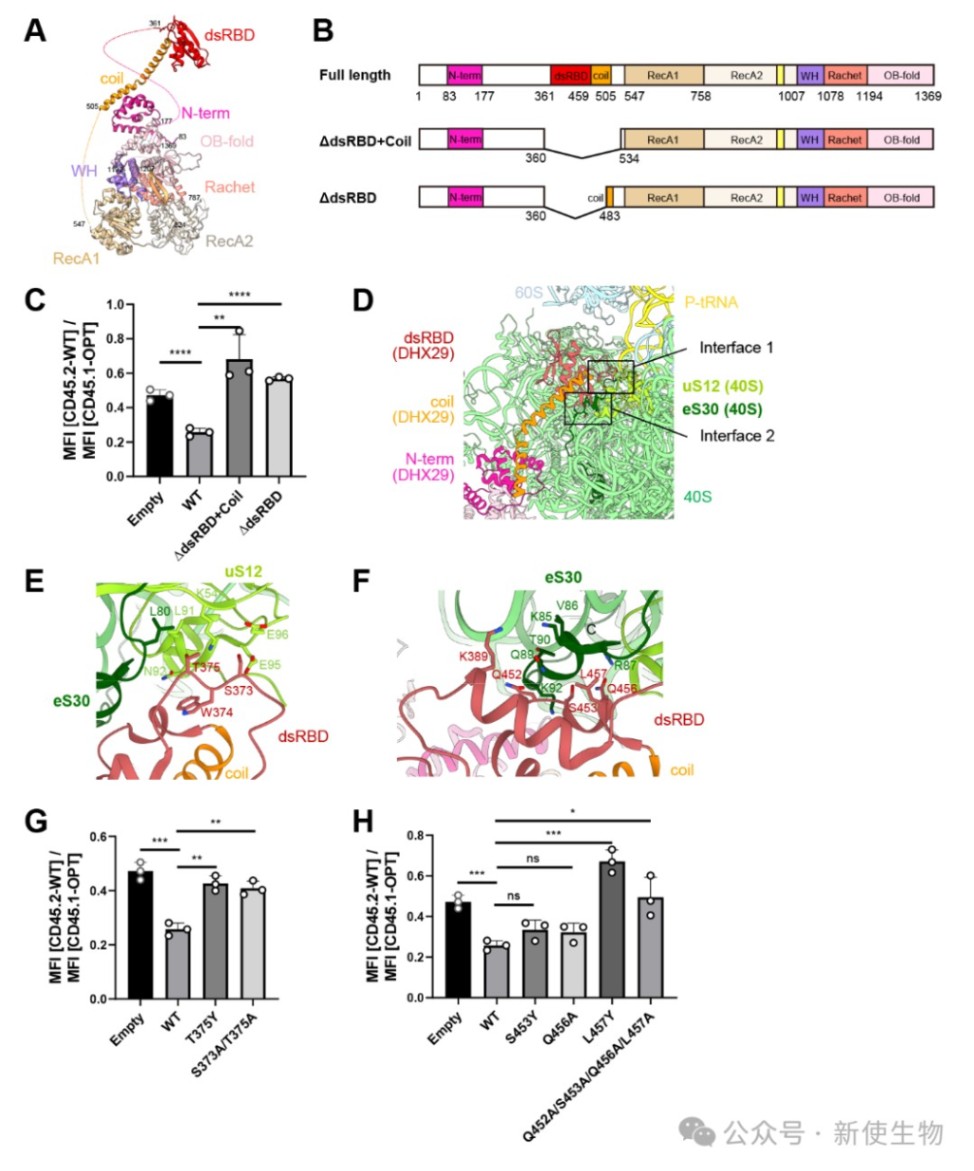
功能性突变分析表明,DHX29的dsRBD结构域是抑制非优选mRNA表达所必需的。
当破坏dsRBD结构域或其与核糖体A位点入口相互作用的关键氨基酸残基时,DHX29便失去了调控非优选mRNA表达的能力。
四、DHX29优先结合解码非优密码子(AU3)的核糖体
研究人员通过选择性Ribo-seq核糖体印迹分析发现,DHX29优先与A位点正在解码非优选密码子(特别是AU结尾的密码子)的核糖体结合。
携带高DHX29占有率的mRNA更容易被降解,这表明DHX29的结合直接引导了对这些mRNA的抑制。
作者通过tRNA-seq分析发现,tRNA的丰度与DHX29对相应密码子的偏好性之间没有显著的相关性。
五、DHX29通过招募GIGYF2•4EHP复合物介导对非优密码子mRNA的抑制
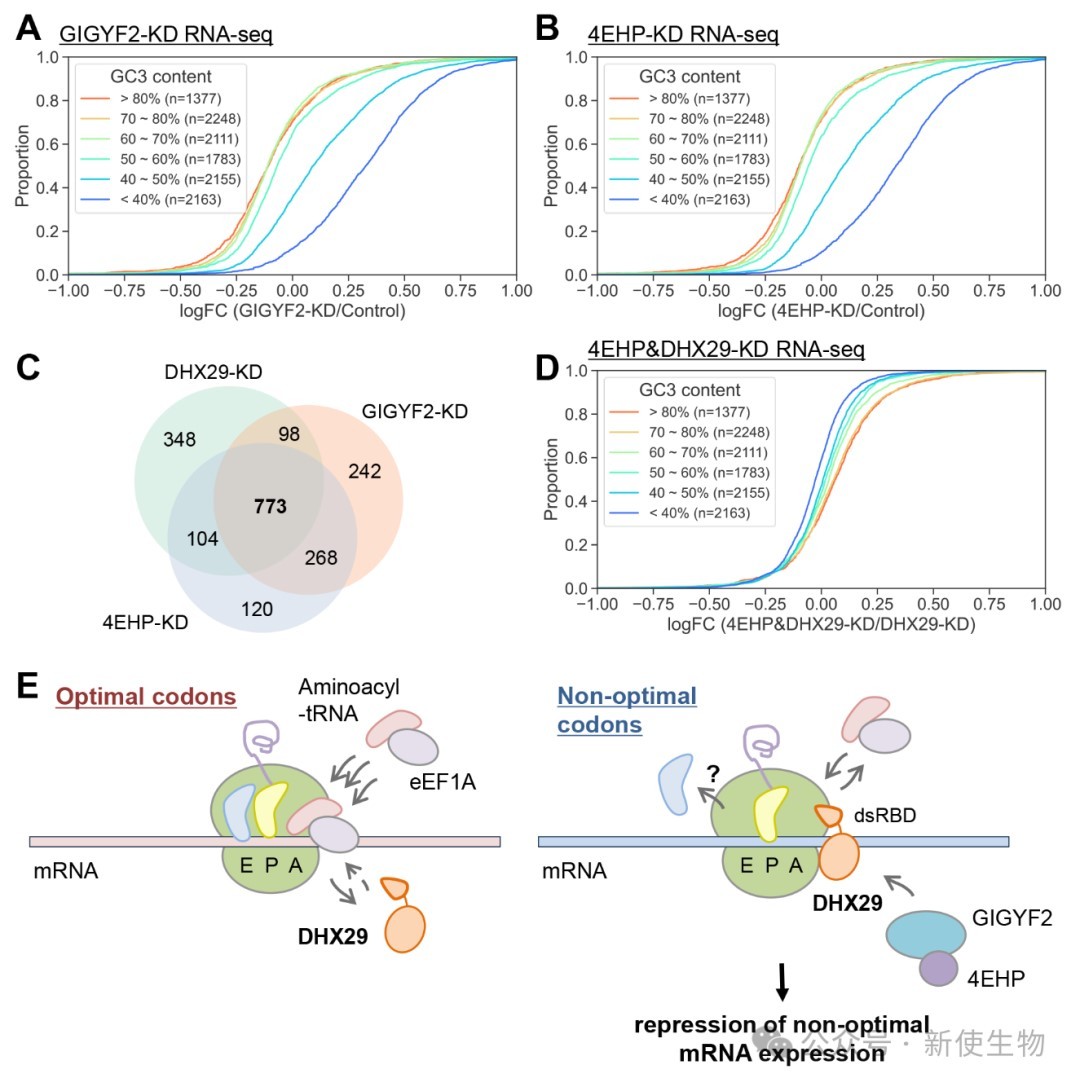
蛋白质互作分析发现,DHX29与GIGYF2•4EHP复合物相关联,该复合物已知与核糖体停滞的mRNA抑制有关。
敲低GIGYF2或4EHP后,细胞表现出与敲低DHX29相似的表型,即非优选mRNA表达上调,且双敲低实验表明它们在同一调控通路中发挥作用。
总结
本研究揭示了RNA结合蛋白DHX29在人类细胞中作为密码子最优性核心监测因子的全新功能。DHX29通过直接感知翻译延伸过程中A位点解码非最优密码子时的空位状态,进而特异性招募GIGYF2•4EHP复合物以促进mRNA降解。该发现有效填补了真核生物同义密码子使用差异与mRNA稳定性调控之间的机制空白,为探究由翻译异常驱动的多种人类疾病发病机制提供了崭新视角。
| 新使生物专业翻译组一站式服务平台 |
| 产品名称 |
点击图片查看
点击图片查看


 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们
