
导读
核糖体已成为一个重要的信号中心,能够感知代谢紊乱并协调细胞响应,以恢复体内平衡或启动细胞死亡。然而,通过核糖体发出信号的损伤范围以及控制细胞命运决定的机制仍未完全阐明。
许多此类威胁最终都会汇聚到整合应激反应(ISR)上,在此过程中,整体蛋白质翻译被抑制,而转录因子ATF4则被选择性翻译以缓解应激。HOIL-1是一种环-环间(RBR)家族E3连接酶,其功能缺失会导致一种致命的多器官疾病,伴有免疫和代谢症状。
HOIL-1最著名的是其作为线性泛素组装复合物(LUBAC)的组成部分在免疫反应中的作用。此外,HOIL-1还能够通过酯键将泛素缀合到其底物上,例如体外直接泛素化糖原,但该疾病致命代谢特征的病因目前尚不清楚。
2026年4月30日,耶鲁大学Todd Douglas团队在Nature Cell Biology上发表了题为“The atypical E3 ligase HOIL-1 safeguards the ribosome during cellular stress”的研究论文。该研究首次将非典型E3泛素连接酶HOIL-1鉴定为核糖体信号网络中一个意想不到的节点,它通过促进核糖体泛素化和细胞保护性核糖体相关质量控制(RQC)来化解细胞应激。

文章索引
【标题】The atypical E3 ligase HOIL-1 safeguards the ribosome during cellular stress
【发表期刊】Nature Cell Biology
【发表日期】2026年4月30日
【作者及团队】耶鲁大学Todd Douglas团队
【IF】19.1
研究结果
一、HOIL-1缺失加剧心脏重塑并抑制糖原分解
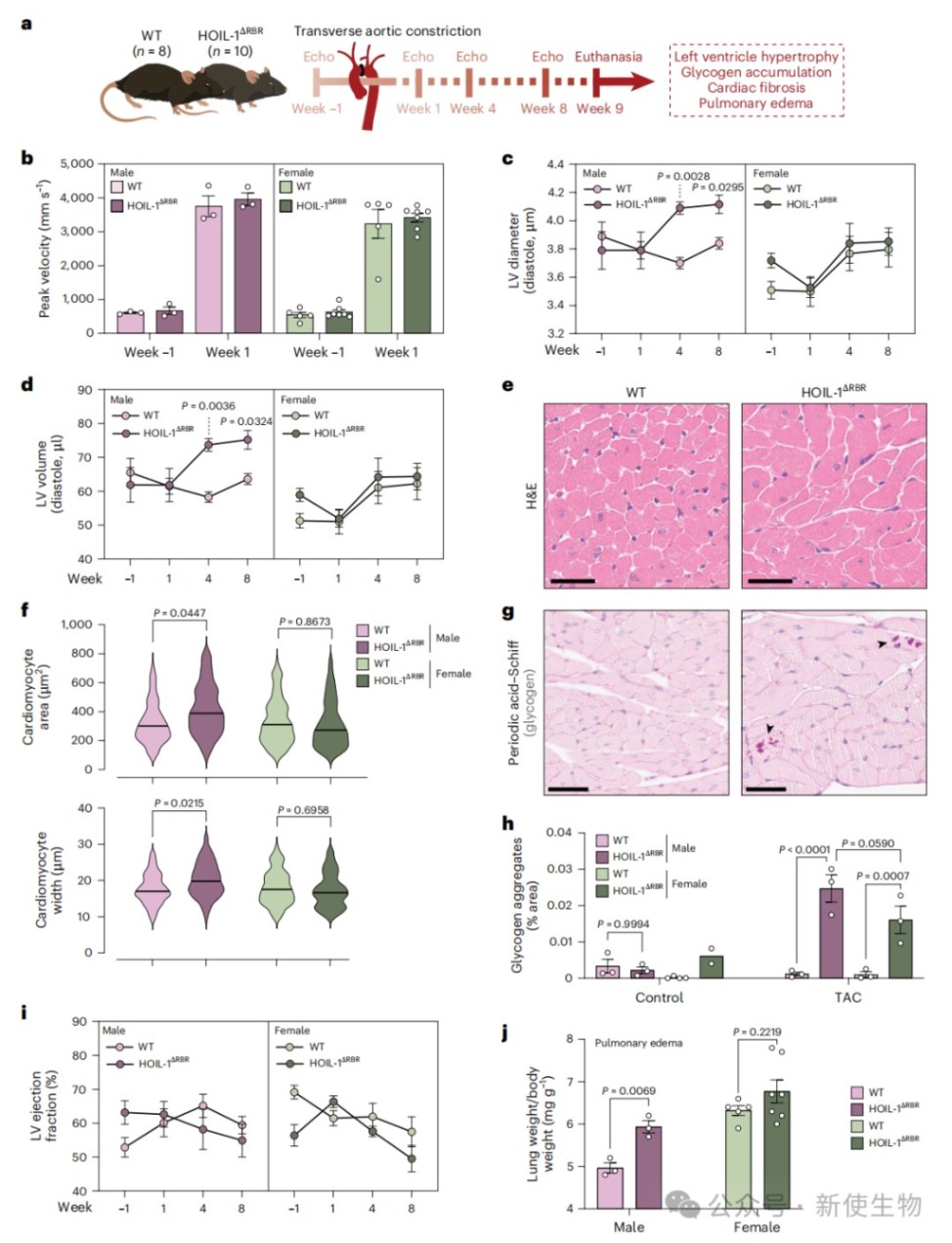
通过对小鼠进行主动脉弓缩窄(TAC)手术诱导压力超负荷,结合超声心动图和组织学染色等方法,研究团队发现HOIL-1ΔRBR雄性小鼠出现更严重的心室扩张、心肌细胞肥大和糖原聚集。
这表明HOIL-1缺失会加剧压力诱导的心脏病理重塑,且其RBR结构域对于营养应激下的糖原分解至关重要。
二、HOIL-1的RBR突变使细胞对葡萄糖饥饿诱导的双硫死亡敏感
利用CRISPR-Cas9技术构建HOIL-1截短突变细胞系,结合LC-MS/MS全代谢组学分析,作者发现HOIL-1ΔRBR细胞在葡萄糖饥饿下极易死亡并积累了大量胱氨酸和氧化型谷胱甘肽。
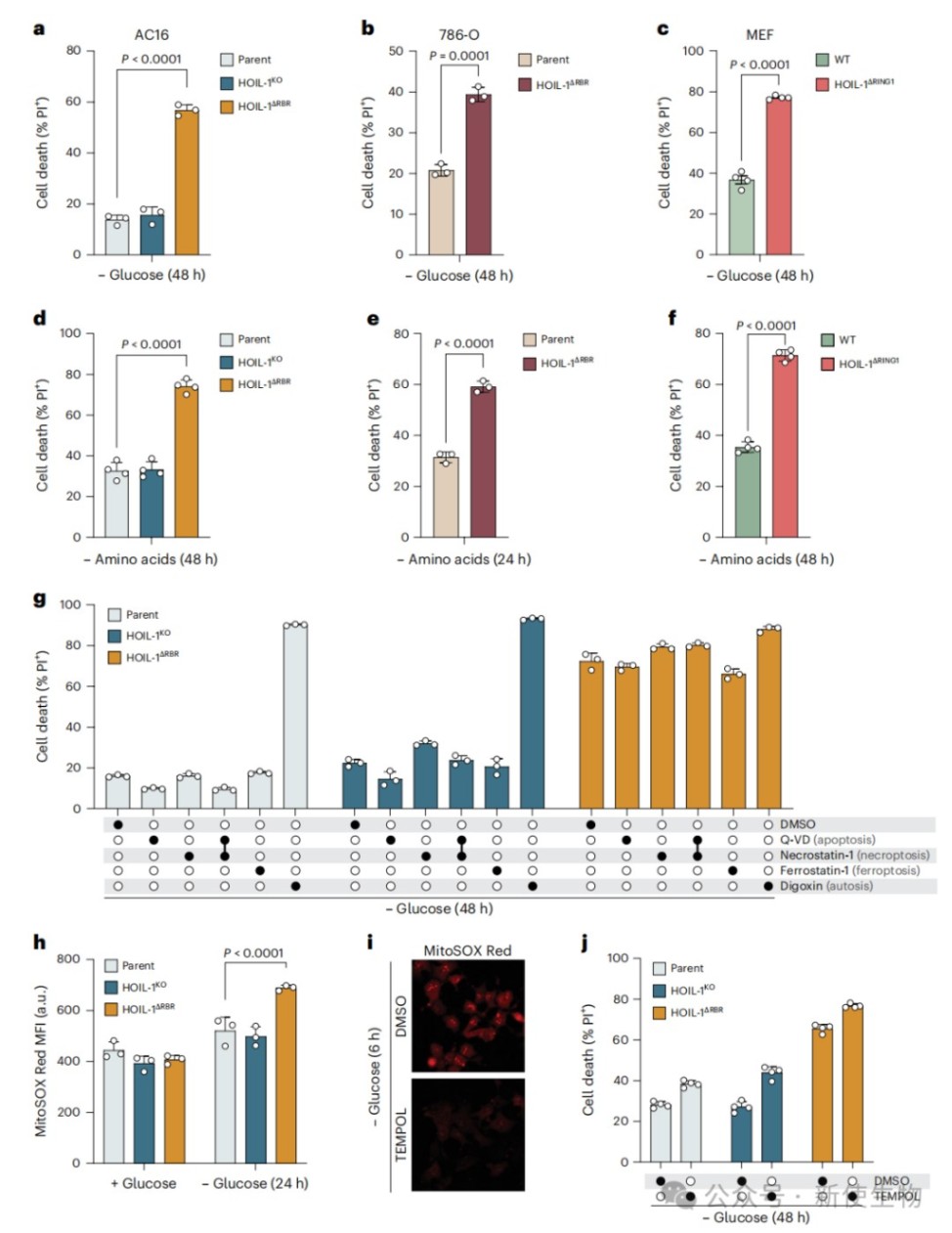
实验证实胱氨酸转运体xCT的过度上调破坏了细胞NADPH及NADP+的还原力稳态,最终驱动了依赖xCT的非经典双硫死亡(disulfidptosis)。
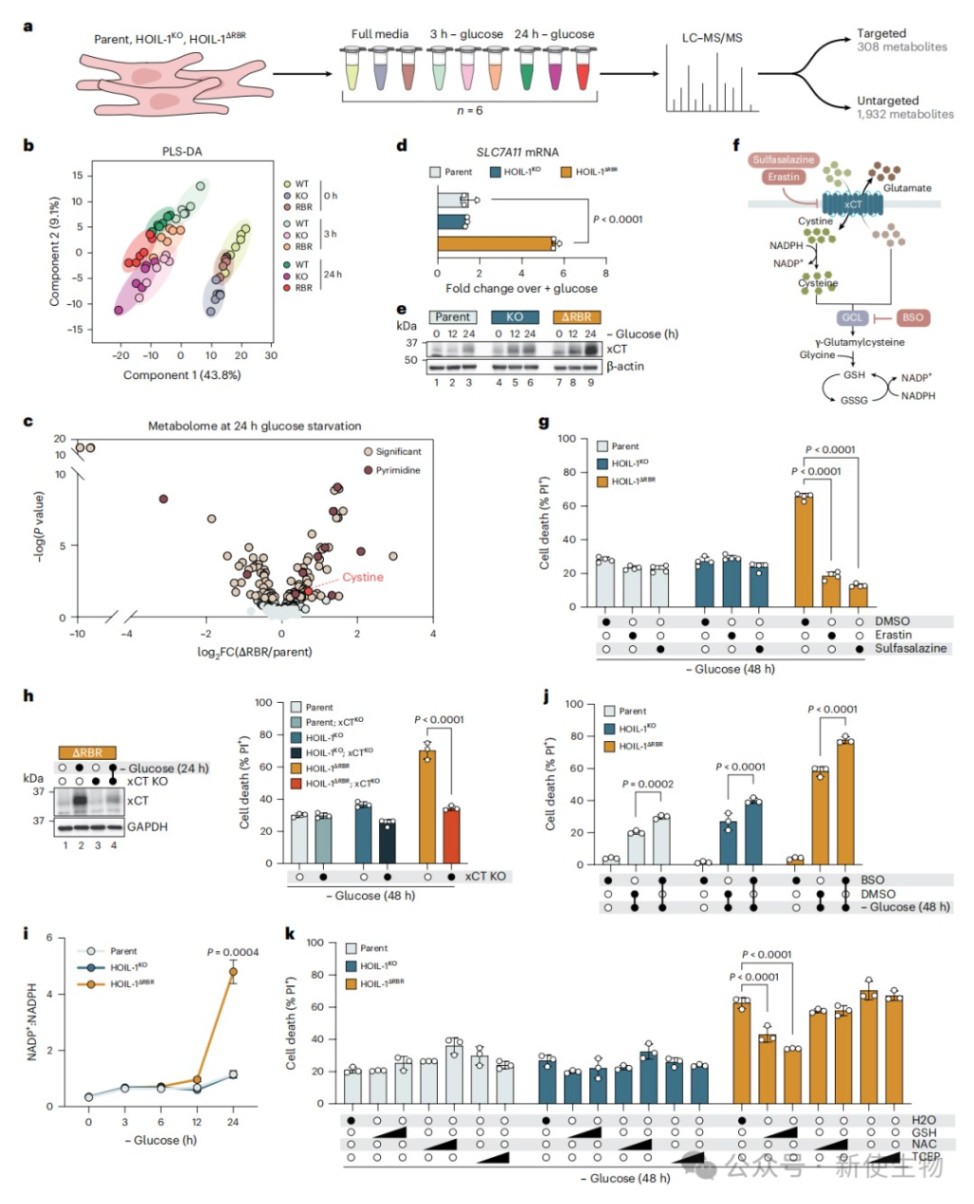
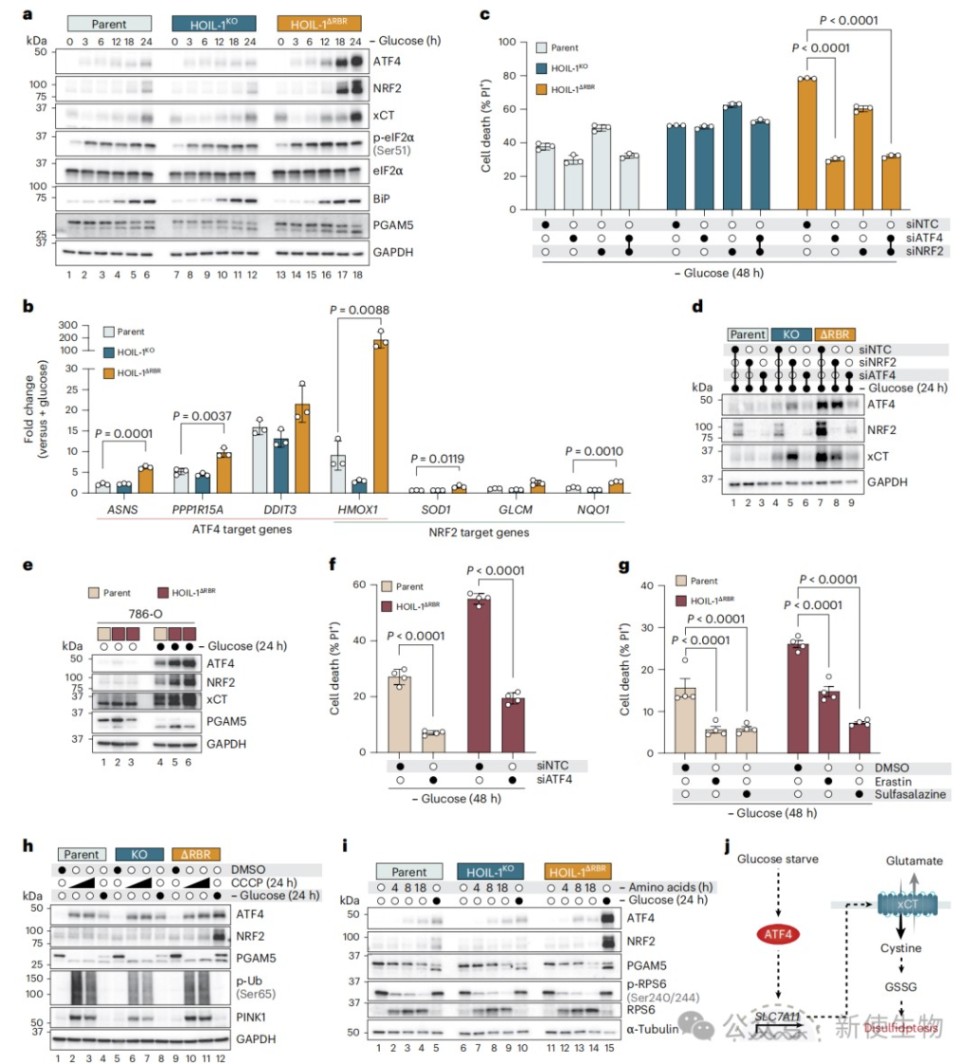
三、ATF4在营养应激下协调xCT依赖性的细胞死亡
通过免疫印迹和RT-qPCR等技术分析转录因子表达情况,作者发现在葡萄糖饥饿期间HOIL-1ΔRBR细胞选择性地激活了整合应激转录因子ATF4及其下游靶基因xCT。
敲低ATF4能显著消除xCT的上调并保护细胞免受双硫死亡,证明ATF4是驱动该致死性代谢网络的核心调控者。
四、核糖体毒性前哨ZAKα感知多聚核糖体停滞并激活ATF4
通过Polysome profiling多聚核糖体分析和靶向激酶抑制实验,研究发现葡萄糖饥饿会导致HOIL-1ΔRBR细胞内翻译停滞并使多聚核糖体崩溃,进而被多聚核糖体应激前哨MAP3K激酶ZAKα感知。
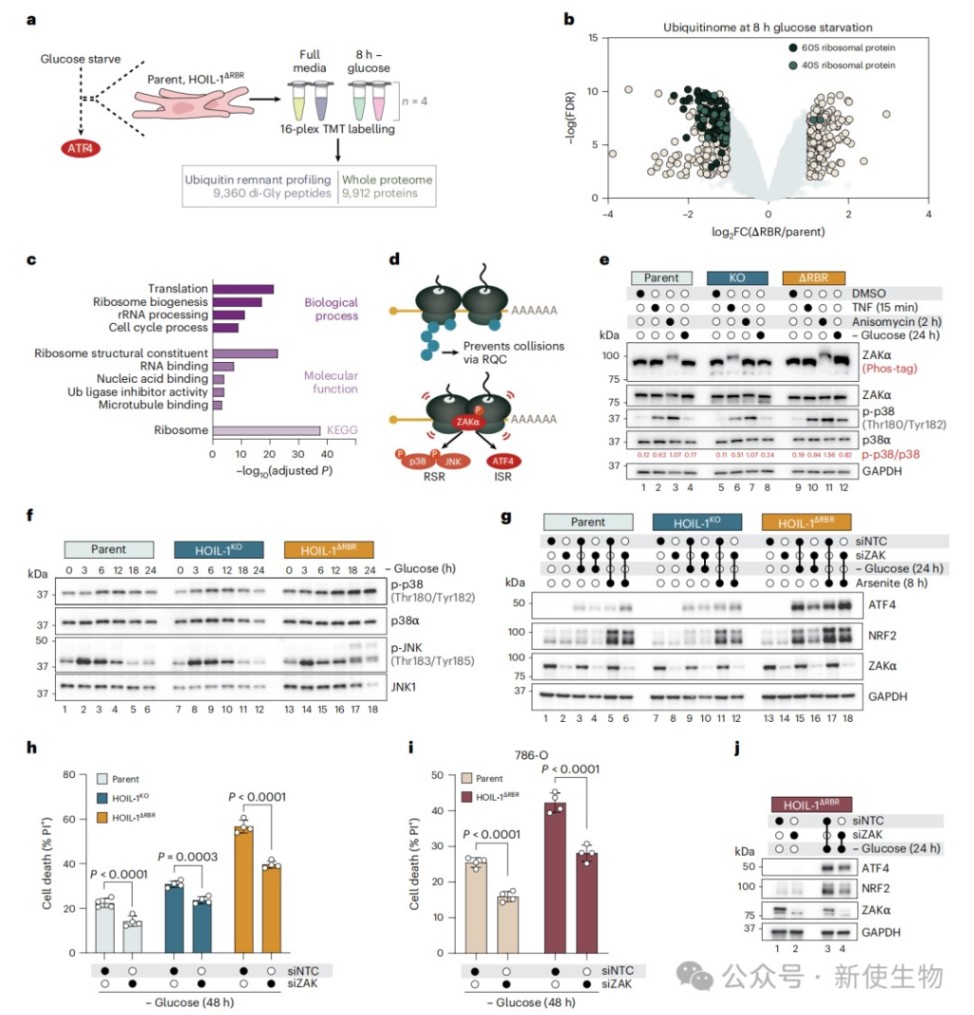
ZAKα的激活不仅诱发p38和JNK磷酸化,还介导了ATF4的翻译和随后的细胞死亡,确立了ZAKα在连接翻译停滞与代谢凋亡中的桥梁作用。
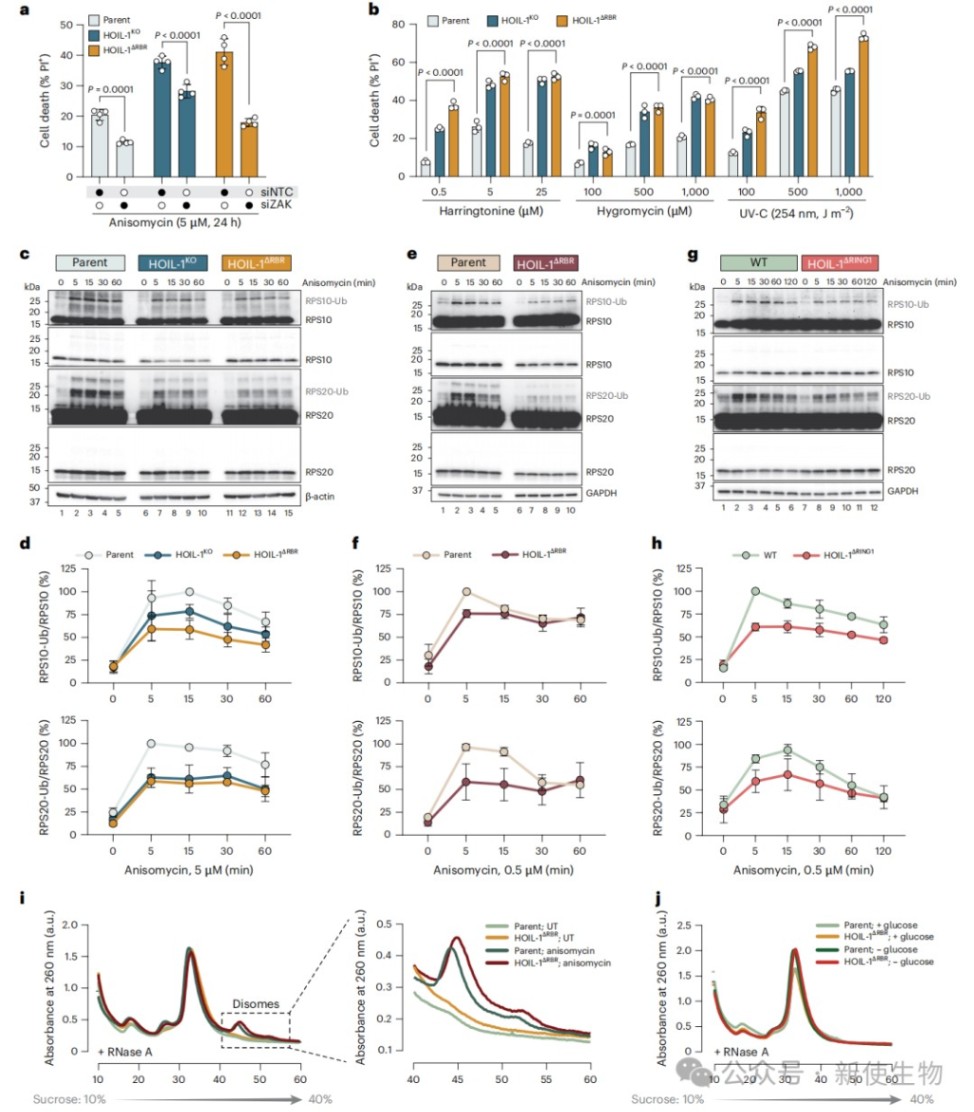
五、突变型HOIL-1重塑核糖体泛素化并破坏质量控制
结合邻近标记技术与质谱技术探究互作组,研究发现截短的HOIL-1作为显性负突变体能结合位于3' UTR的RNA结合蛋白PABPC1,却无法对其进行正常的酯键泛素化修饰。
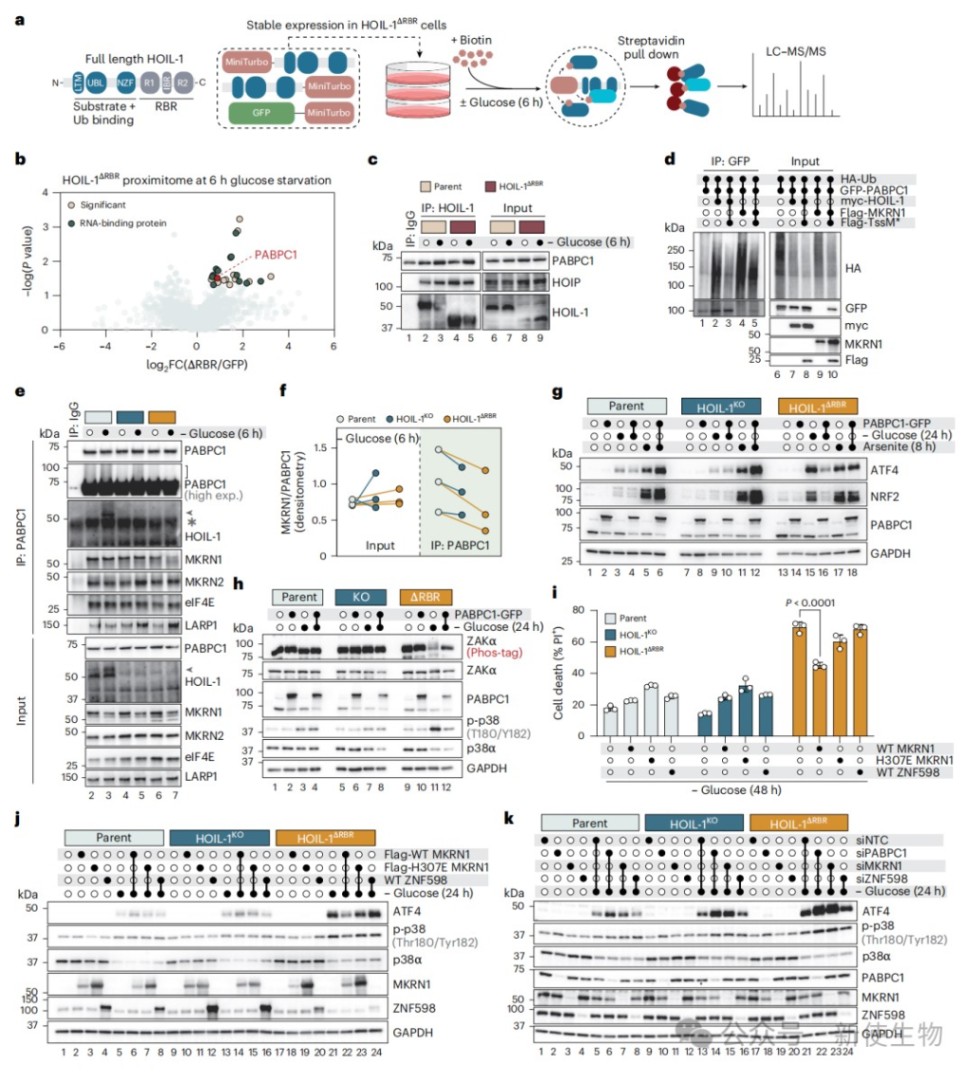
这阻碍了E3连接酶MKRN1的招募与核糖体质量控制(RQC)进程,导致细胞无法处理停滞的多聚核糖体,从而将营养应激转化为致死性的核糖体毒性。
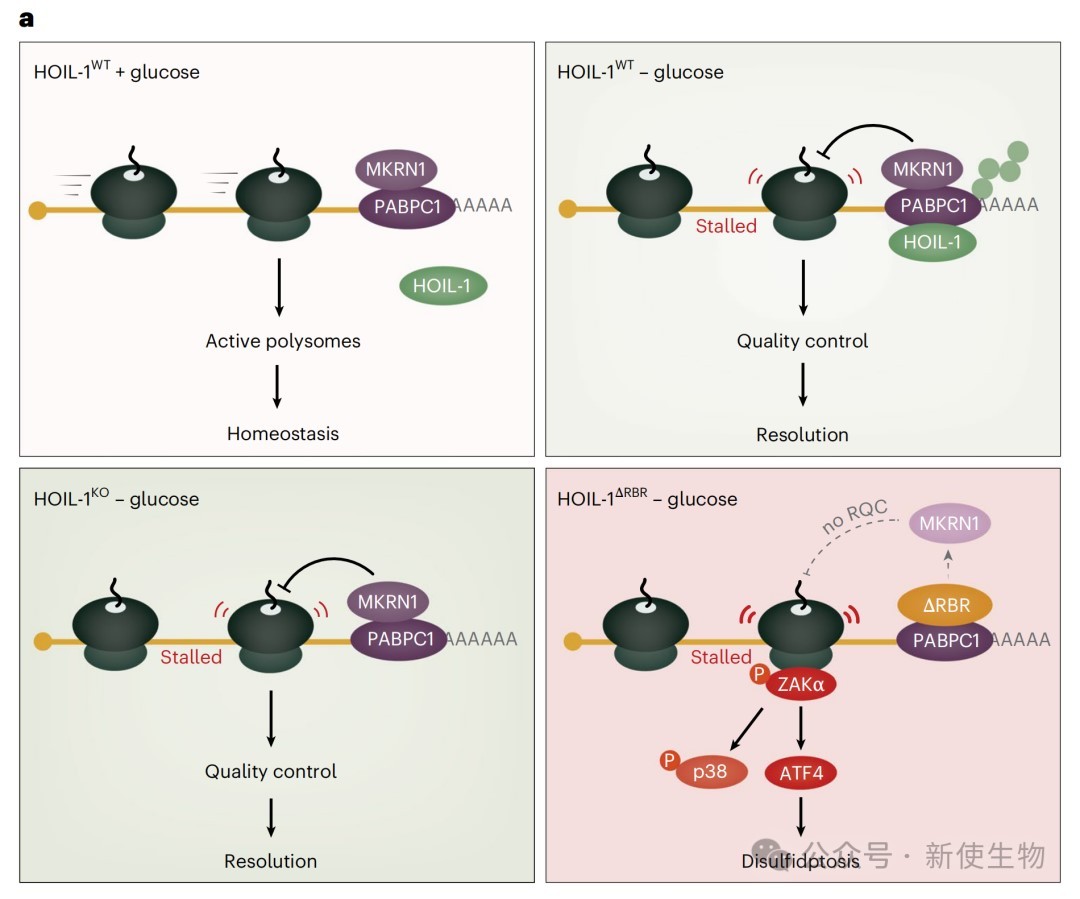
总结
本研究系统揭示了非典型E3泛素连接酶HOIL-1在细胞代谢与翻译应激中保护多聚核糖体免受损伤的核心机制,指出其突变会导致核糖体质量控制失效并引发ZAKα-ATF4信号轴介导的双硫死亡。这些机制的阐明不仅为扩张型心肌病等HOIL-1相关疾病的病理学提供了全新见解,还确立了多聚核糖体作为响应细胞代谢应激关键信号转导平台的地位。
| 新使生物专业翻译组一站式服务平台 |
| 产品名称 |
点击图片查看
点击图片查看


 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们
